 Журнал ЗДОРОВЬЕ ЖЕНЩИНЫ №2(98)/2015
Журнал ЗДОРОВЬЕ ЖЕНЩИНЫ №2(98)/2015
Н.В. Кузьмінова
Вінницький національний медичний університет ім. М.І. Пирогова
У 26 жінок з артеріальною гіпертензією (АГ) та клінічними проявами клімактеричного синдрому вивчено вплив препарату Ноофен®, що додавали до антигіпертензивної терапії, на вегетативні розлади, варіабельність серцевого ритму, добовий профіль артеріального тиску (АТ), якість життя та когнітивні порушення. Установлено покращення показників добового моніторингу АТ, що проявлялось не тільки в нормалізації величин систолічного і діастолічного АТ, а і в достовірному зменшенні варіабельності АТ, порівняно з контролем. Зареєстрована нормалізація вегетативного балансу і варіабельності серцевого ритму, що асоціювалось з позитивною динамікою клінічних проявів вегетативної дисфункції та клімактеричного синдрому, з паралельним покращанням якості життя пацієнток. Отримані результати дозволяють рекомендувати препарат Ноофен® для корекції вегетативних розладів у жінок з АГ в періоди пері- та постменопаузи.
Ключові слова: артеріальна гіпертензія, вегетативні порушення, клімактеричний синдром, варіабельність серцевого ритму, добове моніторування артеріального тиску, якість життя, Ноофен®.
Серед понад 26,3 млн українських жінок приблизно половина (понад 13,2 млн) складають жінки в перехідний та постменопаузальний періоди. Оскільки середня тривалість життя жінки в Україні складає приблизно 72 роки, а середній вік настання менопаузи – 48 років, сучасна жінка проводить третину свого життя в постменопаузі – в період, який супроводжується значним зниженням якості життя за рахунок розвитку широкого спектра вегетосудинних, психоневротичних, урогенітальних порушень та серцево-судинних захворювань [19]. Дослідження останніх десятиліть доводять, що у жінок з настанням менопаузи різко зростає частота виникнення і швидкість прогресування артеріальної гіпертензії (АГ), ішемічної хвороби серця (ІХС), погіршується перебіг серцево-судинних (СС) захворювань, які посідають одне з провідних місць серед причин смерті в розвинених країнах світу [3, 17, 27].
Клімактерій – це період життя жінки, що характеризується загальними віковими інволюційними порушеннями в організмі, на тлі яких відбуваються вікові зміни репродуктивної системи [5]. Безпосередньою причиною розвитку клімактерію є згасання функції яєчників з відповідним зниженням рівнів статевих гормонів (естрогенів, прогестинів, андрогенів) та підвищенням вмісту гонадотропінів. У клімактерії виділяють наступні фази: пременопауза – період від появи перших клімактеричних симптомів до останньої самостійної менструації; менопауза – остання самостійна менструація, що зумовлена функцією яєчників (дату встановлюють ретроспективно: після 12 міс відсутності менструації); перименопауза – період, що об’єднує пременопаузу і 1_й рік після настання менопаузи; постменопауза – починається з менопаузи і закінчується в 65–69 років (прийнято виділяти ранню (до 5 років) та пізню (від 5 до 10 років) постменопаузу [19]. Часові параметри фаз клімактерію деякою мірою є умовними і індивідуальними, проте вони відображують морфо-функціональні зміни в різних ланках репродуктивної системи. Виділення цих фаз є важливим для клінічної практики.
Фундаментом, що визначає перебіг даного періоду за фізіологічним або патологічним типом, є стан адаптаційно-компенсаторних процесів у центральній нервовій системі (ЦНС). Клімактерій, з нейробіологічної точки зору, можна розглядати як поєднання вікових (нейроендокринних, нейромедіаторних, нейрометаболічних) і стрес-індукованих порушень діяльності мозку. У зв’язку з цим, серед клінічно значущих проявів клімактеричного синдрому (КС) виділяють саме порушення зі сторони ЦНС: когнитивні, психоемоційні, вегетативно-регуляторні, больові, астенічні та психосоціальні [5]. Отже, клімактеричний синдром – патологічний стан, що виникає у частки жінок в період клімактерію та є своєрідним симптомокомплексом, що характеризується вегетосудинними, нервово-психічними та обмінно-ендокринними розладами, які пов’язані з гормональною перебудовою і гіпоестрогенемією. Прояви КС визначають у 60–80% жінок при настанні клімактерію, причому до 15% зберігається протягом усього наступного життя [17, 26]. Для правильної діагностики КС слід пам’ятати, що він може розвинутись в пременопаузі та не пізніше 1–2 років після припинення менструацій. У більш пізній період постменопаузи КС виникає вкрай рідко.
Найбільш типовими ранніми симптомами КС є приливи жару до обличчя, голови і верхньої частини тулуба, пітливість, серцебиття, запаморочення, емоційна лабільність, порушення сну, парестезії, втомлюваність. До проявів нейровегетативних симптомів відносяться: головний біль, вестибулопатії, серцебиття в стані спокою, погана переносимість високої температури, мезлякуватість та озноб, відчуття оніміння та повзання «комах», сухість шкіри, пітливість, підвищена збудливість, сонливість та порушення сну, «приливи» жару протягом доби, напади ядухи, симпато-адреналові кризи. Усі ці прояви, що включають нейровегетативні, обмінно-ендокринні та психоемоційні порушення, можуть значно погіршувати якість життя жінки. Зазвичай,
важкість КС визначають за шкалою О.М. Віхляєвої, що враховує кількість «приливів» протягом доби (легка форма – до 10 за добу при загальному задовільному стані та збереженні працездатності; середня – від 10 до 20 «приливів», погіршення загального стану, працездатності, з’являються головний біль, біль у ділянці серця; важка – більше ніж 20 «приливів» та низки інших симптомів, що призводять до часткової чи повної втрати працездатності) або обчислюючи «менопаузальний індекс» Х. Куппермана в модифікації Є.В. Уварової [6, 12, 19, 20].
Патогенез «приливів» вивчений недостатньо. Деякі автори вважають, що гіпоестрогенія в клімактеричний період впливає на центр терморегуляції в ЦНС [2, 12]. Зниження рівня естрогенів в організмі жінки під час клімактерію призводить до зменшення концентрації естрогенів, яка сягає гіпоталамуса. Внаслідок цього, гіпоталамічний центр терморегуляції лишається звичної естрогенної стимуляції з наступним порушенням його функціонування: виникають «приливи» за рахунок надлишкової активації тепловіддачи шляхом вазодилатації і потовиділення [2, 12]. До того ж, «приливи» можуть бути наслідком підвищеної секреції гістаміну при вираженому дисбалансі нейротрансміттерів: гамма-аміномасляної кислоти (ГАМК), серотоніну, ацетилхоліну, дофаміну, норадреналіну [2, 12]. «Приливи» можуть спостерігатися від декількох разів на місяць до багатьох разів на день, що призводить до погіршення настрою, дратівливості, тривоги, зниження концентрації уваги і працездатності. Часті та інтенсивні «приливи» в нічний час можуть викликати безсоння [2, 12].
Отже, в основі розвитку КС лежать дезадаптаційні процеси в ЦНС у цей період, як на нейрональному, так і на системному рівнях [5]. При старінні в цілому і при клімактеричному синдромі зокрема, виникає дисбаланс активності різних нейромедіаторних систем мозку. Так, достатньо добре відомий феномен ослаблення дофамінергічної нейромедіації, на тлі відносної активації адренергічних процесів у період клімактерію, що призводить до розладу діяльності катехоламінергічних систем і сприяє розвитку як вегетативних (припливи, коливання АТ та частоти серцевих скорочень), так і психоемоційних (психастенія, перепади настрою) симптомів. Також важливу роль у розвитку психоемоційних розладів при цьому відіграє ослаблення ГАМК-ергічної нейромедіації, типове як для старіння мозку, так і для естрогенного дефіциту, та пов’язане з ослабленням біосинтезу ГАМК і зі зменшенням ГАМК-рецепторного зв’язування. Саме ці порушення є підгрунтям формування реакції «тривожного очікування», характерної для КС, а при своєму прогресуванні – тривожних розладів, тривожних депресій та панічних нападів [5]. Доведено, що в більшості випадків для стресу характерна функціональна гіперпролактинемія [23]. Підвищена концентрація пролактину пригнічує репродуктивну функцію на різних рівнях: в гіпоталамусі під впливом пролактину зменшується синтез та вивільнення гонадотропін-рилізинг гормону (ГТРГ), знижується чутливість гіпоталамуса до естрогенів; в яєчниках пролактин гальмує гонадотропін-залежний синтез стероїдів, знижує чутливість яєчників до екзогенних гонадотропінів, індукує ранній лютеоліз, знижує секрецію прогестерону жовтим тілом. Клінічно це проявляється зниженням репродуктивного здоров’я жінки, в тому числі настанням раннього клімаксу та важким перебігом клімактеричного синдрому [23]. Проте відомо, що до основних пролактинінгібувальних факторів відносяться дофамін (який безпосередньо пригнічує експресію гена пролактину і стимулює процес кринофагії (автоперероблення гранул вже синтезованого гормону)), гонадотропін-асоційований пептид та ГАМК. Тому достатній рівень цих медіаторів в ЦНС контролює баланс пролактину в організмі [19, 20]. До того ж, певну роль в генезі порушень вищих психічних функцій при КС відіграє ослаблення холінергічних, серотонінергічних, пептидергічних та інших нейромедіаторних систем, що дає підстави вести мову при системний нейромедіаторний дисбаланс, який виникає при КС та потребує особливої фармакотерапевтичної стратегії [5].
Найбільш важко КС перебігає у хворих з СС-захворюваннями, особливо гіпертонічною хворобою (ГХ). У хворих знижується працездатність, скарги різноманітні і здебільшого залежать від основного захворювання, перебіг якого погіршується.
Вегетативні розлади – термін, що об’єднує різноманітні по походженню і проявам порушення вегетативних функцій організму, що зумовлені розладнанням їх нейрогенної регуляції [7]. У свою чергу, вегетативна дисфункція є однією з основних ознак КС. Вегетативна (автономна) нервова система (АНС) бере активну участь у процесах адаптації організму (в тому числі в період клімактерію) та в патогенезі більшості соматичних захворювань [16]. Дисбаланс ланок АНС з підвищенням активності симпатичної і пригніченням парасимпатичної її частини є закономірною реакцією симпатоадреналової системи (САС) на стрес та одним з патогенетичних механізмів виникнення СС-захворювань, в тому числі і в становлення гіпертонічної хвороби (ГХ) [14]. Активація САС призводить до змін в системі нейрогуморальної регуляції (НГР), що відіграє одну з ключових ролей в системі контролю артеріального тиску (АТ) і підтриманні гомеостазу кровообігу [25]. Одним з методів оцінювання стану НГР є аналіз варіабельності серцевого ритму (ВСР), який дозволяє охарактеризувати загальну активність регуляторних механізмів, співвідношення між симпатичним і парасимпатичним відділами АНС та достатньою мірою оцінити параметри, що характеризують вплив АНС на структуру серцевого ритму [1, 24]. Зниження ВСР у хворих з СС-захворюваннями є прогностично несприятливим фактором, що визначає ризик раптової смерті і прогресування захворювання [8].
Клінічні прояви вегетативної дистонії у кардіологічних хворих, в основі яких лежить системний дефект вегетативної регуляції, поліморфні і відображають дисфункцію багатьох органів і систем організму, але найбільш часто проявляються у вигляді емоційно-вегетативних порушень, серцебиття, аритмій, кардіалгій, роздратованості, внутрішнього напруження, тривоги, зниження працездатності, порушень сну та інших, і, як правило, супроводжують органічну патологію СС-системи [14].
Фармакологічна корекція вегетативної активності і нормалізація впливу АНС на діяльність серця може допомогти знизити рівень стресу у хворих з СС-захворюваннями, в тому числі і при ГХ, в становленні і прогресуванні якої стрес відіграє одну з провідних ролей. Також доведена роль хронічного стресу в патогенезі розвитку раннього клімаксу [23]. У комплексній терапії таких хворих найчастіше застосовують седативні засоби, анксіолітики (транквілізатори), нейролептики, ноотропи, антидепресанти [11]. Однак слід зазначити, що багатьом з цих препаратів притаманні властивості, які можуть спричинити міорелаксацію, загальмованість, зниження мислення, сонливість, що обмежує їх використання, особливо на амбулаторному етапі лікування, а також у пацієнток, які ведуть активний спосіб життя [5]. Також є ризик небажаних взаємодій психотропних засобів з препаратами стандартної терапії СС-патології [7]. На сьогодні не існує єдиної думки щодо лікування вегетативних порушень у пацієнтів з ГХ, особливо за наявності КС. Безпосередня участь АНС в становленні і прогресування ГХ зумовлює необхідність комплексного підходу до лікування пацієнтів з ГХ: терапія повинна бути спрямована не тільки на зниження АТ, а і впливати на нормалізацію вегетативної регуляції СС-діяльності. Відновлення балансу між симпатичним і парасимпатичним відділами АНС дозволить попередити ускладнення, та покращити якість життя хворих на ГХ. Украй важливим при визначенні терапевтичної стратегії є поняття як основних патогенетичних ланок вегетативних розладів, так і ефективності і безпечності ліків, що пропонуються.
Система ГАМК головного мозку бере участь у центральній регуляції кровообігу, при її активації спостерігається пригнічення симпатичної активності, зниження АТ [9]. Ослаблення ГАМК-ергічних процесів є суттєвою ланкою розвитку хронічного збудження, і, відповідно, подальшого виснаження нейрональних структур мозку за умов постійного стресорного впливу, з розвитком астенічного синдрому та відіграє певну роль в патогенезі розвитку КС [4, 5]. Тому корекцію таких порушень слід проводити препаратами, що впливають на ГАМК-ергічну передачу, але є цілком безпечними при застосуванні. Певний інтерес з цієї точки зору становить препарат Ноофен® – гідрохлорид бета-феніл-гамма-аміномасляної кислоти, що володіє ноотропними, протитривожними, вегетостабілізувальними та іншими властивостями, але немає тих побічних ефектів, що притаманні класичним транквілізаторам та ноотропам [3, 15, 18]. Відомо, що цей препарат зв’язується в головному мозку тільки з ГАМК-Б-рецепторами, спричиняючи активацію останніх та стимулюючи, таким чином, ГАМК-ергічну медіацію. Дуже важливо, що вікові (в тому числі і при КС) порушення ГАМК-ергічної медіації є пов’язаними саме з недостатністю ГАМК-Б-рецепторів. Таким чином, Ноофен® нормалізує саме ту ланку ГАМК-ергічних процесів, яка найбільшою мірою зазнає впливу вікових та стресових чинників, що є виключно важливим з точки зору патогенезу КС. Ноофену® притаманний м’який транквілізувальний ефект без виявів побічної дії бензодіазепінів [4, 5, 9]. З іншого боку, згідно з сучасними уявленнями, значне зниження концентрації дофаміну в ЦНС при старінні та порушення дофамінергічної медіації є одним з важливих чинників розвитку депресій та когнітивних порушень у людей похилого віку [5]. Одним із чинників, що зумовлює унікальність дії Ноофену®, і з яким можуть бути також пов’язані його катехоламінергічні ефекти, є наявність у його молекулі – бета-фенілетиламіну, який є фізіологічним модулятором дофамінергічної нейромедіації. Бета-фенілетиламін стимулює вивільнення і гальмує зворотне захоплення дофаміну і, тим самим, посилює дофамінергічні впливи. Саме з наявністю описаного механізму пов’язана одна з найбільш характерних клінічних особливостей дії Ноофену® – антиастенічна в поєднанні з психоенергезувальним компонентом без прямого психостимулювального (посилення тривожності, немотивованого збудження, безсоння) ефекту [5]. Продемонстровано, що препарат підвищує фізичну працездатність, усуває психоемоційне напруження, тривожність, страх, покращує сон, чинить анальгезувальний ефект [19, 20]. При цьому покращуються показники вищої нервової діяльності, когнітивних функцій: концентрація уваги, пам’ять, швидкість та точність сенсомоторних реакцій [3, 12, 15, 17, 18, 19, 20, 23]. Таким чином, клініко-фармакологічні характеристики гідрохлориду бета-феніл-гамма-аміномасляної кислоти забезпечують вплив на основні нейромедіаторні ланки патогенезу КС [23]. Однак вплив Ноофену® на прояви вегетативної дисфункції, показники ВСР, параметри добового моніторингу АТ у жінок з АГ та КС потребують подальшого визначення та уточнення.
Мета дослідження: оцінити клінічні прояви вегетативної дисфункції та КС, параметри ВСР та добового моніторингу АТ у жінок с АГ в період пері_ та постменопаузи та їх динаміку під впливом комбінованої терапії із застосуванням Ноофену®.
МАТЕРІАЛИ ТА МЕТОДИ
Проведено обстеження 26 жінок з АГ, віком від 45 до 59 років, середній вік 51,3±5,2 року. ГХ ІІ стадії діагностовано у 21 (80,8%) пацієнтки, ІІІ стадії – у 5 (19,2%). Поєднання ГХ з ІХС мали 5 (19,2%) жінок: стабільну стенокардію напруження ІІ функціонального класу (ФК). Переважна більшість пацієнток (19 (73,1%)) мали 2-й ступінь АГ, 3-й ступень АГ – 7 (26,9%). Хронічна серцева недостатність (ХСН) I стадії (за класифікацією М.Д. Стражеска і В.Х. Василенка (1935 р.) I–II ФК (за критеріями Нью-Йоркської Асоціації серця (NYHA)) була діагностовано у 15 (57,7%) пацієнток, IIА стадії II–III ФК – у 3 (11,5%). Гіпертензивна енцефалопатія І–ІІ ступеня верифікована у 12 (46,2%) хворих. Тривалість АГ становила в середньому 7,5±3,4 року. Діагноз ГХ встановлювали після детального клініко-інструментального обстеження на підставі критеріїв Комітету експертів ВООЗ в умовах стаціонару із застосуванням додаткових методів обстеження, що дозволяли виключити вторинний характер гіпертензії згідно з рекомендаціями Української асоціації кардіологів (2008). У дослідження не включали пацієнток з ГХ, які перенесли інфаркт міокарда або гостре порушення мозкового кровообігу менше 6 міс тому, у яких на момент обстеження були виявлені захворювання печінки або нирок з порушенням функції, цукровий діабет, вади серця, ХСН ІІБ – ІІІ стадії, хронічні обструктивні захворювання легень, дихальна недостатність, онкологічні захворювання.
Прояви КС у обстежених жінок поділялись на вегетосудинні («приливи» жару, озноби, головний біль, запаморочення), психопатологічні невротичного характеру (дратівливість, плаксивість, емоційна лабільність, підвищена втомлюваність, тривожність, порушення сну) та соціально-дезадаптивні (зниження працездатності та життєвого тонусу, звуження кола інтересів).
Початку терапії передував скринінг, ретельний збір скарг та анамнезу, консультації суміжних спеціалістів: окуліста, невролога, гінеколога (разом з яким оцінювали наявність і ступінь важкості КС), отримання інформованої згоди пацієнтки на участь у дослідженні. Усім жінкам проводили обстеження і призначали лікування через 48 год після відміни попередньої антигіпертензивної терапії.
Пацієнткам основної (І) групи призначали гіпотензивну терапію, що складалась із сучасних антигіпертензивних препаратів: інгібіторів ангіотензинперетворювального ферменту або сартанів, антагоністів кальцію, бета-адреноблокаторів, діуретиків в дозах, що були індивідуально підібрані. Крім антигіпертензивної терапії, хворі основної групи вживали Ноофен® (g-аміно-b-фенілмасляної кислоти гідрохлорид, виробництва Olain Farm, Латвія) в добовій дозі 750 мг, що була поділена на 3 вживання: по 1 таблетці 250 мг тричі на день після їди. Термін вживання Ноофену® дорівнював 8 тиж.
Групу порівняння (група ІІ) склали 25 пацієнток з ГХ, що не відрізнялися за віком, статтю, індексом маси тіла, діагнозом, тривалістю АГ, проявами та ступенем важкості КС від жінок основної групи. Пацієнтки ІІ групи також отримували адекватну, індивідуально підібрану, аналогічну за складом антигіпертензивну терапію, що і пацієнтки основної групи, проте без додавання Ноофену®.
Усі пацієнтки, що були включені в дослідження, не отримували замісної гормональної терапії або терапії фітоестрогенами.
Контрольна група включала 30 практично здорових жінок аналогічного віку без ознак КС.
Усім жінкам, що були включені в дослідження проводили клініко-біохімічне обстеження в повному обсязі за сучасними вимогами до призначення лікування та через 12 тиж. від початку лікування.
Оцінювання ефективності лікування проводили на підставі динаміки АТ («дуже добре» – через 2 міс. лікування рівень офісного АТ не перевищував 140/90 мм рт. ст.; «добре» – через 8 тиж. спостереження систолічний АТ (САТ) знижувався на 10 мм рт. ст. і більше, а діастолічний АТ (ДАТ) – на 5 мм рт. ст. і більше; «незадовільне» – зниження САТ менше ніж на 10 мм рт. ст. та/або зменшення ДАТ менше ніж на 5 мм рт. ст., а також на підставі суб’єктивних скарг хворої: головного болю, запаморочення, болю в ділянці серця, загальної слабкості, підвищеної втомлюваності, емоційної лабільності, роздратованості, тривоги, порушень сну.
Для оцінювання динаміки вираженості клінічних проявів КС до та після проведеного лікування визначали модифікований менопаузальний індекс Куппермана [19, 20].
Сприйняття призначеного лікування оцінювали таким чином: «відмінно» – побічні явища протягом періоду спостереження не виникали, «добре» – побічні явища, що з’являлись, не викликали потреби у відміні препарату, «незадовільне» – побічні явища вимагали відміни призначеного лікування.
Перед призначенням комбінованої терапії і до закінчення дослідження всім пацієнткам, а також особам контрольної групи проводили добовий моніторинг АТ (ДМАТ) в реальних життєвих умовах за допомогою амбулаторної системи регістрації АТ – АВРМ_04 («Meditech», Угорщина).
Вимірювання АТ проводили кожні 15 хв в денний період доби (з 6.00 до 24.00) і через 30 хв – в нічний (з 24.00 до 6.00). Визначали середні значення САТ і ДАТ за добу відповідно, в активний і пасивний періоди, показник «навантаження тиском» (індекс часу (ІЧ) гіпертензії), варіабельність АТ, ступінь нічного зниження (СНЗ) АТ і величина його ранкового підвищення (ВРП) [10].
Ступінь важкості вегетативної дисфункції (ВД) визначали за допомогою опитувальника-анкети А.М. Вейна з визначенням кількості балів перед лікуванням та після нього, що заповнювалась пацієнткою самостійно. Сума балів, що перевищувала 15, свідчила про наявність ВД [7].
Вегетативний статус визначали на підставі аналізу ВСР по 5-хвилинному запису кардіоінтервалограми в стані розслабленого неспання в горизонтальному положенні і при вільному диханні після 15 хв адаптації [3]. Регістрацію ВСР проводили за допомогою комп’ютерного електрокардіографа Cardiolab 2000. Стан НГР оцінювали методом часового і спектрального аналізу ВСР, згідно з рекомендаціями Комітету експертів Європейського товариства кардіологів і Північноамериканського товариства стимуляції і електрофізіології (1996). При цьому вивчали такі показники кардіоінтервалограми: частотні – стандартні відхилення середнього значення інтервалів R–R (SDNN) і квадратний корінь із середнього квадратів різниць послідовних інтервалів R–R (rMSSD), відсоток послідовних інтервалів R–R, різниця між якими перевищує 50 мс (pNN50%) та спектральні – загальну потужність спектра – ТР і її складові у доменах дуже низьких частот (0,003–0,05 Гц) – VLF, мс2), низьких (0,05–0,15 Гц) – LF та високих (0,15–0,4 Гц) частот – HF, що відображують відповідно гуморальну, симпатичну та парасимпатичну регуляцію, а також співвідношення (LF/HF, од.) [13]. Згідно з даними Р.М. Баєвського та співавторів (2001), індекс вагосимпатичної взаємодії LF/HF відображує зсув симпато-парасимпатичного балансу в бік переваги симпатичної або парасимпатичної активності.
Усім хворим проведено визначення когнітивних функцій за допомогою шкали оцінки психічного статусу (Mini Mental State Examination – MMSE), що адаптована M. Folstein та співавторами (1985) [3].
Для оцінювання якості життя (ЯЖ) використовували опитувальник Марбурзького університету «General Well_Being Questionnaire» (GWBQ) (J. Siegrist et al., 1989), який включає 8 клінічних шкал: оцінювання пацієнтами свого фізичного самопочуття (I), працездатності (ІІ), позитивного (ІІІ) або негативного (IV) психологічного самопочуття, психологічних здібностей (V), міжособистісних відносин (VI), соціальних здібностей (VII шкала) та 2 питання про настрій та самопочуття протягом останнього тижня [3]. При оцінюванні динаміки GWBQ враховували, що зменшення за І та ІV шкалами та підвищення за рештою шкал свідчать про покращання ЯЖ.
Статистичні розрахунки проводили з використанням пакетів прикладних програм Microsoft Excel, Statistica for Windows 6.0. Результати представлені у вигляді медіани і інтерквартильного розмаху Меd (kvart_1;kvart_3), де Мed – медіана, а kvart_1 – kvart_3 – це 1 і 3 квартилі та персантилі відповідно. Порівняння величин зв’язаних виборок (виборки до і після лікування) проводили непараметричним методом з використанням критерію Вілкоксона [21].
РЕЗУЛЬТАТИ ДОСЛІДЖЕННЯ ТА ЇХ ОБГОВОРЕННЯ
Усі пацієнтки завершили участь у випробуванні згідно з умовами протоколу.
Проведене дослідження свідчить про наявність порушення вегетативної регуляції СС-діяльності у жінок менопаузального віку з АГ. За результатами опитування пацієнток, що були включені в дослідження, практично у 100% спостерігаються ті чи інші клінічні симптоми вегетативної дисфункції. До початку лікування більшість жінок скаржились на відчуття
емоційне напруження, лабільність настрою, підвищену дратівливість, тривогу, порушення сну, підвищену втомлюваність, серцебиття, перебої в роботі серця та симптоми кардіалгії, що зумовлені негативними емоційними впливами. Загальна сума балів, що була розрахована за допомогою анкети-опитувальника А.М. Вейна (1998) перевищувала 15 і дорівнювала в середньому 48,0 (25,0; 56,0). Після проведеного лікування Ноофеном® у більшості пацієнток основної групи відзначено зменшення або повне усунення тривоги, емоційного напруження, нормалізація сну, зменшення кардіалгій, серцебиття та перебоїв у роботі серця на відміну від групи порівняння. Динаміка клінічних проявів вегетативної дисфункції під впливом лікування наведена в табл. 1.
Таблиця 1
Клінічні ознаки вегетативної дисфункції (за анкетою-опитувальником А.М. Вейна, 1998 р.) та їхня динаміка під впливом лікування
|
Клінічні ознаки Клінічні |
І група (основна) (n=26) |
ІІ група (порівняння) (n=25) |
Р |
||||
|
До лікування, n (%) |
Після лікування, n (%) |
D,% |
До лікування, n (%) |
Після лікування, n (%) |
D,% |
||
|
Схильність до почервоніння або блідості обличчя при будь-якому хвилюванні |
19 (73,1) |
6 (23,1) |
-72,2 |
17 (68,0) |
14 (56,0) |
-17,6 |
<0,05 |
|
Оніміння або похолодання пальців кистей, стоп |
18 (69,2) |
5 (19,2) |
-72,2 |
16 (64,0) |
12 (48,0) |
-25,0 |
<0,05 |
|
Чи буває зміна забарвлення пальці кистей стоп |
18 (69,2) |
6 (23,1) |
-66,7 |
15 (60,0) |
12 (48,0) |
-20,0 |
<0,05 |
|
Відчуття серцебиття, "завмирання", "зупинки" серця |
24 (92,3) |
3 (11,5) |
-87,5 |
22 (88,0) |
17 (68,0) |
-22,7 |
<0,05 |
|
Підвищена пітливість ("постійна" або "при хвилюванні") |
19 (73,1) |
4 (15,4) |
-78,9 |
19 (76,0) |
14 (56,0) |
-26,3 |
<0,05 |
|
Відчуття утруднення дихання ("нестачі повітря",прискорене дихання) |
22 (84,6) |
2 (7,7) |
-90,9 |
21 (84,0) |
15 (60,0) |
-28,6 |
<0,05 |
|
Порушення функції травної системи (схильність до запорів,проносів, здуття живота, біль) |
9 (34,6) |
2 (7,7) |
-77,8 |
9 (36,0) |
8 (32,0) |
-11,1 |
<0,05 |
|
Відчуття млості (випадки непритомності або відчуття, що можете знепритомніти) |
11 (42,3) |
1 (3,8) |
-90,9 |
10 (40,0) |
6 (24,0) |
-40,0 |
<0,05 |
|
Напади головного болю (дифузний головний біль, або "половина" голови, "вся голова", біль стискаючого або пульсуючого характеру) |
25 (96,2) |
2 (7,7) |
-92,0 |
24 (96,0) |
12 (48,0) |
-48,0 |
<0,05 |
|
Зниження працездатності, швидка втомлюваність |
25 (96,2) |
2 (7,7) |
-92,0 |
24 (96,0) |
13 (52,0) |
-45,8 |
<0,05 |
|
Порушення сну (труднощі засинання, поверхневий, неглибокий сон з частими пробудженнями, відчуття "нестачі сну",втомленість при пробудженні ранком |
24 (92,3) |
1 (3,8) |
-95,8 |
23 (92,0) |
19 (76,0) |
-17,4 |
<0,05 |
Примітки: D, % – ступінь зміни показників у відсотках до вихідних значень; * – достовірність змін по відношенню до вихідних значень (р<0,05); Р – достовірність змін показників після лікування між двома групами.
Загальна кількість балів за анкетою-опитувальником А.М. Вейна після проведеного лікування становила 15,8 (11,4; 21,6) в основній групі проти 36,4 (23,5; 49,4) в групі порівняння (р<0,05). Отримані дані свідчать про практичне усунення клінічних ознак вегетативної дисфункції під впливом комбінованої терапії із застосуванням Ноофену®.
Клінічними проявами КС у жінок основної групи і групи порівняння були наступні три групи синдромів: вегетосудинні розлади (відчуття припливів жару до голови та верхньої частини тулуба, головний біль, запаморочення, озноб, мерзлякуватість), психопатологічні симптоми невротичного характеру (підвищена втомлюваність, дратівливість, емоційна лабільність, плаксивість, тривожність) та соціально-дезадаптивні проблеми (зниження працездатності, звуження кола інтересів). До початку призначення лікування в жінок основної групи та групи порівняння показник модифікованого менопаузального індексу Куппермана суттєво не відрізнявся і складав 24,3 (22,3; 26,2) та 23,9 (21,8; 26,4) відповідно, р>0,05. Під впливом проведеної терапії із застосуванням Ноофену® суттєво зменшилась важкість проявів КС
по всіх трьох групах синдромів та відбулось покращання загального стану, що підтверджується достовірним (р<0,05) зниженням величини модифікованого менопаузального індексу Куппермана до рівня 16,4 (14,3; 17,1) на відміну від групи порівняння, в якій відзначена лише в тенденція до зниження індексу Куппермана (19,6 (18,1; 21,5), р>0,05) (мал. 1).
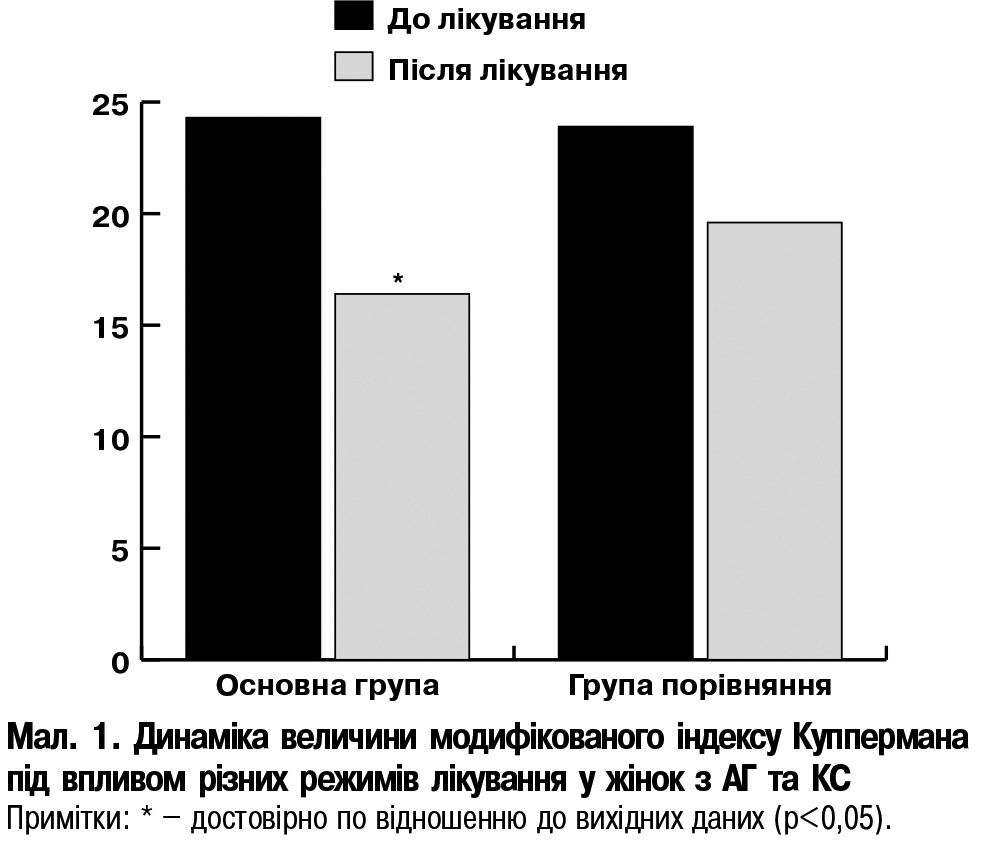
Так, особливо слід відзначити зменшення основних проявів КС, таких, як приливи, пітливість, втомлюваність, серцебиття, емоційна лабільність, безсоння та тривожність під впливом запропонованого лікування з додаванням Ноофену®.
Через 3 міс від початку призначеної терапії в основній групі відзначено зменшення клінічних проявів гіпертензивної енцефалопатії: покращання пам’яті на теперішні події,
зменшення забутливості, підвищення концентрації уваги, зменшення відчуття головного болю та шуму в вухах, запаморочення, загальної слабкості, втомлюваності та порушень сну. Наприкінці дослідження у більшості жінок, які вживали Ноофен®, спостерігалось зменшення когнітивного дефіциту, що підтверджено достовірним збільшенням інтегральніх показників інтелекту. Так, сумарні бали опитувальника MMSE зросли на 24,3% (р<0,05). Отримані дані можуть бути зумовлені наявністю у Ноофену ноотропної, нейропластичної та нейропротекторної дії завдяки його унікальним фармакологічним властивостям [4, 5, 9].
Результати наших досліджень свідчать, що комбінована терапія із застосуванням Ноофену® у пацієнтів з ГХ зменшувала ступінь вегетативного дисбалансу як за даними шкали вегетативної дисфункції (анкети-опитувальника А.М. Вейна), так і за результатами дослідження ВСР до та після проведеного лікування (табл. 2)
Таблиця 2
Динаміка показників ВСР під впливом різних варіантів терапії
|
Показники ВСР |
І група (основна: АнтиГТ+ Ноофен) (n=26) |
ІІ група (порівняння: АнтиГТ) (n=25)
|
Р1-2 |
||||||
|
До лікування |
Після лікування |
D, % |
Р1 |
До лікування |
Після лікування |
D, % |
Р2
|
||
|
SDNN, мс |
77* (41; 103) |
109* (77; 149) |
+41,5 |
0,0002 |
88* (41; 145) |
90* (49; 155) |
+2,3 |
0,51 |
0,0006 |
|
rMSSD, мс |
47 (31; 73) |
61 (49; 99) |
+29,7 |
0,040 |
43 (32; 91) |
39 (32; 51) |
-9,3 |
0,32 |
<0,0001 |
|
pNN50, % |
15* (11; 38) |
19 (9; 39) |
+26,7 |
0,007 |
18 (10; 36) |
20 (12; 27) |
+11,1 |
0,28 |
0,020 |
|
VLF, мс2 |
1384 (984; 2095) |
1036 (915; 1548) |
-25,1 |
0,055 |
1296 (995; 2244) |
1012 (903; 1454) |
-21,9 |
0,057 |
0,15 |
|
LF, мс2 |
1125 (885; 1234) |
1011 (878; 1235) |
-10,1 |
0,48 |
1038 (815; 1309) |
1025 (776; 1218) |
-1,25 |
0,92 |
0,31 |
|
HF, мс2 |
456* (236; 786) |
675 (591; 917) |
+48,0 |
0,002 |
484* (318; 615) |
470* (301; 656) |
-2,9 |
0,25 |
<0,0001 |
|
LF/HF, од. |
2,41* (1,65; 2,88) |
1,52 (1,14; 1,88) |
-36,9 |
0,011 |
2,15* (1,61; 2,72) |
2,18* (1,63; 2,88) |
+1,4 |
0,33 |
<0,0001
|
Проведене оцінювання ВСР у жінок з АГ до призначення терапії виявила наявність дисбалансу вегетативної (автономної) нервової системи, що проявлялось зниженням загальної
активності вегетативної нервової системи (значення показника SDNN), підвищення тонусу симпатичної ланки АНС на фоні пригнічення активності парасимпатичного відділу (HF) та порушенням симпатовагального балансу (LF/HF). Зниження вагусної активності по відношенню до СС-системи і домінування симпатичних впливів можна розглядати як прогностично несприятливий фактор ризику електричної нестабільності серця. Реакція АНС, що супроводжується зниженням високочастотного компонента, на сьогодні розглядається як один з маркерів раптової смерті. Отримані дані збігаються з результатами наших попередніх досліджень та висновками інших дослідників і свідчать про суттєвий вплив АНС на становлення і перебіг захворювання, а також про напруження регуляторних систем у пацієнток з ГХ [14, 15]. Після проведеного лікування із застосуванням Ноофену визначено покращання часових і спектральних показників ВСР, що проявлялось суттєвим підвищенням загальної ВСР (SDNN) на 41,5% (р<0,05), значним збільшенням активності парасимпатичної ланки: величина rMSSD – на 29,7% (р<0,05), компонента HF – на 48,0% (р<0,05) та достовірним зниженням симпатовагального індексу LF/HF на 36,9% (р<0,05) до рівня в контрольній групі у здорових осіб. У групі порівняння, пацієнтки якої отримували індивідуально підібрану антигіпертензивну терапію, за час спостереження не виявлено будь-яких суттєвих змін показників ВСР. Отримані дані свідчать про нормалізацію симпатовагального балансу, відновлення активності парасимпатичної ланки АНС, покращання стану вегетативної та нейрогуморальної регуляції діяльності СС-системи під впливом лікування із застосуванням Ноофену®.
Добрий результат лікування АГ через 2 тиж (зниження АТ до цільових величин – менше ніж 140/90 мм рт.ст.) був досягнутий у 23 хворих (88,5%) основної групи та у 18 (72,0%) – у групи порівняння, задовільний (зниження САТ більш ніж на 10% і/або ДАТ більше ніж на 5%) – у 3 (11,5%) пацієнток основної групи та у 4 (16,0%) – групи порівняння і недостатнє зниження АТ (САТ менше ніж на 10% і/або ДАТ менше ніж на 5%) мало місце у 3 (12,0%) жінок групи порівняння. Отже, додавання Ноофену® до антигіпертензивної терапії сприяє не тільки нормалізації діяльності АНС, але і більш суттєвому і скорішому, проте поступовому зниженню АТ.
Під впливом лікування спостерігалось поліпшення показників ДМАТ як в основній групі, так і в групі порівняння: зменшилися середні величини САТ і ДАТ як за 24 ч, так і в денний і нічний період, істотно знизились рівні пульсового АТ (табл. 3).
Таблиця 3
Динаміка показників добового моніторингу АТ під впливом різних варіантів терапії
|
Показники ДМАТ
|
І група (основна: АнтиГТ+ Ноофен) (n=26) |
ІІ група (порівняння:АнтиГТ) (n=25)
|
Р1-2
|
||||||
|
До лікування
|
Після лікування
|
D, % |
Р1 |
До лікування
|
Після лікування
|
D, % |
Р2
|
||
|
САТ доб, мм рт.ст. |
148,0* (143,0; 165,0) |
121,0 (115,0; 124,0) |
-18,9 |
<0,0001
|
146,0* (141,0; 161,0) |
118,0 (114,0; 125,0) |
-19,2 |
<0,0001 |
0,44 |
|
ДАТ доб, мм рт.ст. |
89,0* (83,0; 95,0) |
72,0 (64,0; 76,0) |
-19,1 |
<0,0001
|
90,0* (82,0; 94,0) |
73,0 (65,0; 77,0) |
-18,9 |
<0,0001 |
0,35 |
|
ПАТ доб, мм рт.ст.
|
64,0* (59,0; 68,0) |
47,0 (42,0; 51,0) |
-26,6 |
<0,0001
|
62,5* (54,0; 69,0) |
46,0 (46,5; 50,5) |
-26,4 |
<0,0001 |
0,46
|
|
ВСАТ доб, мм рт.ст.
|
16,0* (14,5; 19,3) |
13,0 (12,6; 17,0) |
-18,8 |
0,001
|
16,1* (14,3; 18,9) |
14,6 (13,2; 18,0) |
-9,3 |
0,68 |
0,039
|
|
ВДАТ доб, мм рт.ст.
|
14,1* (11,4; 16,1) |
10,1 (10,0; 13,9)
|
-28,4 |
0,010
|
13,8* (12,0; 16,0) |
12,3 (11,2; 14,2)
|
-10,9 |
0,21 |
0,007
|
Зменшились «навантаження тиском» і величина ранішнього підвищення АТ. Привертає увагу вельми істотне зростання ступеня нічного зниження САТ на 84,1% (р=0,012) та ДАТ – на 35,2% в групі хворих, які отримували Ноофен®, що сприяло покращанню добового профілю АТ – збільшенню кількості пацієнток з нормальним добовим профілем АТ-dipper.
Особливо слід зазначити позитивний вплив призначеного лікування з додаванням Ноофену® на показники варіабельності АТ за даними ДМАТ, що проявлялось достовірним зменшенням підвищеної варіабельності АТ протягом усієї доби, порівняно з групою порівняння (табл. 3). Відомо, що підвищення варіабельності АТ є прогностично загрозливою ознакою в плані розвитку СС-ускладнень і відіграє важливу роль в ураженні органів-мішеней [10].
Комбінована терапія з додавання Ноофену® призводила до покращання самопочуття, підвищення розумової та фізичної активності і фонового настрою. Оцінка динаміки показників ПЖ під впливом призначеного лікування показала поліпшення параметрів, що характеризують ЯЖ пацієнток з АГ та КС, особливо в основній групі. Так, зареєстровано зниження показників за I і IV та підвищення за рештою шкал опитувальника ЯЖ (які охоплюють практично всі складові ЯЖ), що також збігається з даними інших дослідників [3]. Відзначено покращання фізичного самопочуття (І шкала) та підвищення працездатності (ІІ шкала). Спостерігалось значне поліпшення психологічної компоненти ЯЖ: психологічних здібностей (V шкала) і психологічного самопочуття (IV шкала). До того ж суттєво зросла здатність до соціальних контактів (VII шкала) (мал. 2).
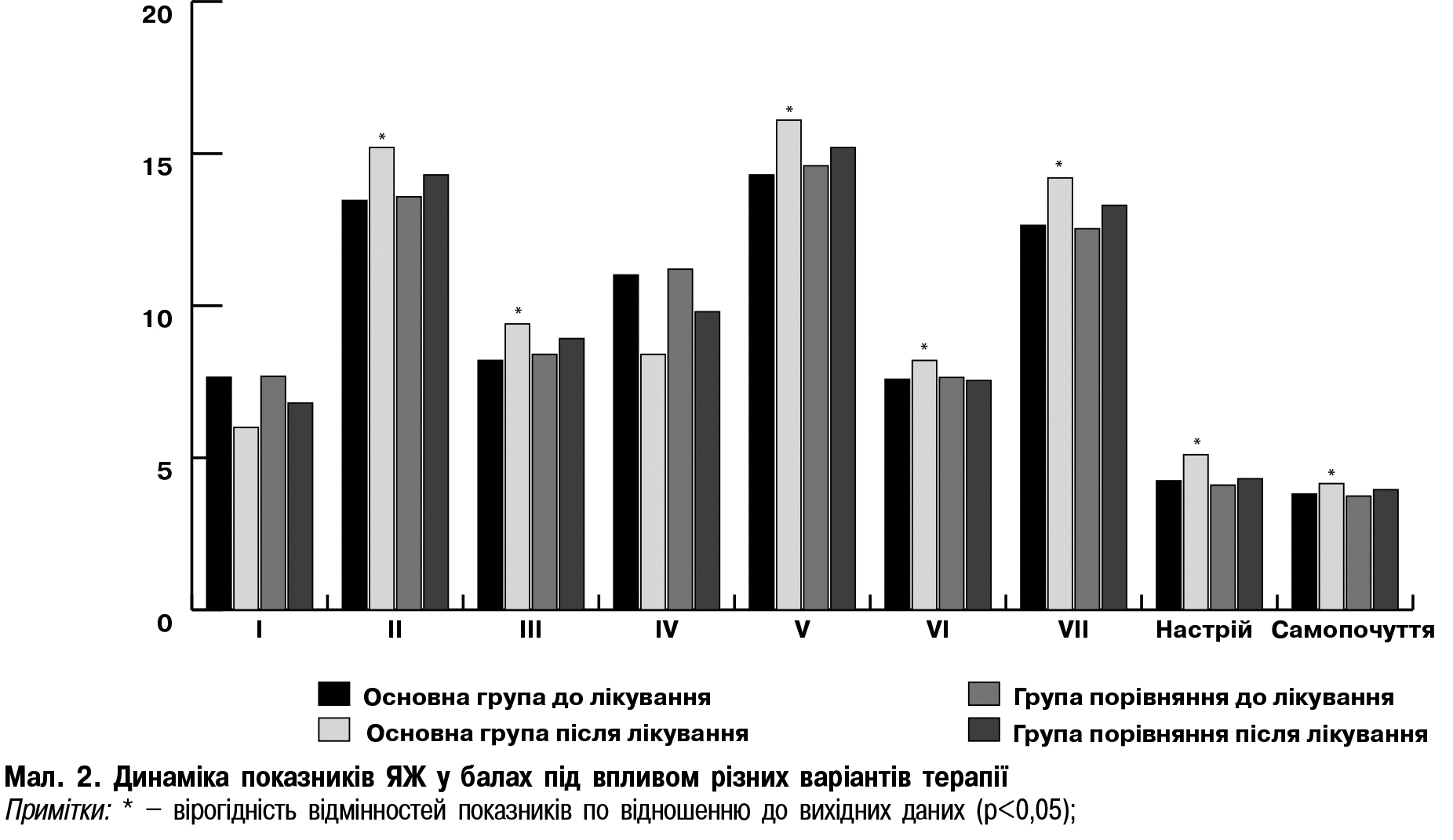
Відзначена метаболічна нейтральність застосованого лікування. Вивчення показників біохімічного гомеостазу не виявило негативного впливу додаткового призначення Ноофену® на біохімічні показники сироватки крові. Слід зазначити, що в групі пацієнток, що додатково отримували Ноофен®, визначено достовірне підвищення рівня загальної антиоксидантної активності плазми на 18,8% (р=0,003) та зниження активності фактора Віллебранда на 26,7% (р<0,0001) порівняно з жінками ІІ групи (р<0,01), що може в свою чергу позитивно вплинути на прогноз захворювання.
Сприйняття призначеного лікування в обох групах обстежених було добрим. Побічні та небажані явища при вживанні Ноофену® не спостерігались. У 3 жінок на початку вживання Ноофену® відзначена сонливість, яка повністю пройшла через 3 доби та не потребувала корекції дози або відміни препарату. Напроти, жінки відзначали добрий сон та покращання самопочуття після пробудження.
Результати нашого дослідження свідчать, що комбінована терапія із застосуванням Ноофену® у жінок з ГХ та КС позитивно впливала на ЯЖ, клінічні прояви КС (зниження частоти
«приливів», зменшення пітливості, почервоніння шкіри, запаморочень, порушень сну), зменшувала ступінь вегетативного дисбалансу як за даними шкали вегетативного тонусу (анкети-опитувальника А.М. Вейна), так і за результатами дослідження ВСР після проведеного лікування. Нормалізація симпатовагального балансу, відновлення активності парасимпатичної ланки АНС, покращання стану вегетативної та нейрогуморальної регуляції діяльності СС-системи, суттєве зменшення варіабельності АТ, позитивні зміни біохімічного гомеостазу, значне поліпшення самопочуття хворих, відсутність небажаних побічних ефектів та добре сприйняття призначеного лікування можуть бути підставою для рекомендації щодо використання Ноофену® (Olain Farm, Латвія) для оптимізації терапії жінок з АГ в період пері_ і постменопаузи та для медикаментозної корекції різноманітних клінічних проявів вегетативної дисфункції та клімактеричного синдрому.
ВИСНОВКИ
1. Застосування Ноофену® у складі комбінованої терапії жінок з артеріальною гіпертензією (АГ) в період пері- та постменопаузи призводить до нормалізації емоційного стану, зменшення клінічних проявів вегетативної дисфункції на тлі клімактеричного синдрому та покращання якості життя пацієнток, що супроводжується добрим сприйняттям призначеного лікування.
2. Комбінована терапія з Ноофеном® у жінок з АГ та клімактеричним синдромом (КС) призводила до суттєвого зменшення частоти найбільш характерних скарг КС, що відображують нейровегетативну складову: «приливів», відчуття жару, пітливості, запаморочення, почервоніння шкіри та порушень сну. Крім того, зареєстроване значне зниження вираженості психоемоційних і ендокринно-метаболічних розладів.
3. Додавання Ноофену® до основної антигіпертензивної терапії зменшує клінічні прояви гіпертензивної енцефалопатії та покращує когнітивні функції: поліпшується пам’ять, підвищується концентрації уваги і швидкість сенсомоторних реакцій.
4. Застосування Ноофену® пацієнтками з гіпертонічною хворобою призводить до відновлення симпатовагального балансу та покращанню показників варіабельності серцевого
ритму, що свідчить про нормалізацію вегетативної і нейрогуморальної регуляції серцевої діяльності.
5. Додавання Ноофену® до комбінованої антигіпертензивної терапії жінок з АГ дозволяє покращити параметри добового моніторингу артеріального тиску (АТ), що проявляється в зменшенні варіабельності АТ та нормалізації добового профілю АТ.
6. Комбінована терапія із застосуванням Ноофену® у жінок з АГ та КС призводить до нормалізації вегетативних розладів, відновлення вегетативного балансу, покращання нейрогуморальної і вегетативної регуляції серцевої діяльності, зменшення варіабельності АТ та нормалізація добового профілю АТ, що, в свою чергу, зменшує загальний кардіоваскулярний ризик. Отримані в ході нашого дослідження результати дозволяють рекомендувати препарат Ноофен® для корекції вегетативних порушень у жінок з КС та АГ.
Продовження подальших досліджень в цьому напрямку, вивчення впливу препаратів, що володіють вегетотропними та стреспротективними властивостями, патогенетично впливають на перебіг як основного захворювання, так і на патологічні стани, що його супроводжують, ретельне оцінювання клініко-біохімічних і вегетативних параметрів, дозволить оптимізувати лікування різних категорій хворих з АГ, покращити якість життя, поліпшити прогноз і знизити ризик СС-ускладнень, що є дуже важливим з практичної точки зору.
Диагностика и медикаментозная коррекция вегетативных расстройств у женщин с артериальной гипертензией в пери- и постменопаузальный периоды
Н.В. Кузьминова
У 26 женщин с артериальной гипертензией (АГ) и клиническими проявлениями климактерического синдрома изучено влияние Ноофена®, который добавляли к антигипертензивной терапии на вегетативные расстройства, вариабельность сердечного ритма, суточный профиль артериального давления (АД), качество жизни и когнитивные нарушения. Установлено улучшение показателей суточного мониторинга АД, что проявлялось не только в нормализации величин систолического и диастолического АД, а и в достоверном уменьшении вариабельности АД, по сравнению с контролем. Зарегистрирована нормализация вегетативного баланса и вариабельности сердечного ритма, что ассоциировалось с положительной динамикой клинических проявлений вегетативной дисфункции и климактерического синдрома, с параллельным улучшением качества жизни пациенток. Полученные результаты исследования позволяют рекомендовать препарат Ноофен для коррекции вегетативных расстройств у женщин с АГ в периоды пери- и постменопаузы.
Ключевые слова: артериальная гипертензия, вегетативные нарушения, климактерический синдром, вариабельность сердечного ритма, суточное мониторирование артериального давления, качество жизни, Ноофен®.
Diagnostics and drug correction of autonomic disorders in women with hypertension in perimenopausal and postmenopausal periods
N.V. Kuzminova
In 26 women with hypertension and clinical manifestations of the climacteric syndrome studied the effect Noofen, which adds to antihypertensive therapy on autonomic dysfunction, heart rate variability, circadian blood pressure profile, quality of life and cognitive impairment. Established improvement in the daily monitoring of blood pressure (BP), which is manifested not only in the normalization of systolic and diastolic blood pressure, and in authentic reduction of variability in blood pressure, compared with the control. Joined normalization of autonomic balance and heart rate variability, which was associated with the positive dynamics of clinical manifestations of autonomic dysfunction and menopausal syndrome, with a parallel improvement in the quality of life of patients. The obtained results of the study allow us to recommend the drug for correction Noofen autonomic disorders in women with hypertension in perimenopausal and postmenopausal periods.
Key words: hypertension, autonomic disorders, menopausal syndrome, heart rate variability, blood pressure monitoring, quality of life, Noofen.
Сведения об авторе
Кузьминова Наталия Витальевна – Кафедра внутренней медицины № 1 Винницкого национального медицинского университета им. М.И. Пирогова, 21018, г. Винница, ул. Пирогова, 56; тел.: (0432) 35-45-49, (050) 442-47-07. E-mail: kuzminova5507@mail.ru
СПИСОК ЛІТЕРАТУРИ
1. Баевский P.M. Вариабельность сердечного ритма: теоретические аспекты и возможность клинического применения / P.M. Баевский, Г.Г. Иванов // Ультразвуковая и функциональная диагностика. – 2001. – № 3. – С. 106–127.
2. Балан В.Е. Новое в лечении климактерического синдрома / В.Е. Балан, Л.А. Ковалева // Женское здоровье. – М.: «Медиа_Медика». – 2012. – Т. 14, № 6. – С. 70–72.
3. Беловол А.Н. Лечение артериальной гипертензии у женщин в постменопаузе / А.Н. Беловол, И.И. Князькова, А.И. Цыганков // Вісник морфології. – 2011. – Т. 17, № 3.
4. Бурчинський С.Г. Перспективи застосування нейротропних засобів як стрес та геропротекторів: препарат Ноофен / С.Г. Бурчинський // Ліки. – 2004. – № 3–4. – С. 7–12.
5. Бурчинський С.Г. Клімактеричний синдром: можливості та перспективи нейрофармакологічної корекції / С.Г. Бурчинський // Ліки, 2006. – № 1–2. – С. 17–24.
6. Вихляева Е.М. Руководство по эндокринной гинекологии / Е.М. Вихляева, под ред. // М: МИД. – 1998. – 385 с.
7. Вейн А.М. Вегетативные расстройства. Клиника, диагностика, лечение / А.М. Вейн // Медицина, Москва. – 1998. – 740 с.
8. Воронков Л.Г. Варіабельність ритму серця та її прогностичне значення у хворих з хронічною серцевою недостатністю / Л.Г. Воронков, Н.В. Богачова // Укр. кардіол. журнал. – 2004. – № 2. – С. 49–52.
9. Громов Л. Фармакологический профиль действия ГАМК_эргических препаратов в ряду психотропных средств / Л. Громов // Вестник фармакологии и психиатрии. – 2001. – № 11. – С. 12–14.
10. Дзяк Г.В. Суточное мониторирование артериального давления / Г.В. Дзяк, Т.В. Колесник, Ю.Н. Погорецкий // Днепропетровск. – 2005. – 200 с.
11. Долженко М.Н. Психокардиология: применение анксиолитиков в лечении сердечно-сосудистых заболеваний / М.Н. Долженко // Therapia. – 2007. – № 10. – С. 35–40.
12. Дубоссарская Ю.А. Возможности оптимизации терапии при вазомоторных пароксизмах у женщин в перименопаузе и постменопаузе / Ю.А. Дубоссарская // Здоровье женщины. – 2013. – № 6. – С. 107–109.
13. Ибатов А.Д. Вариабельность ритма сердца при ортопробе и показатели центральной гемодинамики у больных ишемической болезнью сердца с сопутствующей артериальной гипертензией / А.Д. Ибатов // Рос. кардиол. журнал. – 2004. – Т. 1, № 45. – С. 13–18.
14. Коваленко В.Н. Вариабельность ритма сердца как показатель функции вегетативной нервной системы у больных с сердечно-сосудистыми заболеваниями / В.Н. Коваленко, Е.Г. Несукай, Е.В. Дмитриченко // Укр. кардіол. журнал. – 2006. – № 3. – С. 68–71.
15. Кузьмінова Н.В. Вегетативні розлади у хворих на гіпертонічну хворобу: діагностика та медикаментозна корекція / Н.В. Кузьмінова, В.К. Серкова // Укр. мед. часопис. – 2009. – № 2 (70). – С. 37–41.
16. Морозова О.Г. Вегетативные дисфункции в общесоматической практике / О.Г. Морозова // Здоров’я України. – 2008. – № 3. – С. 51–52.
17. Несукай Е.Г. Диагностика и лечение дисфункции вегетативной нервной системы у женщин с климактерическим синдромом / Е.Г. Несукай // Укр. кард. журнал. – 2012. – № 1. – С. 52–57.
18. Опыт применения «Ноофена» в лечении больных нейроциркуляторной дистонией / Ю.И. Монастырский, В.К. Серкова, Н.В. Кузьминова, Ю.В. Домбровская // Укр. терапевт. журнал. – 2007. – № 4. – С. 84–87.
19. Поворознюк В.В. Вплив Ноофену на клімактеричний синдром та психофізіологічні функції головного мозку в жінок у постменопаузальному періоді / В.В. Поворознюк, О.М. Слюсаренко,Т.В. Орлик // Сучасні принципи діагностики, профілактики та лікування захворювань кістково-м’язової системи в людей різного віку. – К., 2008. – С. 153–156.
20. Поворознюк В.В. Менопауза и костно-мышечная система / В.В. Поворознюк, Н.В. Григорьева. – К., 2004. – 512 с.
21. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA / О.Ю. Реброва // М.: МедиаСфера. – 2006. – 312 с.
22. Рекомендації Української Асоціації кардіологів з профілактики та лікування артеріальної гіпертензії. Посібник до Національної програми профілактики і лікування артеріальної гіпертензії. 4-е
видання, виправлене і доповнене. – К.: ППВМБ, 2013. – 80 с.
23. Татарчук Т.Ф. Стресс и инволюция репродуктивной системы женщины / Т.Ф. Татарчук, О.А. Ефименко, Т.Н. Тутченко // Репродуктивное здоровье женщины. – 2007. – Т. 34, № 5. – С. 153–156.
24. Яблучанский Н.И., Вариабельность ритма сердца у больных с сердечно-сосудистыми заболеваниями / Н.И. Яблучанский, А.В. Бильченко // Укр. кардиол. Журнал. – 1999. – № 5. – С. 71–75.
25. Brook R.D., Julius S. (2000) Autonomic imbalance, hypertension and cardiovascular risk. Amer. J. Hypertension, 13(6 Pt 2): 112S–122S.
26. Kim E.S.H. Status of women in cardiovascular clinical trials / E.S.H. Kim, V. Menon // Arterioscler. Tromb Vasc. Biol. – 2009. – Vol. 29. – P. 279–283.
27. Shaw L.J. Women and ischemic heart disease: evolving knowledge / L.J. Shaw, R. Bugiardini, C.N.B. Merz // J. Amer. Coll. Cardiology. – 2009. – Vol. 54. – P. 1561–1575.
28. Task Force of the European Society ot Cardiology and the North American Society of Pacing and Electrophysiology. Heart Rate Variability. Standarts of Measurements, Physiological Interpretation, and Clinical Use // Circulation. – 1996. – Vol. 93. – P. 1043–1065.

