ЖУРНАЛ КЛІНІЧНА ІМУНОЛОГІЯ. АЛЕРГОЛОГІЯ. ІНФЕКТОЛОГІЯ. СПЕЦВИПУСК № 2 2014
С. В. Зайков, д.м.н., профессор
кафедра фтизиатрии и пульмонологии Национальная медицинская академия
последипломного образования им. П.Л. Шупика, Б.А. Стремедловский Винницкая городская клиническая
больница № 1
Крапивница (КР) представляет собой серьезную медицинскую и социальную проблему в связи с высокой распространенностью, отсутствием до недавнего времени унифицированных подходов к ее диагностике и лечению, большими финансовыми затратами на терапию и реабилитацию, резким снижением качества жизни пациентов [6, 11]. Основными клиническими проявлениями КР является появление типичных обратимых зудящих волдырей (уртикарий) розового или красного цвета, похожих на следы ужаления крапивой или комарами.
Обычно кожный зуд определяется как неприятное субъективное ощущение, возникающее в результате стимуляции кожи или слизистых оболочек каким-либо раздражителем (пруритогеном) и вызывающее рефлекс расчесывания, трения или сбрасывания раздражителя. При этом зуд кожи сопровождается нанесением повреждений в виде расчесов различной степени выраженности, негативно влияет на общее состояние и существенно снижает качество жизни пациентов, вызывая бессонницу, тревожность, депрессию и даже появление суицидальных мыслей.
Часто зуд возникает в области кожи, свободной от высыпаний, может быть изолированным (без высыпаний) и обычно усиливается к вечеру [10, 20]. Волдыри могут возникать на любом участке тела за исключением слизистых оболочек, захватывать большие области тела, достигать гигантских (до 10 см в диаметре) размеров. Часто КР сопутствует ангионевротический отек (АНО), который сопровождается зудом, располагается асимметрично, может сопровождаться болью и жжением, не характерными для изолированной КР [11, 19].
Клиническая картина КР и АНО может изменяться в зависимости от их локализации. Так, отек области шеи и глотки может приводить к дисфагии и диспноэ, стенки кишечника — к рвоте, диарее, абдоминальному болевому синдрому. У пациентов с КР часто наблюдается уртикарный дермографизм, проявляющийся в развитии зуда, эритемы и волдыря в месте штрихового раздражения кожи, возникновение волдырей в местах сдавления кожи нательным бельем, ремнем, браслетами и пр. У части пациентов развитие КР может сопровождаться появлением признаков анафилаксии (снижение артериального давления, респираторные симптомы и симптомы со стороны пищеварительного тракта, стридор и пр.), что требует оказания им неотложной помощи [11, 12].
Общепринятая классификация КР до настоящего времени отсутствует, но на практике она чаще подразделяется на аллергическую и неаллергическую. В соответствии с «Официальным заключением проблемной комиссии по номенклатуре ЕААС1 (2001)», аллергической считается КР, которая опосредована иммунологическими механизмами, а если есть доказательства того, что она обусловлена lgЕ-зависимыми механизмами, то используется название «lgЕ-опосредованная КР».
Клиническая классификация КР предполагает ее разделение по:
- длительности заболевания:
- острая — не более 6 нед;
- хроническая — более 6 нед;
- патогенетическим механизмам:
- иммунологическая, или аллергическая;
- анафилактоидная, или псевдоаллергическая;
- физическая;
- наследственная, другие виды.
КР может быть одним из клинических проявлений различных по патогенезу и прогнозу заболеваний (аллергические, аутоиммунные, онкологические, системные, паразитарные и пр.), что определяет сложности ее классификации, диагностики и терапии.
Основными принципами лечения больных КР в настоящее время являются:
- устранение (элиминация) причинных и провоцирующих факторов;
- фармакотерапия;
- лечение основного заболевания;
- коррекция сопутствующих заболеваний;
- обучение пациентов.
С целью устранения причинных и провоцирующих факторов больные КР в зависимости от ее формы должны соблюдать гипоаллергенную диету с исключением из рациона пищевых продуктов-аллергенов и либераторов гистамина; избегать контакта с другими экзоаллергенами; ограничить влияние физических факторов (физическая нагрузка, холод, тепло и пр.); использовать фотозащитные средства; отказаться от ношения тяжестей, использования ремней, тесной одежды и обуви, купания в холодной воде, употребления холодной еды и напитков и пр. Пациентам с КР необходимо пройти санацию хронических очагов инфекции, дегельминтизацию, курс лечения сопутствующих заболеваний, которые могут вызывать обострение КР. При аллергической КР может быть эффективна аллерген-специфическая иммунотерапия (АСИТ) причинно-значимыми аллергенами [11—13].
Хотя участие гистамина доказано не при всех формах КР, антигистаминные препараты (АГП) остаются главным средством симптоматической терапии и контроля над ее клиническим течением. Связано это с тем, что кожный зуд является наиболее мучительным симптомом при КР различного генеза, а нервные окончания, воспринимающие его, содержат рецепторы, чувствительные к гистамину и некоторым другим химическим веществам (например, к серотонину). Кроме того, гистамин является важным посредником аллергического процесса при КР, а АГП обладают противоаллергическим и противовоспалительным действием, что также играет важную роль в лечении пациентов с КР [7, 8].
Однако многочисленный опыт применения данной группы лекарственных средств со временем продемонстрировал недостаточную их эффективность в отношении купирования зуда кожи, что привело к предположению о наличии целого ряда других биологически активных веществ, помимо гистамина, которые могут участвовать в возникновении данного ощущения. К таким веществам, как указывалось выше, относится серотонин, биологические эффекты которого во многом схожи с гистамином.
В связи с этим в лаборатории академика М.Д. Машковского был синтезирован уникальный класс АГП - хинуклидиновые производные (хифенадин; Фенкарол) и позже — сехифенадин (Гистафен). Кроме того, что данные средства являются эффективными блокаторами Н1-рецепторов гистамина, они также блокируют
5-НТ1-серотониновые рецепторы, в значительной степени ослабляя действие основных медиаторов кожного зуда — гистамина и серотонина [2, 4]. Уникальность хинуклидиновых производных состоит также в том, что они оказывают и антимедиаторное действие, не только блокируя Н1-рецепторы гистамина и
5-НТ1- рецепторы серотонина, но и уменьшают содержание гистамина в тканях путем ускорения его разрушения диаминооксидазой (гистаминазой), которая расщепляет до 30% эндогенного (уже образованного) гистамина [2, 4].
Все это объясняет высокую эффективность хинуклидиновых производных в лечении больных с кожным зудом, причем даже в тех случаях, когда применение других АГП не дает достаточного желаемого результата [16, 17]. Кроме того, эффект при их применении наступает достаточно быстро (уже через 40—60 мин после перорального приема), что дает возможность сразу оценить динамику симптоматики, а при необходимости — увеличить дозу и откорректировать тактику лечения. Полученный во время лечения эффект сохраняется длительно, даже после прекращения приема этого класса лекарственных средств, что выгодно отличает данную группу препаратов от других АГП. Особенностью данных препаратов является и их высокая безопасность: они не обладают снотворным, М-холинолитическим, кардиотоксическим (проаритмогенным) действиями, их эффект не уменьшается при длительном применении.
Важным свойством, о котором следует сказать отдельно, является химическая инертность хинуклидиновых производных, что позволяет использовать их у пациентов с сопутствующей патологией, которые получают другое медикаментозное лечение [2, 4]. Важно, что Фенкарол является препаратом, разрешенным к широкому применению в педиатрической практике (начиная с 3-летнего возраста), безопасность которого доказана более чем 30-летним опытом использования. Фенкарол и Гистафен оказывают не только выраженное противозудное действие продолжительного характера, но и обладают антиэкссудативным, противовоспалительным действиями, снижают явления лихенизации, везикуляции, эритемы, мокнутия кожи, которые часто сочетаются с кожным зудом и присутствуют у пациентов с КР и атопическим дерматитом (АД).
Эффективность и безопасность применения Фенкарола в лечении пациентов с КР и АД была продемонстрирована ранее в ряде клинических исследований. Так, автором работы [9] исследование лечебного действия Фенкарола было проведено среди большого количества пациентов с острой или хронической рецидивирующей КР легкого и среднетяжелого течения, которые находились на амбулаторном лечении и в связи с рецидивами болезни неоднократно принимали АГП. При острой КР и АНО Фенкарол назначали по 50 мг 3 раза в сутки на фоне гипоаллергенной диеты. Через 2—3 дня после начала лечения у больных исчезали кожные проявления без последующих рецидивов (наблюдения в течение нескольких месяцев). У больных хронической КР проявления болезни купировались приемом 2—3 таблеток в течение нескольких суток, но после отмены препарата вновь возникали обострения болезни. Многие пациенты этой группы отмечали лучшую переносимость и большую эффективность Фенкарола по сравнению с другими АГП, особенно I поколения (диазолин, тавегил, супрастин), а также возможность применения небольших доз (1—2 таблеток по 25 мг в сутки) для поддержания ремиссии заболевания [9].
Эффективность и безопасность Фенкарола также была изучена у пациентов с хронической рецидивирующей КР и АД, проходивших лечение на базе отделения иммунопатологии у взрослых ГНЦ РФ Института иммунологии МЗ РФ [19]. Отбор пациентов авторами осуществлялся методом случайной выборки согласно современным критериям диагностики указанных состояний и в соответствии с российскими и международными согласительными документами. Фенкарол назначали по 25 мг 3 раза в сутки в течение 30 дней в комплексе с симптоматической терапией по поводу сопутствующей патологии (при хронической КР) и с базовой терапией АД (топическими глюкокортикостероидными препаратами). Оценка состояния пациентов (с учетом симптомов и жалоб) проводилась на исходном визите (визит 1), на 10-й день (визит 2), 20-й день (визит 3) и 30-й день (визит 4). Все 30 больных, включенных в исследование, получили полный 30-дневный курс лечения.
На 10-й день лечения хороший терапевтический эффект отмечен у 7 больных хронической КР, а у 11 пациентов с АД наблюдали уменьшение кожного зуда и числа высыпаний на коже, улучшился сон по сравнению с исходным состоянием. Одновременно с этим значительно снизилась и выраженность симптомов сопутствующего риноконъюнктивита. На 20-й день лечения хороший эффект был получен у 9 больных хронической КР и у 13 пациентов с АД, отсутствовал эффект терапии лишь у одной пациентки с КР. У остальных больных лечебное действие Фенкарола оценено как удовлетворительное. К 30-му дню лечения у 3 пациентов удалось достигнуть полного исчезновения признаков КР. Отрицательный эффект терапии по-прежнему был у той же пациентки.
Таким образом, у 11 (73,8%) больных хронической КР был получен отличный или хороший результат, у 13 (86,7%) больных АД — хороший и у 3 пациентов с хронической КР и 2 пациентов с АД — удовлетворительный. Очень слабое седативное действие, не требовавшее отмены препарата, наблюдалось только у 2 (6,6%) пациентов. Все пациенты отмечали хорошую переносимость Фенкарола. На основании этих данных автором было сделано заключение о том, что Фенкарол является эффективным АГП в комплексном лечении больных хронической КР и АД, препарат безопасен и хорошо переносится пациентами. Помимо уменьшения кожного зуда и высыпаний у больных с АД он способен эффективно снижать выраженность симптомов риноконъюнктивита, обусловленного бытовой сенсибилизацией [19].
Высокая противозудная активность Фенкарола при лечении АД в острый период у детей без развития у них седативного и снотворного эффекта продемонстрирована С.Н. Недельской и соавт. [15]. Под их наблюдением находились 42 ребенка с АД в стадии обострения. Средний возраст пациентов составил 10±2,6 года. Все пациенты были разделены на 2 группы: 1-я (основная), в которую вошли 24 ребенка, получала традиционную терапию+Фенкарол в возрастной дозировке, и 2-я (сравнения), включающая 18 детей, которых лечили помимо традиционных средств добавлением клемастина в возрастной дозировке. Дети были рандомизированы по полу, возрасту, тяжести течения и обострения АД. Степень тяжести обострения и динамика клинической картины в процессе лечения оценивалась по индексу шкалы SCORAD (Scoring of atopic dermatitis). Выраженность зуда оценивали отдельно по субъективной 10-балльной шкале (ребенка просили отметить на линейке выраженность данного симптома).
Проведенное исследования показало, что регрессирование симптоматики заболевания происходило значительно быстрее в группе детей, получавших Фенкарол, причем к 16-му дню в основной группе наступала полная ремиссия, в то время как в группе сравнения сохранялся зуд выраженностью в 4 балла. В группе пациентов, которые принимали Фенкарол, 96% детей оценили эффект как отличный и хороший, что достоверно (р<0,05) отличалось от результатов лечения с применением клемастина, где аналогичный результат был достигнут только в 67% случаев. Значительное улучшение своего состояния уже на 3-й день после начала приема Фенкарола отметили 54,1% детей, что проявлялось в нормальной дневной активности за счет значительного уменьшения зуда и в спокойном сне. На фоне приема клемастина подобный эффект отмечался только у 17% детей (р<0,05). Ни у кого из детей, получавших Фенкарол, не отмечалось сонливости и других побочных реакций. Таким образом, исследователи пришли к выводу, что Фенкарол является эффективным и безопасным АГП в комплексном лечении детей с АД, приводящим к клинической ремиссии уже через 2 нед от начала применения [15].
Уменьшение клинических проявлений аллергической симптоматики при аллергодерматозах (АД, КР, АНО) наблюдалось у 21 ребенка (в возрасте от 2 до 17 лет) в результате применения Фенкарола в стандартной возрастной дозировке [5]. В зависимости от тяжести состояния Фенкарол принимали в течение 10—20 дней, что приводило к снижению интенсивности зуда, гиперемии, высыпаний и, соответственно, к улучшению сна и качества жизни детей с аллергодерматозами. При необходимости поддерживающую терапию после достижения клинического эффекта продолжали до 1—2 мес.
Большинство пациентов отметили быстрое начало действия Фенкарола: у 35% детей уменьшение выраженности симптоматики происходило в течение 1-х суток, у 63% — на 2-3-й день терапии. Стойкий терапевтический эффект сохранялся на протяжении всего периода лечения, а также после отмены терапии. Параллельно с уменьшением клинических проявлений отмечали улучшение лабораторных показателей крови: снижение уровня эозинофилии и уровня общего IgE (который определяли при помощи иммуноферментного анализа; ИФА) в сыворотке крови. Препарат хорошо переносился, в том числе и при длительном применении. Из побочных эффектов — незначительную сухость слизистых оболочек полости рта, носа и горла отметили только несколько детей, однако это не потребовало отмены препарата; других побочных эффектов не наблюдалось.
Таким образом, лечение препаратом Фенкарол детей с аллергодерматозами показало его высокую эффективность и безопасность, быструю динамику клинической симптоматики, нормализацию лабораторных показателей крови, свидетельствовавших в пользу снижения интенсивности аллергического воспаления. Автор особо отметила отсутствие эффекта тахифилаксии при длительном применении препарата (1—2 мес), что очень важно в педиатрической практике [5].
Сходные результаты были получены А.В. Зубаренко и соавт. [12, 14] при лечении КР и АД у 50 детей в возрасте от 3 до 15 лет. Целью их исследования стало изучение клинической эффективности и профиля безопасности препарата Фенкарол в лечении аллергодерматозов у детей. Все обследованные дети были разделены на 2 репрезентативные группы: 30 пациентов составили основную группу и 20 детей — группу сравнения. Детям основной группы в комплексе с базисной терапией назначался препарат Фенкарол в течение 7—10 дней в возрастной дозировке: от 3 до 12 лет — 10 мг 2—3 раза в сутки, от 12 до 15 лет — 25 мг 2—3 раза в сутки. Пациенты группы сравнения получали традиционную базисную терапию (гипоаллергенная диета, элиминационный режим, мембраностабилизаторы, топические стероиды), а также АГП I поколения (диазолин, тавегил, супрастин).
Динамика клинических данных основной группы и группы сравнения характеризовалась уменьшением зуда, значительным уменьшением вновь возникших волдырей уже через 1,5 ч после приема АГП. В группе детей, получавших Фенкарол, отмечалось более динамичное исчезновение локального отека кожи и слизистых оболочек. Полное исчезновение уртикарных высыпаний отмечалось в основной группе в среднем на двое суток раньше, чем в группе сравнения: на 6-7-е сутки и на 8-9-е сутки соответственно. Клинической динамике соответствовало достоверное снижение уровня эозинофилии крови. Кроме того, установлено, что у пациентов основной группы отмечалось более выраженное улучшение сна, повседневной активности и самочувствия вследствие уменьшения зуда (66,7+8,6% против 35,0+10,6%; р<0,05). Важно также отметить, что повышенной сонливости, заторможенности, нарушения когнитивных функций в группе детей, принимавших Фенкарол, не наблюдалось.
Через 6 нед у пациентов основной группы сохранялось статистически значимое уменьшение зуда по сравнению с группой сравнения (р<0,05), что указывало на стойкость терапевтического эффекта препарата. У больных с АД под влиянием терапии Фенкаролом наблюдалась более быстрая динамика клинической симптоматики и субъективных ощущений кожного зуда (от 8,5 до 1 балла в основной группе и до 2,1 балла в группе сравнения; р<0,001). Величина индекса SCORAD к окончанию лечения составила (24,2±2,3) в основной группе и (30,2±4,3) — в группе сравнения (при исходном значении 52,4±3,9). Качество сна к концу терапии у детей основной группы было достоверно лучше, чем в группе сравнения (р<0,001). В ходе проведения терапии все пациенты хорошо переносили прием Фенкарола, атропиноподобные эффекты не регистрировались, проявлений признаков бронхиальной обструкции не отмечалось. Клинически и электрокардиографически не установлено нарушений со стороны сердечно-сосудистой системы. Таким образом, проведенные клинические наблюдения свидетельствуют о высокой эффективности препарата Фенкарол в схемах лечения аллергодерматозов у детей.
Все вышеуказанное свидетельствует в пользу того, что Фенкарол обладает выраженным антиаллергическим, противовоспалительным, противозудным действием и является более предпочтительным по сравнению с АГП I поколения при лечении взрослых и детей с КР и АД. В связи с этим авторами работ [1, 3, 5, 12, 14—19] Фенкарол был рекомендован в качестве препарата выбора в лечении пациентов с аллергическими дерматозами и прочими кожными заболеваниями, сопровождающимися выраженным кожным зудом.
Собственный опыт применения препарата Фенкарол в лечении пациентов с обострением хронической КР
Нами была изучена эффективность и безопасность применения препарата Фенкарол у пациентов с хронической КР в сравнении с референтным АГП. Исследование было открытым проспективным сравнительным. В основную группу вошли 25 пациентов обоего пола (10 мужчин и 15 женщин), которым был назначен препарат Фенкарол по 25 мг внутрь 3 раза в сутки. К группе сравнения были отнесены также 25 пациентов (9 мужчин и 16 женщин), получавших референтный АГП (левоцетиризин) в дозе 5 мг 1 раз в сутки. Средний возраст обследованных составил 32,09+5,17 и 35,30+4,84 года соответственно. Сопоставляемые группы статистически (р>0,05 для всех случаев) не отличались между собой по полу, возрасту, тяжести заболевания и характеру проводимой терапии.
При первичном обращении за медицинской помощью обследуемым обеих групп был назначен тот или иной АГП. Назначение Фенкарола пациентам основной группы было обусловлено не только задачами нашего исследования, но также и тем, что наличие у Фенкарола дополнительных (антисе- ротониновое и гистаминоразрушающее действие) эффектов, по данным вышеприведенных исследований, способно быстро и эффективно устранять наиболее мучительный для пациентов симптом КР — кожный зуд.
Оценка симптомов КР (интенсивность кожного зуда, наличие высыпаний на коже, их распространенность и выраженность, нарушение сна в баллах), а также развития возможных побочных эффектов терапии проводилась нами в течение 30 дней при помощи ежедневного анкетирования пациентов, заполнения ими дневника самонаблюдения, а также во время их контрольных визитов к врачу. Тридцатидневный курс терапии пациентов с обострением хронической КР был обусловлен тем, что для данного заболевания характерно рецидивирующее течение, а рецидивы данной патологии чаще могут наблюдаться после краткосрочных курсов терапии и отмены АГП. Все обследуемые прошли собеседование и подписали лист информированного согласия на участие в исследовании, женщины были опрошены на предмет возможной беременности.
Критерии включения:
- клинические симптомы КР (уртикарные высыпания, сопровождающиеся кожным зудом, нарушением сна, общего состояния, психологического статуса, утомляемость, снижение дневной активности);
- длительность заболевания более 6 мес;
- возраст от 19 до 50 лет;
- отсутствие тяжелого течения КР;
- информированное согласие пациентов на участие в исследовании;
- отсутствие тяжелых сопутствующих заболеваний печени, почек, сердечно-сосудистой и дыхательной систем, хронического алкоголизма, наркомании, аутоиммунных заболеваний, ВИЧ/СПИДа, а также беременности и лактации.
Критерии исключения:
- прием топических и системных глюкокортикостероидов;
- прием иммуностимулирующих средств и иммунодепрессантов;
- прием других АГП;
- неспособность пациента выполнять врачебные назначения;
- нежелание пациента принимать участие в исследовании;
- одновременное участие пациента в другом клиническом исследовании;
- возраст до 19 и старше 50 лет;
- необходимость в назначении нерекомендованных методов лечения.
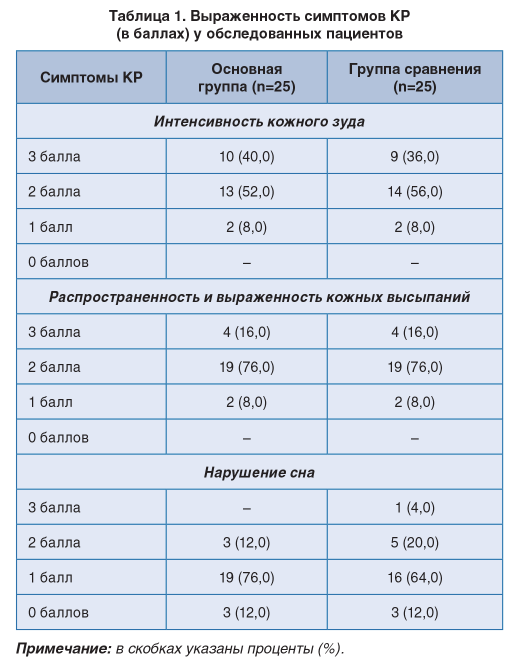
Оценка тяжести симптоматики обострения КР проводилась нами по 3-балльной шкале (0 — симптомы отсутствуют, 1 — симптомы выражены слабо, 2 — симптомы выражены умеренно, 3 — симптомы выражены сильно). Как мы указывали выше, степень выраженности симптоматики КР в обеих группах пациентов была сравнимой (р>0,05 для всех случаев). Так, чаще всего у них выявлялись симптомы, выраженность которых можно было оценить в 2 или 3 балла, что указывало на наличие у всех обследованных признаков обострения КР. Балльная оценка выраженности основных симптомов КР приведена в табл. 1.
Все пациенты, принимавшие участие в исследовании, были проинструктированы относительно применения препаратов и необходимости проведения самостоятельной оценки самочувствия. Она проводилась при помощи ежедневного опроса (анкетирования) пациентов, заполнения ими дневника самонаблюдения, а также во время их контрольных визитов. В течение исследования учитывались выраженность жалоб и симптомов КР на исходном визите (визит 1), на 10-й (визит 2), 20-й (визит 3) и 30-й день (визит 4). При этом врач-исследователь детально изучал данные дневника самонаблюдения пациента, оценивал выраженность клинических симптомов и побочные эффекты терапии, определяя их возможную связь с приемом Фенкарола или референтного препарата. При этом все полученные в процессе обследования пациента данные сопоставлялись между собой, а полученные результаты фиксировались в амбулаторной карте больного.
Динамика основных симптомов КР в процессе терапии у пациентов основной группы и группы сравнения представлена в табл. 2.
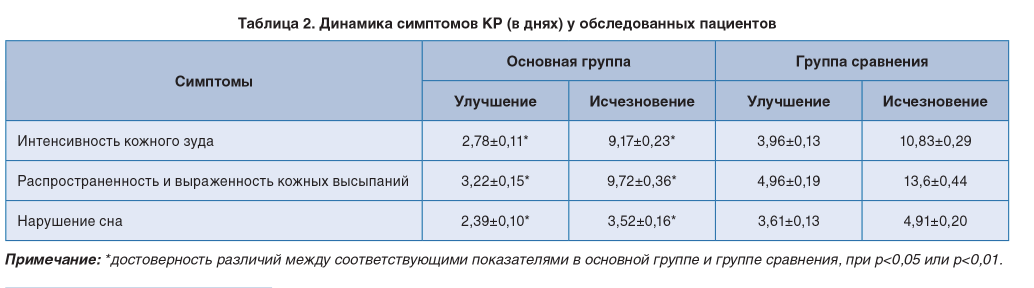
Результаты ежедневного анкетирования пациентов, заполнения ими дневника самонаблюдения, а также их контрольных визитов к врачу продемонстрировали, что у пациентов основной группы положительная динамика клинических признаков обострения КР (интенсивность кожного зуда, распространенность и выраженность кожных высыпаний, нарушение сна) отмечалась в существенно более короткие сроки (р<0,05 и р<0,01 для всех случаев). Так, уже через 2,78+0,11 дня после начала приема Фенкарола у пациентов основной группы нами отмечено существенное снижение выраженности кожного зуда, что наступило у обследованных из группы сравнения через 3,96+0,13 дня (р<0,01). Полностью кожный зуд был купирован у пациентов основной группы также быстрее, чем у обследованных из группы сравнения (через 9,17+0,23 и 10,83+0,29 дня соответственно, при р<0,05).
Распространенность и выраженность кожных высыпаний значительно уменьшились в основной группе через 3,22+0,15 дня, а в группе сравнения — через 4,96+0,19 дня (р<0,01). Полностью кожные высыпания исчезли у пациентов основной группы также значительно быстрее, чем у обследованных из группы сравнения (через 9,72+0,36 и 13,6+0,44 дня соответственно, при р<0,01). Аналогичным образом у пациентов группы сравнения улучшение и нормализация сна отмечены через 2,39+0,10 и 3,52+0,16, а у обследованных в группе сравнения — через 3,61+0,13 и 4,91+0,20 дня соответственно, при р<0,05 для обоих случаев.
Следовательно, включение в режим терапии пациентов с обострением хронической КР препарата Фенкарол по сравнению с референтным препаратом (левоцетиризин) позволило в существенно более короткие сроки купировать основные и наиболее мучительные (интенсивность кожного зуда, распространенность и выраженность кожных высыпаний, нарушение сна) патологические симптомы данного заболевания.
Кроме эффективности нами также была изучена безопасность применения Фенкарола и референтного препарата у 50 пациентов с обострением хронической КР. В нашем случае побочные реакции были отмечены у 1 из 25 (4,0%) пациентов основной группы и также у 1 из 25 (4,0%) обследованных из группы сравнения. В первом случае это был слабый седативный эффект, а во втором — сухость во рту, тошнота и расстройства стула. В обоих случаях отмены препаратов и проведения дополнительных медицинских мероприятий не потребовалось. В дальнейшем все пациенты продолжили применение терапии и не отказались от участия в исследовании.
В заключение следует еще раз отметить, что КР остается частой и нередко трудно решаемой мультидисциплинарной проблемой. Лечение пациентов с КР требует комплексного и индивидуального подхода. Существенными преимуществами среди АГП в лечении КР, сопровождающихся интенсивным кожным зудом и уртикарными высыпаниями, обладают средства не только с антигистаминным, но и антисеротониновым действием, а также способные дополнительно разрушать эндогенный гистамин. Именно к таким препаратам и относится Фенкарол, что позволяет широко использовать его для лечения пациентов различных возрастных групп.
Литература
- Антоньев, АА Фенкарол в лечении кожных заболеваний [Текст] / А.А. Антоньев, Л.К. Горяйнов, С.Н. Попова // Патогенез, клиника и лечение некоторых дерматозов. — Свердловск-Горький. — 1977. - Вып. 13. - С. 56-61.
- Белан, Э.Б. Антигистаминные производные хинуклидинов [Текст] / Э.Б. Белан, М.В. Гутов // Клиническая дерматология и венерология. — 2010. — № 5. — С. 1 -7.
- Белан, Э.Б. Профилактика нежелательных поствакцинальных явлений у детей с атопическим дерматитом [Текст] / Э.Б. Белан, М.В. Іутов, Л.В. Лабай // Российский аллергологический журнал. - 2006. - № 4. - С. 1 -4.
- Влияние антигистаминного препарата фенкарол и других хинуклидинлкарбинолов на активность тканевых аминооксидаз [Текст] / ЭА. Бауманис, В.З. Горкин, И.Э. Калниня [и др.] // Фармакол. и токсикол. - 1980. - № 1. - С. 36-40.
- Головин, Р.Р. Досвід використання препарату фенкарол при алергічній патології у дітей [Текст] / Р.Р. Головин // Укр. мед. часопис. - 2009. - № 3 (71). - У/УІ. - С. 48-50.
- Господарський, І.Я. Порівняльна ефективність застосування антигістамінних засобів у пацієнтів з ^Е-залежною кропів’ян- кою [Текст] / І.Я. Господарський, І.П. Мельничук, Х.О. Господарська // Український терапевтичний журнал. - 2013. - № 4. - С. 107-111.
- Гущин, И.С. Аллергическое воспаление и его фармакологический контроль [Текст] / И.С. Гущин. - М.: Фармарус Принт. - 1998. - 252 с.
- Гущин, И.С. Потенциал противоаллергической активности и клиническая эффективность Н1-антагонистов [Текст] / И.С. Гущин // Аллергология. - 2003. - № 1. - С. 37-44.
- Гущин, И.С. Фенкарол антигистаминный препарат. Значение в современной клинической практике и рекомендации по применению [Текст] / И.С. Гущин, М.Э. Каминка // Москва. - 2009. - 32 с.
- Зайков, С.В. Дифференциальная диагностика и лечение кожного зуда [Текст] / С.В. Зайков // Здоров’я України. - 2014. - № 1 (25), лютий. - С. 46-47.
- Зайков, С.В. Острая крапивница и отек Квинке: клиника, диагностика, неотложная помощь [Текст] / С.В. Зайков // Здоров’я України. - 2010. - № 4, грудень. - С. 40-41.
- Зубаренко, А.В. Лечение аллергодерматозов в педиатрической практике [Текст] / А.В. Зубаренко, Т.В. Стоева, Л.В. Решетило // Материалы IV Юбилейной международной конференции АО «Оіаіп- farm». - Латвия, Рига. - 12 октября 2012. - С. 42-46.
- Кузнецова, Л.В. Опыт применения антигистаминных препаратов в лечении различных видов аллергии / Л.В. Кузнецова // Ліки. - 2003. - № 3 -4. - С. 1 -7.
- Лечение аллергодерматозов в педиатрической практике в регионе Северного Причерноморья с применением антигистаминного препарата фенкарол [Текст] / А.В. Зубаренко, О.А. Портнова, В.В. Скрипник [и др.] // Вісник морської медицини. - 2009. - № 1. - С. 41-44.
- Лечение атопического дерматита в острый период [Текст] / С.Н. Недельская, Е.Д. Кузнецова, И.В. Солодова [и др.] // Український журнал дерматології, венерології і косметології. - 2008. - № 3. - С. 34-37.
- Лусс, Л.В. Антигистаминные препараты - производные хинуклидина при аллергических заболеваниях. В чем преимущество? [Текст] / Л.В. Лусс, Н.В. Шартанова // Терапевтический архив. - 2013. - № 1. - С. 1 -4.
- Лусс, Л.В. Выбор антигистаминных препаратов в лечении аллергических и псевдоаллергических реакций [Текст] / Л.В. Лусс // Астма та алергія. - 2010. - № 1 -2. - С. 1 -7.
- Опыт применения нового отечественного противогистаминного препарата - фенкарола - в дерматологии [Текст] / К.К. Борисенко, Ю.С. Бутов, Н.Г. Короткий [и др.] // Вестник дерматологии и венерологии. - 1977. - № 4. - С. 72-75.
- Феденко, Е.С. Фенкарол в комплексной терапии атопического дерматита и хронической крапивницы [Текст] / Е.С. Феденко // Аллергия, астма и клиническая иммунология. - 2003. - № 6. - С. 10-12.
- Чебуркин, АА. Зуд: симптом, синдром, болезнь [Текст] / А.А. Чебуркин // Аллергология и иммунология в педиатрии. - 2006. - № 2 -3. - С. 26-33.

