ЖУРНАЛ НЕВРОЛОГІЇ ім. Б.М. МАНЬКОВСКОГО 2015, ТОМ 3, № 4
С. М. Кузнецова, В. В. Кузнецов, Д. В. Шульженко, В. П. Чижова, М. С. Егорова, А. Г. Скрипченко
ГУ «Институт геронтологии им. Д.Ф. Чеботарева НАМН Украины», г. Киев
Эндотелий — маэстро кровообращения.
Дж. Вейн, 2001 г.
Резюме. В статье представлены результаты сравнительного анализа влияния препаратов Капикора и Милдроната в комплексном клинико-инструментальном обследовании 45 пациентов пожилого возраста (средний возраст 64,з±з,8 года) с дисциркуляторной атеросклеротической энцефалопатией I-II ст. (ДЭ). Первая группа (25 пациентов) получала препарат Капикор по 2 капсулы 2 раза в день (30 дней); вторая группа (20 пациентов) получала препарат Милдронат 500 мг по 1 капсуле 2 раза в день (30 дней).
У больных ДЭ I-II ст. под влиянием Капикора улучшается долговременная память, внимание, церебральная гемодинамика за счет увеличения ЛССК преимущественно в экстракраниальных сосудах каротидного бассейна и уменьшения индексов периферического сопротивления в отдельных сосудах головного мозга, а также вследствие улучшения капиллярного кровообращения. Капикор повышает функциональную активность эндотелия, вызывает реорганизацию структуры биоэлектрической активности головного мозга, уменьшая мощность медленных ритмов на фоне увеличения частоты и мощности в диапазоне альфа-ритма. Капикор нормализует вегетативную регуляцию сердца за счет активизации парасимпатического звена вегетативной нервной системы и повышает уровень ауторегуляции мозгового кровообращения.
Ключевые слова: пациенты пожилого возраста, дисциркуляторная атеросклеротическая энцефалопатия, Капикор, Милдронат.
В настоящее время цереброваскулярные заболевания представляют одну из наиболее актуальных проблем современной неврологии, учитывая высокую распространенность этой патологии. Наиболее частое проявление цереброваскулярных заболеваний — дисциркуляторная энцефалопатия (ДЭ) [8]. Основными факторами, приводящими к развитию ДЭ, являются атеросклероз, сахарный диабет и артериальная гипертензия [13]. Дисфункция эндотелия рассматривается как важное звено в патогенезе хронической ишемии мозга и, в частности, атеросклеротической дисциркуляторной энцефалопатии [10, 16, 20].
Согласно современным представлениям, эндотелиальные клетки — автономный сердечно-сосудистый эндокринный орган с выраженной метаболической активностью, выполняющий ряд важнейших функций [14, 29, 30, 32]. Эндотелиоциты синтезируют факторы, влияющие на тонус гладкой мускулатуры, гемостаз, пролиферацию, ангиогенез, иммунную систему (табл. 1) [5, 22].
К настоящему времени установлена роль эндотелия в поддержании гомеостаза путем сохранения динамического равновесия между разнонаправленными процессами [3, 17, 28]. Эндотелий участвует в:
- регуляции вазодилятации и вазоконстрикции, высвобождении сосудорасширяющих и сосудосуживающих факторов, модулировании сократительной активности гладкомышечных клеток;
- поддержании гемостаза (синтез и ингибирование факторов агрегации тромбоцитов, факторов фибринолиза, про- и антикоагулянтов);
- регуляции иммунной системы (выработка про- и противовоспалительных факторов, регуляция сосудистой проницаемости, активности Т-лимфоцитов);
- процессах ремоделирования сосудов (синтез и ингибирование факторов пролиферации, ангиогенез).
Механизмы, определяющие эндотелиальную дисфункцию, — это нарушение биодоступности N0 за счет снижения синтеза N0; уменьшение плотности на поверхности эндотелиальных клеток мускариновых и брадикининовых рецепторов; увеличение деградации N0; повышение эндотелиальными клетками вазоконстрикторных веществ, в частности эндотелина-1; нарушение целостности эндотелия, что ведет к непосредственному взаимодействию циркулирующих веществ с гладкомышечными клетками, вызывает их сокращение и повышение активности АПФ на поверхности эндотелиальных клеток [3, 6, 18, 31].
Таблица 1 Факторы, синтезируемые эндотелиоцитами и регулирующие их функцию
|
Факторы, влияющие на тонус гладкой мускулатуры |
|
|
Констрикторы |
Дилататоры |
|
Эндотелин |
Оксид азота |
|
Ангиотензин ІІ |
Простациклин (PGI2) |
|
Тромбоксан А2 |
Ацетилхолин |
|
|
Эндотелиальный фактор деполяризации (EDHF) |
|
Факторы гемостаза |
|
|
Протромбогенные |
Антитромбогенные |
|
Тромбоцитарный ростовой фактор (PDGF) |
Оксид азота |
|
Ингибитор активатора плазминогена |
Тканевой активатор плазминогена |
|
Фактор Виллебранда |
Простациклин (PGI2) |
|
Ангиотензин IV |
|
|
Эндотелин-1 |
|
|
Факторы, влияющие на рост и пролиферацию (ангиогенез) |
|
|
Стимуляторы |
Ингибиторы |
|
Эндотелин-1 |
Оксид азота |
|
Ангиотензин II |
Простациклин (PGI2) |
|
Супероксидные радикалы |
С-натрийуретический пептид |
|
Факторы, влияющие на воспаление и иммунную систему |
|
|
Стимуляторы |
Ингибиторы |
|
Фактор некроза опухоли |
Оксид азота |
|
Супероксидные радикалы |
С-натрийуретический пептид |
Важным биологически активным веществом, вырабатываемым эндотелием, является оксид азота, характеризующийся широким спектром биологического действия. Эндоте- лийзависимая вазодилятация связана с синтезом в эндотелии преимущественно трех основных веществ: монооксида азота (N0), эндотелиального гиперполяризующего фактора (ED ОТ) и простациклина [22]. Ацетилхолин, АТФ, гипоксия, механическое воздейсвие вызывают стимулированную секрецию N0, опосредованную системой вторичных мессенджеров. N0 является мощным вазодилятатором и тормозит процессы ремоделирования стенок сосудов, подавляет пролиферацию гладкомышечных клеток, адгезию и агрегацию тромбоцитов [2, 4, 24, 28, 31]. Одним из важных механизмов, определяющих эндотелиальную дисфункцию, является недостаточная продукция N0. N0 обладает антиоксидантным действием и участвует во многих процессах в нервной и иммунной системах [21].
Эндотелиальная дисфункция является универсальным механизмом патогенеза и прогрессирования артериальной гипертензии, атеросклероза, цереброваскулярных заболеваний, и эти заболевания усугубляют эндотелиальное повреждение [5, 14]. Так, дефицит N0 ускоряет развитие и прогрессирование атеросклероза [29, 30, 32].
Изучение роли эндотелия в патогенезе сердечно-сосудистых заболеваний привело к формированию концепции об эндотелии как о мишени для профилактики и лечения процессов, формирующих сердечно-сосудистую патологию. Дисфункция эндотелия является ранней фазой повреждения сосудистой стенки, что в дальнейшем ведет к развитию атеросклероза, артериальной гипертензии [4]. Эндотелиальная дисфункция — это дисбаланс физиологических механизмов и биологических веществ, обеспечивающих гомеостаз и регулирующих тонус сосудов. Поэтому коррекция дисфункции эндотелия — важное направление терапии сердечно-сосудистых заболеваний [11].
Фармакологические методы коррекции эндотелиальной дисфункции у больных хронической ишемией мозга предусматривают устранение агрессивных для эндотелия факторов (гиперлипидемия, снижение АД, гипергликемия и др.) и нормализацию синтеза эндотелиального N0 [24, 33].
В середине 70-х годов в Латвийском Институте органического синтеза профессором И.Я. Калвиньшем с сотрудниками был разработан лекарственный препарат с международным названием мельдоний. Это лекарственное средство широко используется в медицинской практике с 1984 года под названием Милдронат, а с недавнего времени и под названием Вазонат [12]. Механизм действия мельдония обусловлен ингибированием гамма-бутиробетаин-гидроксилазы, которая превращает у-бутиробетаин (ГББ) в карнитин. В результате этого постепенно (в течение 10 дней) происходит снижение концентрации карнитина и накопление ГББ, что приводит к снижению (3-окисления жирных кислот и оптимизации энергопроизводства в зонах ишемии за счет активации аэробного синтеза энергии. ГББ активирует процессы биосинтеза N0 (рис. 1) [12, 26].
Эфиры ГББ, взаимодействуя с рецепторами эндотелия кровеносных сосудов, вызывают индукцию биосинтеза N0-радикалов. Структура этилового эфира у-бутиробетаина в определенной степени напоминает структуру ацетилхолина. Эфиры ГББ связываются с ацетилхолиновыми рецепторами и являются мощными агонистами М-ацетилхолиновых рецепторов [26]. Молекулярная структура ГББ позволяет связываться с активным центром ацетилхолинэстеразы, что увеличивает содержание ацетилхолина и активирует холинергическую систему [19].
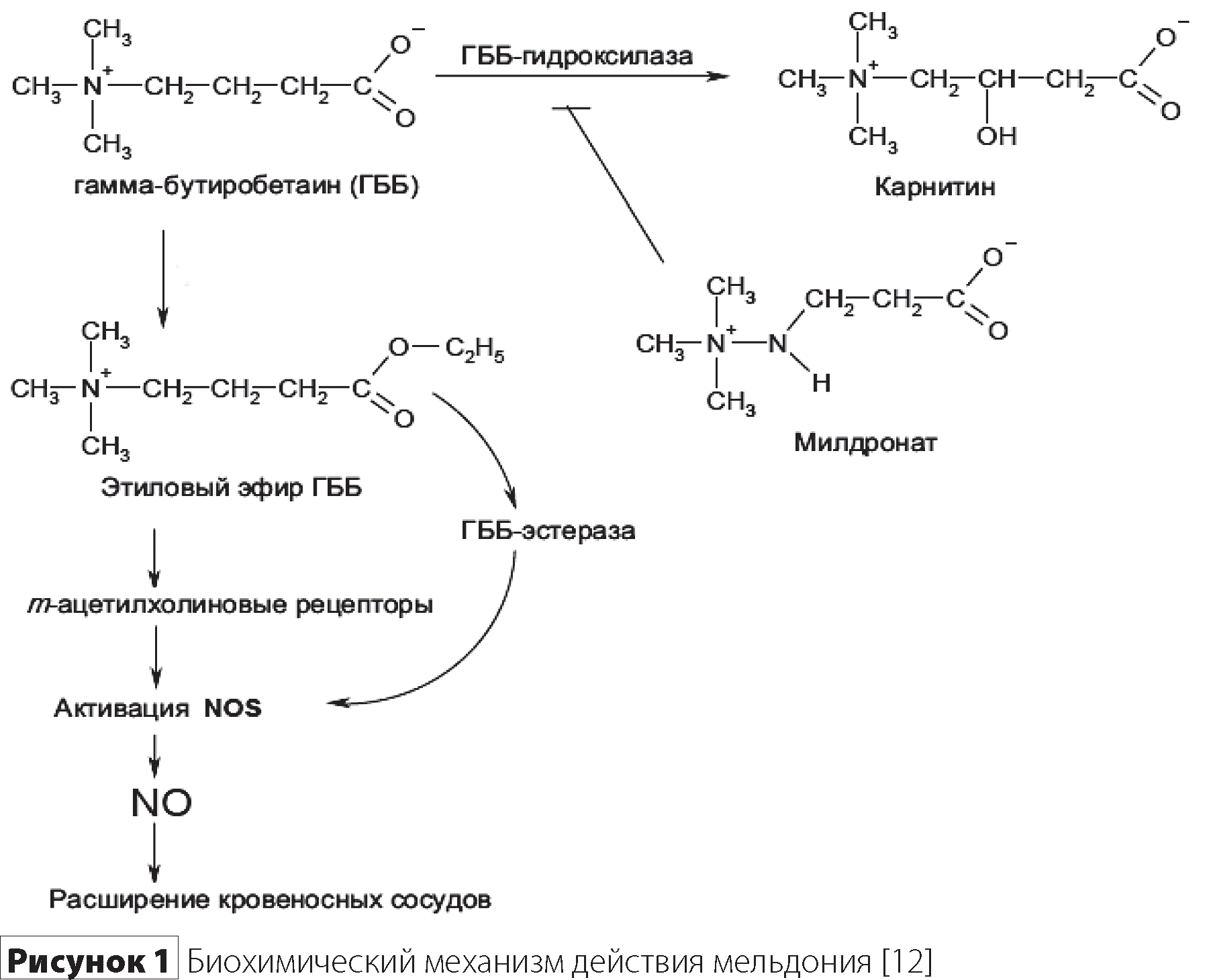
В 2000-х годах создана инновационная комбинация мельдония и ГББ с целью быстрого комплексного воздействия на различные звенья патогенеза ишемических состояний. В 2013 году препарат с торговым названием Капикор (содержит мельдония дигидрат — 180 мг, гамма-бутиробетаина дигидрат — 60 мг) зарегистрирован в Украине [19]. Механизм действия Капикора обусловлен быстрым накоплением высоких концентраций эфиров ГББ, т.к. мельдоний блокирует гидроксилирование ГББ. Эфиры ГББ связываются с М-ацетилхолиновыми рецепторами, происходит активация эндотелиального синтеза оксида азота и биосинтез оксида азота. Окись азота вызывает вазорелаксацию и другие NO-зависимые механизмы. Таким образом, комбинация мельдония и у-бутиробетаина способствует в большей степени физиологическому образованию эфиров ГББ и более активному синтезу оксида азота, что обеспечивает более мощное кардио- и церебропротекторное влияние Капикора по сравнению с действием только мельдония [7, 9, 19, 26]. Итак, биохимический механизм действия Капикора:
- угнетение гидроксилирования у-бутиробетаина в карнитин (уменьшается количество фермента у-бутиробетаин- гидроксилазы);
- увеличивает образование эфиров у-бутиро- бетаина (действие на М-холинорецепторы, эстераза ГББ гидролизует связанные с рецепторами эфиры подобно антихолинэстеразе);
- эфиры у-бутиробетаина — мощные NO-зависимые вазорелаксанты;
- усиливает вазорелаксантный эффект у-бутиробетаина;
- увеличивает синтез N0. Цель работы — сравнительный анализ влияния Капикора и Милдроната на функциональное состояние центральной нервной и сердечно-сосудистой систем у лиц с атеросклеротической дисциркуляторной энцефалопатией I-II ст.
Материал и методы исследования
Проведено комплексное клинико-инструментальное обследование 45 пациентов пожилого возраста (средний возраст 64,3±3,8 года) с дисциркуляторной атеросклеротической энцефалопатией I-II ст. (ДЭ). 1-я группа (25 пациентов) получала препарат Капикор по 2 капсулы 2 раза в день (30 дней); 2-я группа (20 пациентов) получала препарат Милдронат 500 мг по 1 капсуле 2 раза в день (30 дней).
Для анализа влияния Капикора и Милдроната на функциональное состояние мозга, кардиальную гемодинамику и эндотелиальную функцию у больных ДЭ I-II ст. проводилось комплексное обследование, включающее:
- клинико-неврологический осмотр;
- нейропсихологическое тестирование (тест Лурия, тест Мюнстерберга, шкала тревоги Спилберга-Ханина);
- анализ биоэлектрической активности мозга методом компьютерной ЭЭГ на 16-канальном электроэнцефалографе Neurofax EEG-1100K; NIHON KOHDEN, Япония;
- исследование мозгового кровотока методом ультразвукового дуплексного сканирования экстра- и интракраниальных отделов магистральных артерий головы и шеи на приборе Philips EnVisor (PHILIPS);
- определение состояния центральной и кардиальной гемодинамики (холтеровское мониторирование ЭКГ на аппарате «Кардиотехника-04» (ЗАО «Инкарт»), эхокардиография на приборе Toshiba Aplio 300);
- изучение функции эндотелия методом лазерной допплеровской флоуметрии (BLF-21D, Transonic Systems Inc., США) по методике, разработанной в отделе клинической физиологии и патологии внутренних органов института геронтологии НАМН Украины [15];
- состояние микроциркуляции бульбарной конъюнктивы с использованием телевизионной щелевой лампы фирмы Zeiss (Германия) с регистрацией изображения с помощью прикладных компьютерных программ;
- статистическая обработка данных с помощью пакета прикладных программ Statistica 6,0 StatSoft USA.
Результаты и их обсуждение
Одним из проявлений хронической ишемии мозга являются эмоционально-мнестические изменения [1, 23]. При ДЭ Ш ст. отмечаются функционально-метаболические нарушения, где ведущую роль играет снижение уровня макроэргов — АТФ и креатинфосфата и снижение функциональной активности холинергической системы [25]. Учитывая энергокоррегирующее и холинергическое действие Капикора, проведен анализ влияния препарата на нейропсихологическое состояние у больных ДЭ Ш ст. Установлено, что под влиянием Капикора и Милдроната отмечается улучшение кратковременной и долговременной памяти, снижение уровня реактивной и личностной тревожности (рис. 2, табл. 2).
У больных ДЭ Ш ст. курсовой прием Капикора и Милдроната вызывает некоторое снижение реактивной и личностной тревоги (табл. 2) и более активное под влиянием Капикора.
Важным показателем интенсивности формирования мнестических процессов является уровень внимания. Курсовой прием Капикора и Милдроната у больных ДЭ Ш ст. активизирует внимание. У 50% больных ДЭ Ш ст. под влиянием Милдроната и у 40% под влиянием Капикора нормализуются показатели внимания (табл. 3).
Краткосрочная память

КАПИКОР МИЛДРОНАТ
■ до лечения ■ после лечения
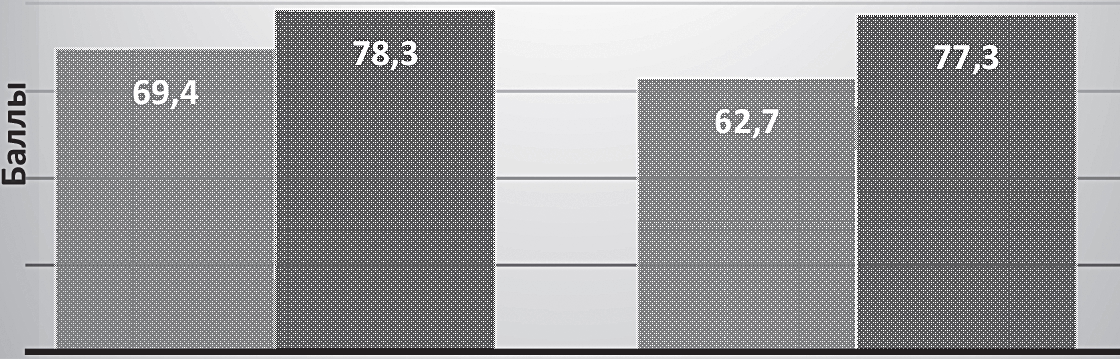
Долговременная память
Капикор Милдронат
■ до лечения ■ после лечения
Рисунок 2 Динамика показателей теста Лурия у больных дисциркуляторной энцефалопатией І-ІІ ст. под влиянием терапии Капикором и Милдронатом
Таблица 2 Динамика показателей шкалы тревоги Спилберга-Ханина у больных дисциркуляторной энцефалопатией І-ІІ ст. под влиянием терапии Капикором и Милдронатом
|
Тип и выраженность тревожности |
Капикор |
Милдронат |
|||
|
До лечения |
После лечения |
До лечения |
После лечения |
||
|
Реактивная тревож ность |
низкая |
24% |
32% |
20% |
25% |
|
умеренная |
28% |
44% |
35% |
40% |
|
|
высокая |
48% |
24% |
45% |
35% |
|
|
Личностная тревож ность |
низкая |
12% |
28% |
5% |
20% |
|
умеренная |
40% |
48% |
35% |
45% |
|
|
высокая |
56% |
32% |
60% |
35% |
|
Таблица 3 Динамика показателей внимания (тест Мюнстерберга) у больных дисциркуляторной энцефалопатией І-ІІ ст. под влиянием терапии Капикором и Милдронатом
|
Характеристика |
Капикор |
Милдронат |
|||
|
До |
После |
До |
После |
||
|
уровня внимания |
|||||
|
лечения |
лечения |
лечения |
лечения |
||
|
Снижено выраженно |
48% |
28% |
25% |
5% |
|
|
Умеренно снижено |
40% |
20% |
55% |
25% |
|
|
Норма |
12% |
52% |
20% |
70% |
|
Проведен анализ влияния Капикора и Милдроната на различные уровни регуляции и функционирования церебральной и кардиальной гемодинамики у больных дисциркуляторной энцефалопатией І-ІІ ст. Влияние Капикора на мозговое кровообращение оценивалось по данным морфо-функционального состояния церебральных сосудов и скоростным показателям. Анализ размеров комплекса «интима- медиа» (КИМ) общей сонной артерии свидетельствует о том, что размеры КИМ у больных ДЭ І-ІІ ст. составляют в среднем 0,94±0,05 мм, что соответствует нормальным показателям.
У 31% больных диагностированы атеросклеротические бляшки различных типов (рис. 3) и преимущественно стенозы до 50%, не влияющие на кровоток, и только у 1 (2,2%) больного — стеноз 60%.
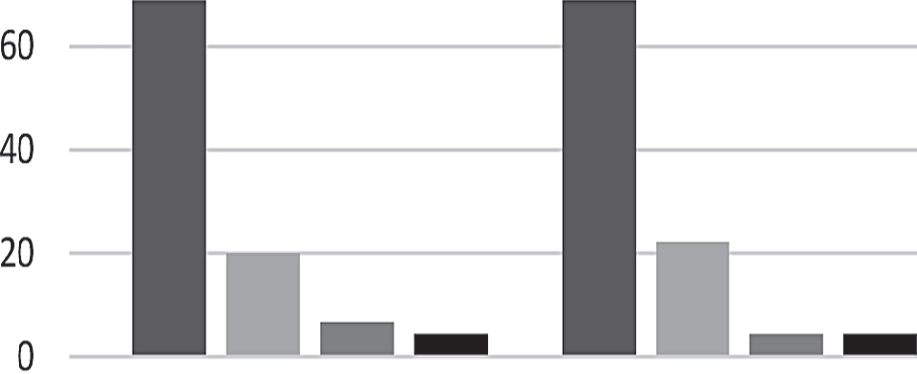
правая ОСА левая ОСА
■ нет бляшек П гетерогенные ■ гипоэхогенные ■ гиперэхогенные
Рисунок 3 Частота и характеристика атеросклеротических бляшек у больных ДЭ І-ІІ ст.
Характеристика размеров КИМ, частота атеросклеротических бляшек и стенозов ОСА свидетельствуют о начальных атеросклеротических поражениях сосудов головного мозга у обследованных больных.
Следует отметить, что под влиянием Капикора и Милдроната не отмечено статистически достоверных изменений структурно-морфологических характеристик экстракраниальных каротидных сосудов мозга (КИМ, частота атеросклеротических бляшек, размеры стенозов) у больных ДЭ І-ІІ ст. Сравнительный анализ курсового влияния Капикора и Милдроната на мозговое кровообращение у больных дисциркуляторной энцефалопатией І-ІІ ст. свидетельствует о том, что Капикор оказывает более выраженное, чем Милдронат, влияние на скоростные показатели кровотока и периферическое сопротивление в сосудах каротидного и вертебро-базилярного бассейнов. Так, под влиянием Капикора статистически достоверно увеличивается линейная систолическая скорость кровотока (ЛССК) в двух ВСА, в правой ПМА и СМА (табл. 4), снижается периферическое сопротивление: пульсаторный индекс (Pi) в двух ОСА, СМА, правых вСа и ПМА, в левой ПА и ОА и индекс резистентности (Ri) в левой ОСА и правых ВСА и СМА (табл. 5-6).
У больных ДЭ 1-11 ст. Милдронат увеличивает ЛССК только в левой ВСА и правой ЗМА и статистически достоверно снижается периферическое сопротивление (Ri) в правой ПМА (табл. 4-6).
Таблица 4 Динамика ЛССК у больных ДЭ І-ІІ ст. под влиянием курсового приема Капикора и Милдроната
|
|
|
КАПИКОР |
МИЛДРОНАТ |
||
|
|
|
До |
После |
До |
После |
|
|
|
лечения |
лечения |
лечения |
лечения |
|
ОСА |
Правая |
74,3±4,6 |
71,5±2,6 |
68,3±3,9 |
66,1±3,8 |
|
Левая |
75,4±3,7 |
78,2±3,3 |
80,3±5,6 |
76,3±6,1 |
|
|
ВСА |
Правая |
67,2±2,6 |
78,7±2,1* |
67,5±3,8 |
70,6±3,3 |
|
Левая |
69,5±2,4 |
76,9±2,1* |
68,2±3,4 |
75,4±1,9* |
|
|
ПА |
Правая |
37,7±2,7 |
39,3±3,1 |
39,0±2,5 |
38,6±1,7 |
|
Левая |
44,6±1,9 |
45,6±2,1 |
41,4±2,9 |
38,9±2,9 |
|
|
ПМА |
Правая |
78,9±3,9 |
89,5±3,3* |
84,9±4,8 |
84,4±6,2 |
|
Левая |
85,8±4,1 |
83,0±3,5 |
76,2±5,3 |
78,1±8,3 |
|
|
СМА |
Правая |
87,4±2,6 |
96,7±3,0* |
89,6±6,6 |
88,3±7,0 |
|
Левая |
89,7±3,3 |
94,6±3,9 |
87,9±4,7 |
87,6±5,7 |
|
|
ЗМА |
Правая |
55,2±2,1 |
56,8±3,5 |
52,4±3,2 |
65,3±4,0* |
|
Левая |
57,1±3,3 |
56,7±2,5 |
55,8±3,4 |
57,0±3,2 |
|
|
ОА |
55,7±2,8 |
54,6±3,9 |
50,6±3,8 |
50,8±4,3 |
|
Таблица 5 Динамика пульсаторного индекса (Рі) у больных ДЭ І-ІІ ст. под влиянием курсового приема Капикора и Милдроната
|
|
|
КАПИКОР |
МИЛДРОНАТ |
||
|
|
|
До |
После |
До |
После |
|
|
|
лечения |
лечения |
лечения |
лечения |
|
ОСА |
Правая |
1,71±0,1 |
1,46±0,08* |
1,48±0,1 |
1,46±0,1 |
|
Левая |
1,51±0,07 |
1,35±0,07* |
1,42±0,08 |
1,35±0,08 |
|
|
ВСА |
Правая |
1,04±0,05 |
0,93±0,04* |
0,84±0,03 |
0,88±0,06 |
|
Левая |
0,97±0,05 |
0,88±0,04 |
0,87±0,04 |
0,85±0,04 |
|
|
ПА |
Правая |
1,18±0,09 |
1,05±0,07 |
1,24±0,1 |
1,11±0,08 |
|
Левая |
1,14±0,07 |
0,99±0,05* |
0,96±0,06 |
1,03±0,05 |
|
|
ПМА |
Правая |
0,95±0,09 |
0,79±0,07* |
0,87±0,07 |
0,72±0,06* |
|
Левая |
0,92±0,12 |
0,86±0,04 |
0,77±0,1 |
0,74±0,05 |
|
|
СМА |
Правая |
0,88±0,03 |
0,74±0,03* |
0,79±0,07 |
0,74±0,04 |
|
Левая |
0,86±0,05 |
0,74±0,03* |
0,72±0,03 |
0,74±0,05 |
|
|
ЗМА |
Правая |
0,80±0,05 |
0,77±0,05 |
0,77±0,03 |
0,78±0,04 |
|
Левая |
0,83±0,05 |
0,78±0,03 |
0,72±0,03 |
0,72±0,04 |
|
|
ОА |
0,84±0,05 |
0,75±0,05* |
0,73±0,03 |
0,76±0,03 |
|
Таблица 6 Динамика индекса резистентности (Ri) у больных ДЭ І-ІІ ст. под влиянием курсового приема Капикора и Милдроната
|
|
|
КАПИКОР |
МИЛДРОНАТ |
||
|
|
|
До |
После |
До |
После |
|
|
|
лечения |
лечения |
лечения |
лечения |
|
ОСА |
Правая |
0,73±0,02 |
0,70±0,02 |
0,71±0,02 |
0,72±0,02 |
|
Левая |
0,72±0,01 |
0,67±0,01* |
0,66±0,02 |
0,65±0,03 |
|
|
ВСА |
Правая |
0,61±0,02 |
0,57±0,01* |
0,55±0,01 |
0,56±0,03 |
|
Левая |
0,58±0,02 |
0,56±0,02 |
0,55±0,02 |
0,55±0,02 |
|
|
ПА |
Правая |
0,66±0,02 |
0,62±0,02 |
0,65±0,03 |
0,63±0,02 |
|
Левая |
0,63±0,02 |
0,61±0,02 |
0,59±0,03 |
0,62±0,02 |
|
|
ПМА |
Правая |
0,59±0,02 |
0,56±0,04 |
0,56±0,01 |
0,52±0,02* |
|
Левая |
0,58±0,04 |
0,56±0,04 |
0,54±0,05 |
0,52±0,02 |
|
|
СМА |
Правая |
0,56±0,01 |
0,51±0,01* |
0,52±0,02 |
0,51±0,02 |
|
Левая |
0,55±0,02 |
0,52±0,02 |
0,52±0,02 |
0,52±0,02 |
|
|
ЗМА |
Правая |
0,54±0,03 |
0,52±0,02 |
0,53±0,02 |
0,51±0,02 |
|
Левая |
0,55±0,02 |
0,55±0,02 |
0,51±0,01 |
0,50±0,02 |
|
|
ОА |
0,55±0,02 |
0,52±0,02 |
0,51±0,02 |
0,51±0,02 |
|
Примечание к табл. 4-6. * — Статистически достоверные различия между показателями до и после лечения препаратами Капикор и Милдронат.
Формирование атеросклеротического процесса ассоциируется с эндотелиальной дисфункцией. Эндотелиальная дисфункция препятствует адекватной регуляции мозгового кровообращения. Нарушение ауторегуляции церебральной перфузии является предиктором развития дисциркуляторной атеросклеротической энцефалопатии [16].
Анализ функционального состояния эндотелия по данным объемной скорости кожного кровотока в покое и при проведении пробы с постокклюзионной гиперемией (рис. 4) показал, что у больных ДЭ І-ІІ ст. снижена объемная скорость кожного кровотока (ОСКК) как в исходном состоянии (в покое), так и на пике реактивной гиперемии по сравнению с контрольной группой пожилого возраста.
Так, в группе больных ДЭ І-ІІ ст. показатель объемной скорости кожного кровотока в исходном состоянии составляет 1,о±о,1 мл/ (мин.100 г), у здоровых лиц того же возраста (КГ) — 1,31±о,04 мл/(мин-юо г) (р<о,05). После окклюзии максимальные цифры ОССК составляли: у больных ДЭ І-ІІ ст. — 5,6±о,4 мл/ (мин.100 г), в КГ — 6,10±о,24 мл/(мин.100 г) (р<о,05). Показатели прироста ОСКК составили соответственно 4,20±о,20 и 4,8±о,44 мл/ (мин.100 г). Восстановительный период также достоверно меньше у больных ДЭ І-ІІ ст. по сравнению с КГ, что указывает на уменьшение вазорелаксации, которая может быть обусловлена пониженной секрецией N0.
Итак, представленные данные свидетельствуют о наличии эндотелиальной дисфункции у больных ДЭ І-ІІ ст. по сравнению с практически здоровыми лицами соответствующего возраста.
Было проведено исследование влияния Капикора и Милдроната на функциональное состояние эндотелия у больных ДЭ І-ІІ ст. (табл. 7).
Анализ динамики показателей объемной скорости кожного кровотока при проведении пробы с реактивной гиперемией у больных ДЭ І-ІІ ст. после приема Капикора и Милдроната показал статистически достоверное повышение ОСКК в исходном состоянии, более выраженное при приеме Капикора. Такая же закономерность получена и при сопоставлении показателей времени наступления пика реактивной гиперемии и продолжительности восстановления ОСКК к исходному уровню, что может свидетельствовать о нормализации функционального состояния эндотелия (табл. 7).
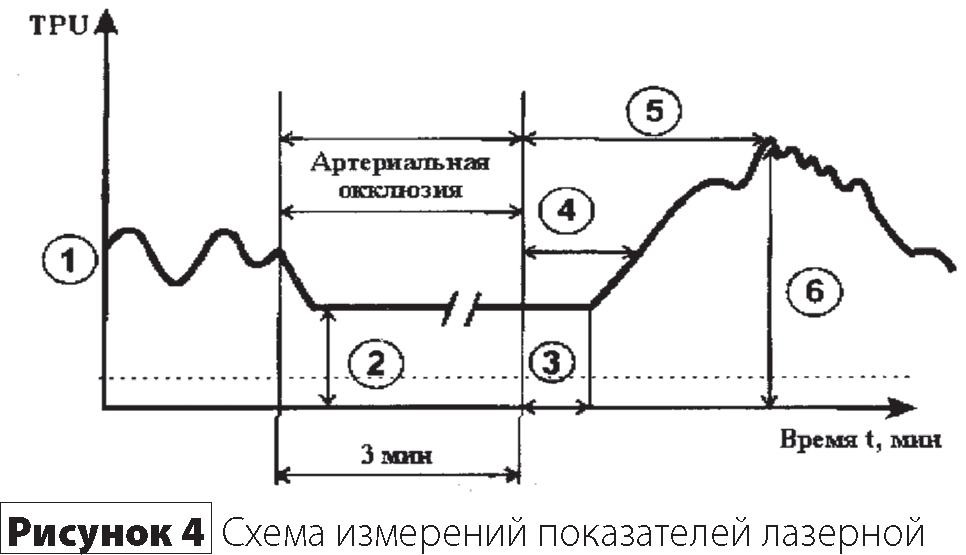
допплеровской флоуметрии при постишемической пробе, где: 1 — объемная скорость кожного кровотока в исходном состоянии; 2 — биологический ноль;
3 — время до начала постишемического ответа; 4 — время восстановления до исходного кровотока; 5 — время максимального постишемического кровотока;6 — максимальный постишемический кровоток.
У больных ДЭ І-ІІ ст. изучалось также влияние препарата на микроциркуляцию бульбарной конъюнктивы. На фоне терапии Капикором у больных ДЭ І-ІІ ст. отмечается улучшение капиллярного кровотока, характеризующееся дилатацией артериол и гомогенизацией капиллярного кровотока. Пример капилляроскопии бульбарной конъюнктивы до и после лечения Капикором пациентки В., 64 года, представлен на рис. 5.
Таким образом, Капикор у больных ДЭ І-ІІ ст. улучшает эндотелиальную функцию (по данным лазерной допплеровской флуоме- трии) и капиллярный кровоток (по данным капилляроскопии бульбарной конъюнктивы).
Тесные взаимосвязи метаболизма и церебральной гемодинамики и влияние Капикора на различные уровни функционирования гемодинамики (от системного до эндотелиального) определило целесообразность проведения анализа действия Капикора на структуру биоэлектрической активности головного мозга [25].
Таблица 7 Показатели объемной скорости кожного кровотока при проведении пробы с реактивной гиперемией у больных ДЭ І-ІІ ст. под влиянием курсового приема Капикора и Милдроната
|
Показатель |
Период исследования |
Милдронат |
Капикор |
|
Исходная ОСКК, мл/(мин-100 г) |
До лечения |
1,0±0,1 |
0,9±0,1 |
|
После лечения |
1,1±0,1 |
1,1±0,1 |
|
|
д |
0,1±0,1 |
0,3±0,1* |
|
|
ОСКК на пике реактивной гиперемии, мл/(мин-100 г) |
До лечения |
5,4±0,5 |
5,0±0,8 |
|
После лечения |
6,1±1,1 |
5,7±0,6 |
|
|
д |
1,8±0,8 |
1,0±0,4 |
|
|
Время наступления пика реактивной гиперемии, с |
До лечения |
11,3±1,8 |
13,5±0,9 |
|
После лечения |
8,6±1,5 |
10,3±1,5 |
|
|
д |
3,8±1,3 |
3,4±1,4 |
|
|
Время восстановления, с |
До лечения |
98,0±9,4 |
101,7±11,7 |
|
После лечения |
130,6±15,8 |
142,5±19,6 |
|
|
д |
30,1±4,8 |
46,2±5,4* |
Примечание. * — Статистически достоверные различия между показателями в группе Капикора и Милдроната.
У больных ДЭ І-ІІ ст. курсовой прием Капикора и Милдроната вызывает реорганизацию биоэлектрической активности головного мозга (табл. 8-10).
Следует отметить, что под влиянием Капикора более выраженные изменения мощности в диапазоне дельта-, альфа 1-, бета 2-ритмов и частоты альфа-ритма отмечаются преимущественно в правом полушарии (табл. 8, 9). Так, снижается мощность дельта-ритма во всех областях правого полушария, а в левом полушарии только в височной области.
В правом полушарии Капикор увеличивает в височной области мощность в диапазоне альфа 2- (до лечения — 0,59±0,04 мкВ, после лечения — 0,68±0,03 мкВ), бета 1-ритмов (о,41±о,о6 мкВ и о,6о±о,05 мкВ соответственно), мощность бета 2-ритма в височной (до лечения — 0,і6±0,02 мкВ, после лечения — о,25±о,о6 мкВ) и затылочной (о,17±о,о1 и 0,24±0,04 мкВ соответственно) областях и повышает частоту альфа-ритма в лобной области (до лечения — 9,47±о,31 Гц, после лечения — 10,58±0,2б Гц).
Влияние Милдроната на биоэлектрическую активность головного мозга менее выражено и характеризуется снижением мощности дельта-ритма в лобной области двух полушарий (справа: до лечения — о,8о±о,о6 мкВ, после лечения — 0,б5±0,07 мкВ; слева: 0,7б±0,02 и о,65±о,о6 мкВ соответственно). Под влиянием Милдроната снижается мощность в диапазоне тета-ритма в центральной области двух полушарий, в правом полушарии в лобной, височной и затылочной областях и в левом полушарии в височной области (табл. 10).
Статистически достоверных изменений мощности в диапазоне других ритмов под влиянием терапии Милдронатом у больных ДЭ І-ІІ ст. не отмечается. Увеличивается частота альфа-ритма в центральных областях двух полушарий (справа: до лечения — 9,б5±0,2 Гц, после лечения — 1о,16±о,18 Гц; слева: 9,74±0,13 Гц и 10,22±о,18 Гц соответственно).
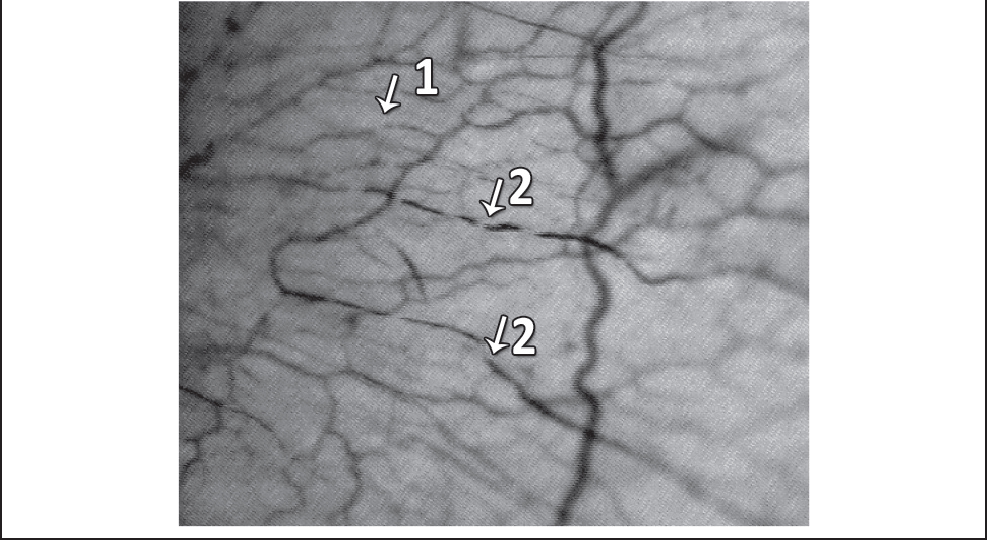
До лечения
Соотношение диаметров артериол и соответствующих венул 1:4. Выражена сетевидная структура сосудов, множественные артериоло-венулярные анастомозы, выражен периваскулярный отек в 1 кв. мм. 10 функционирующих капилляров, (1) кровоток гомогенно-зернистый, в венулах (2) и артериолах определяется сладж-феномен
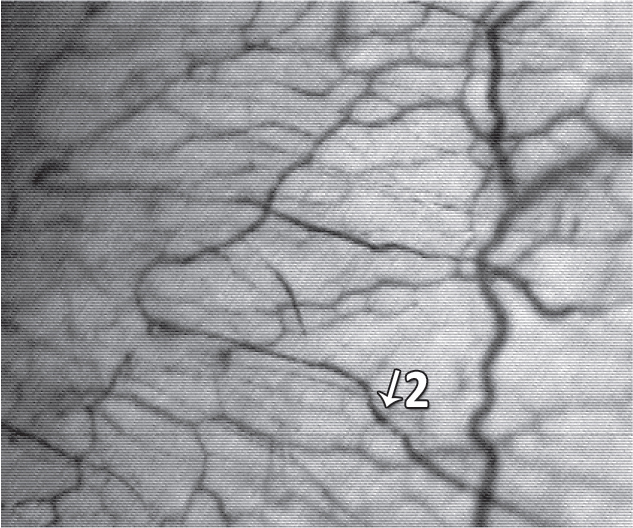
После лечения
Соотношение диаметров артериол и соответствующих венул 1:3. Выражена сетевидная структура сосудов, множественные артериоло-венулярные анастомозы, слегка выражен периваскулярный отек в 1 кв. мм. 10 функционирующих капилляров, кровоток гомогенный, сладж-феномен определяется только в венулах (2)
Таблица 8 Динамика мощности дельта-ритма у больных ДЭ І-ІІ ст под влиянием терапии Капикором, мкВ
|
Области мозга |
До лечения |
После лечения |
||
|
правое |
левое |
правое |
левое |
|
|
Лобная |
0,78±0,09 |
0,62±0,05 |
0,61±0,05* |
0,61±0,03 |
|
0,79±0,09 |
0,59±0,04 |
0,62±0,04* |
0,61±0,04 |
|
|
0,54±0,1 |
0,46±0,04 |
0,43±0,03 |
0,45±0,03 |
|
|
Центральная |
0,76±0,1 |
0,60±0,05 |
0,63±0,04 |
0,58±0,04 |
|
0,74±0,08 |
0,57±0,06 |
0,59±0,04* |
0,53±0,03 |
|
|
Височная |
0,55±0,09 |
0,47±0,05 |
0,45±0,04 |
0,51±0,04 |
|
0,63±0,07 |
0,68±0,07 |
0,48±0,04* |
0,50±0,04* |
|
|
Затылочная |
0,71±0,06 |
0,67±0,05 |
0,59±0,04* |
0,56±0,06 |
Таблица 9 Динамика мощности альфа 1-ритма у больных ДЭ I-II ст. под влиянием терапии Капикором, мкВ
|
Области мозга |
До лечения |
После лечения |
||
|
правое |
левое |
правое |
левое |
|
|
Лобная |
1,12±0,15 |
1,1±0,12 |
1,12±0,15 |
1,14±0,13 |
|
1,21±0,16 |
1,2±0,14 |
1,26±0,18 |
1,29±0,16 |
|
|
0,81±0,12 |
0,82±0,11 |
0,80±0,12 |
0,87±0,08 |
|
|
Центральная |
1,15±0,13 |
1,18±0,17 |
1,48±0,14* |
1,39±0,12 |
|
1,54±0,18 |
1,44±0,16 |
2,14±0,17* |
1,85±0,16* |
|
|
Височная |
0,92±0,17 |
0,93±0,15 |
1,11±0,19 |
1,05±0,18 |
|
1,57±0,15 |
1,24±0,12 |
1,93±0,16* |
1,64±0,15* |
|
|
Затылочная |
1,83±0,12 |
1,67±0,17 |
2,33±0,13* |
2,16±0,19* |
Примечание к табл. 8-д. * — Статистически достоверные различия между показателями до и после лечения препаратом Капикор.
Таким образом, у больных ДЭ І-ІІ ст. под влиянием Капикора изменяется мощность основных ритмов ЭЭГ в правом полушарии в 13 областях, в левом — в 6 областях. У больных ДЭ І-ІІ ст. Милдронат изменяет мощность в 7 и 5 областях соответственно. Направленность изменений мощности основных ритмов ЭЭГ под влиянием Капикора и Милдроната однотипна и характеризуется снижением в диапазоне медленных ритмов (дельта- и тета-) и ростом мощности в диапазоне альфа- и бета-ритмов в отдельных областях на фоне повышения частоты альфа-ритма.
Для оценки влияния Капикора на сердечно-сосудистую систему у больных ДЭ І-ІІ ст. исследовалась динамика показателей вариабельности ритма сердца и структурно-функционального состояния сердца. Значения показателей суточной динамики ЧСС у пациентов с ДЭ І-ІІ ст. находились в пределах допустимой нормы, регламентируемой Европейскими рекомендациями по амбулаторному мониторированию. После лечения Капикором наблюдалось статистически значимое снижение максимальной ЧСС в дневное время (до лечения — 118±4 уд/мин, после лечения — 106±3 уд/мин) и снижение циркадного индекса (ЦИ — отношение средней дневной ЧСС к средней ночной, норма — 122-142) (до лечения — 147±2, после лечения — 122±з). Известно, что ЦИ является фундаментальной, «жесткой константой», отражающей формирование и регуляцию суточного ритма сердца, не зависящей от уровня автоматизма интракардиального источника водителя ритма. Изменения ЦИ характерны для больных с выраженными нарушениями центрального и вегетативного звена регуляции ритма сердца. Повышение ЦИ отмечается при заболеваниях, в патогенезе которых задействовано прогрессирующее поражение интракардиального нервного аппарата сердца, повышение вагосимпатической регуляции. Клинически это ассоциировано с высоким риском развития жизнеугрожающих аритмий.
У больных ДЭ І-ІІ ст. оценивали такой показатель холтеровского мониторирования, как время удлинения QTс, причем принята во внимание его суточная динамика, а также средние, максимальные и минимальные значения. Нормальными значениями длительности интервала QT принято считать 320-440 мс. С интервалом QT связывают такие нарушения, как развитие электрической нестабильности миокарда, аритмий, идиопатической фибрилляции предсердий и внезапной сердечной смерти. Так, Капикор у больных ДЭ 1-11 ст. вызывает снижение длительности среднего QTc (до лечения — 455±1б мс, после лечения — 373±19 мс), среднего QTc днем и ночью (до лечения — 4бо±7 мс, после лечения — 390±11 мс и до лечения — 4б2±13 мс, после лечения — 39б±8 мс соответственно).
Для больных с атеросклеротической ДЭ І-ІІ ст. характерно снижение физиологической вегетативной регуляции, повышение уровня функциональной активности симпато-адреналовой системы, что повышает риск прогрессирования сердечно-сосудистой патологии [27].
Гипоксия мозга приводит к изменениям автономной регуляции сердечно-сосудистой системы, нарушению вариабельности ритма сердца, повышению уровня катехоламинов плазмы и увеличению инцидентности кардиальных аритмий. Исследование вариабельности ритма сердца позволяет определить состояние вегетативной нервной системы, риск развития кардиальной патологии и дать объективную характеристику адаптивному потенциалу больных [27].
Установлена связь между предрасположенностью к летальным аритмиям и наличием признаков повышенной симпатической или пониженной вагусной активности, что стимулирует поиск дальнейших исследований количественных показателей обеспечения вегетативной регуляции. Вариабельность сердечного ритма (ВРС) — один из наиболее многообещающих показателей такого рода — заключается в колебаниях интервала между последовательными ударами сердца, а также колебаниях между последовательными частотами сердечных сокращений. Обнаружена взаимосвязь нарушений ВРС с поражением корковых и подкорковых структур мозга, гипоталамуса, других центров вегетативной регуляции [27].
Для оценки влияния Капикора на вегетативный статус был проведен анализ вариабельности ритма сердца до и после применения данного препарата. Рассчитывали временные и спектральные показатели ВРС. У больных ДЭ І-ІІ ст. до лечения Капикором отмечено снижение спектральных показателей, в частности, низких частот 53Ш12 (нормальное значение — 1170±41б) и высоких частот 249±86 (норма — 975±203), что может свидетельствовать о недостаточной суммарной ВРС. Данное снижение общей ВРС может быть связано со снижением всех вегетативных влияний на сердце. Необходимо отметить, что при этом показатель НЧ/ВЧ до лечения Капикором был выше нормальных значений (2,2±0,18 при норме 1,5-2,0), что характерно для смещения симпато-парасимпатического баланса в сторону превалирования симпатического отдела центральной нервной системы и активизации подкоркового симпатического центра. После лечения Капикором у больных ДЭ І-ІІ ст. показатель НЧ/ВЧ нормализовался (1,78±о,16), что свидетельствует о гармонизации симпатико- парасимпатического баланса.
У больных ДЭ І-ІІ ст. под влиянием Капикора изменяется временная структура ритма сердца: увеличивается триангулярный индекс, характеризующий общую мощность спектра и являющийся маркером парасимпатической активности ВНС (до лечения — 112±13, после лечения — 159±19).
Таким образом, изменения структуры ритма сердца при спектральном и временном анализе ВРС под влиянием Капикора свидетельствуют о гармонизации симпатико-пара- симпатического баланса вегетативной нервной системы у больных ДЭ, что обусловлено холиномиметическим эффектом данного препарата.
У больных ДЭ І-ІІ ст. на фоне лечения Капикором не изменялись и находились в пре- делах нормальных значении показатели интракардиальной (КДО, КСО, УО) и центральной (ОПСС, СИ, МОК и ФВ) гемодинамики (табл. 11).
Таблица 11 Параметры интракардиальной и системной гемодинамики у пациентов ДЭ 1-11 ст. на фоне лечения Капикором
|
Показатель |
До лечения |
После лечения |
|
КСО, мл |
44,0±2,39 |
43,78±2,56 |
|
КДО, мл |
118,2±7,44 |
118,4±7,86 |
|
УО, мл |
74,4±5,41 |
74,9±5,72 |
|
ОПСС, кПа^с^л'1 |
750,8±61,25 |
781,3±65,42 |
|
СИ, л/мин»м2 |
2,72±1,3 |
2,83±1,6 |
|
МОК, л/мин |
5,77±3,3 |
5,56±3,2 |
|
ФВ,% |
62,3±1,2 |
62,6±1,1 |
В определении механизмов влияния Капикора на функциональное состояние мозга и сердца у больных ДЭ І-ІІ ст. важным является и анализ структуры кардио-церебральных взаимосвязей. Проведен корреляционный анализ взаимосвязи ЛССК в экстра- и интракраниальных сосудах каротидного и верте- бро-базилярного бассейнов с показателями системной и кардиальной гемодинамики. На рис. 6 представлены эти статистически достоверные корреляционные связи.
Для больных ДЭ І-ІІ ст. статистически достоверные корреляционные связи характерны только для ЛССК в экстракраниальных сосудах каротидного бассейна (ОСА, ВСА) с показателями кардиальной и системной гемодинамики. У больных ДЭ 1-11 ст. констатируются корреляционные связи между ЛССК в правой ОСА с 9 показателями, ЛССК в левой ОСА с 3 показателями и ЛССК в правой ВСА с 2 показателями системной и интракардиальной гемодинамики. Под влиянием Капикора уменьшается количество корреляционных связей между ЛССК в правой и левой ОСА и в правой ВСА до 4 связей и формируется 1 статистически достоверная корреляционная связь между ЛССК в правой ПА и Е/Е. У больных ДЭ І-ІІ ст. Милдронат также уменьшает количество корреляционных связей между показателями кардиальной и системной гемодинамики и ЛССК в каротидных сосудах до 10, но формируются корреляционные связи с ЛССК в интракраниальных сосудах (правой и левой СМА).
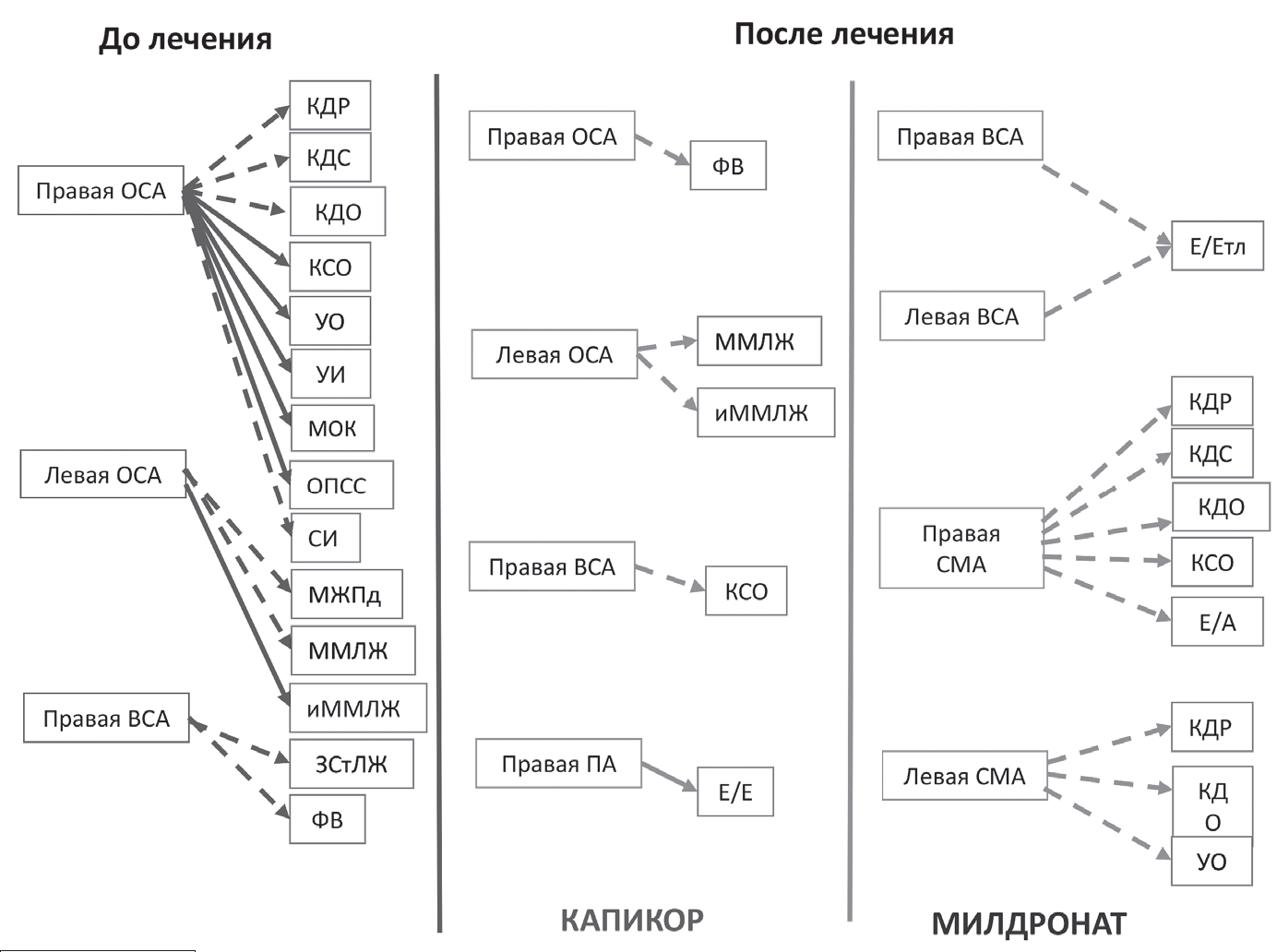
Рисунок 6 Эндотелиальная дисфункция - фармакологическая мишень дисциркуляторной энцефалопатии
Итак, у больных ДЭ І-ІІ ст. отмечается сужение диапазона автономности ауторегуляции мозга, так как эндотелиальная дисфункция препятствует регуляции мозгового кровотока. Под влиянием Капикора повышается функциональная активность процессов ауторегуляции мозгового кровообращения.
Таким образом, у больных ДЭ І-ІІ ст. под влиянием Капикора улучшается долговременная память, внимание, церебральная гемодинамика за счет увеличения ЛССК преимущественно в экстракраниальных сосудах каротидного бассейна и уменьшения индексов периферического сопротивления в отдельных сосудах головного мозга, а также вследствие улучшения капиллярного кровообращения. Капикор повышает функциональную активность эндотелия, вызывает реорганизацию структуры биоэлектрической активности головного мозга, уменьшая мощность медленных ритмов на фоне увеличения частоты и мощности в диапазоне альфа-ритма. Капикор нормализует вегетативную регуляцию сердца за счет активизации парасимпатического звена вегетативной нервной системы и повышает уровень ауторегуляции мозгового кровообращения.
Список использованной литературы
- Бачинська Н.Ю., Полєтаєва К.М., Демченко О.В. та ін. Діагностика легких та помірних когнітивних порушень: Методичні рекомендації. — 2012. — 49 с.
- Бувальцев В.И. Вазодилатирующая функция эндотелия и возможные пути ее коррекции у больных артериальной гипертонией // Дис.. д-ра мед. наук: 14.00.06. М., 2003. — 222 с.
- Бувальцев В.И. Дисфункция эндотелия как новая концепция профилактики и лечения сердечно-сосудистых заболеваний // Международный медицинский журнал. — 2001. — № 3. — С. 202-208.
- Визир В.А., Березин А.Е. Роль эндотелиальной дисфункции в формировании и прогрессировании артериальной гипертензии. Прогностическое значение и перспективы лечения // Український медичний часопис. — 2000. — № 4 (і8). — С. 23-33.
- Головченко Ю.И., Трещинская М.А. Обзор современных представлений об эндотелиальной дисфункции // Consilium medicum Шгата. — 2008. — № 11. — С. 38-40.
- Ельский В.Н., Ватутин Н.Т., Калинкина Н.В., Салахова А.М. Роль дисфункции эндотелия в генезе сердечно-сосудистых заболеваний // Журнал АМН Украины. — 2008. — 14 (1). — С. 51-62.
- Зупанец И.А., Шебеко С.К., Отришко И.А. Значение элементов политропности в механизме реализации фармакологического потенциала препарата Капи- кор // Therapia. — 2015. — № 5 (98). — С. 2-4.
- Кадыков А.С., Манвелов Л.С., Шахпаронова Н.В. Хронические сосудистые заболевания головного мозга: дисциркуляторная энцефалопатия: руководство для врачей. — 2-е изд. — М.: ГЭОТАР-Медиа, 2013. — 232 с.
- Клиническое значение эндотелиальной дисфункции и возможности фармакологической коррекции // Новости медицины и фармации. — 2015. — № 5 (534). — С. 1-7.
- Кузнецова С.М., Кузнецов В.В., Данич Е.И., Шульженко Д.В., Лукач О.И. Новые возможности в лечении дисциркуляторной энцефалопатии // Українська медична газета. — 2007. — № 11. — С. 5-6.
- Кузнецова С.М., Кузнецов В.В., Егорова М.С., Шульженко Д.В., Чижова В.П. Роль коррекции эндотелиальной дисфункции в терапевтической стратегии дисциркуляторной энцефалопатии // Матеріали науково-практичної конференції з міжнародною участю «Ендотеліальна дисфункція при вік-залежній патології: діагностика, профілактика, лікування» (12-13 листопада, м. Київ). — С. 5-6.
- Логина И.П., Калвиньш И.Я. Милдронат в неврологии. — Рига, 2012. — 53 с.
- Неверовский Д.В., Случевская С.Ф., Парфенов В.А. Дифференциальный диагноз дисциркуляторной энцефалопатии в амбулаторной практике // Журнал неврології ім. Б.М. Маньковского. — 2014. — № 4. — С. 76-80.
- Новикова Н.А. Дисфункция эндотелия — новая мишень медикаментозного воздействия при сердечно-сосудистых заболеваниях // Врач. — 2005. — № 8. — С. 51-53.
- Пат. 46415А Украины, МПК 6 А 61 В 5/00, А 61 В 10/00. Способ определения функционального состояния эндотелия микрососудов у лиц пожилого возраста. — № 2001074868; заявл. 11.07.2001; опубл. 15.05.2002. — Бюл. № 5. — 2002.
- Петрищев Н.Н. Дисфункция эндотелия. Причины, механизмы, фармакологическая коррекция. — СПб: Изд-во СПбГМУ, 2003. — 181 с.
- Сторожаков Г.И., Верещагина Г.С., Малышева Н.В. Эндотелиальная дисфункция при артериальной гипертонии у пациентов пожилого возраста // Клиническая геронтология. — 2003. — № 1. — С. 23-28.
- Супрун Э.В. Влияние рецепторного антагониста интерлейкина-1 на эффекты системы оксида азота при экспериментальном ишемическом инсульте // Архів клінічної та експериментальної медицини. — 2012. — Т. 21, № 1. — С. 11-16.
- Сьяксте Н.И., Дзинтаре М.Я., Калвиньш И.Я. Роль индукции NO в механизме действия цитопротектора Олвазола — оригинального регулятора эндотелиальной функции // Мед. перспективы. — 2012. — Т. XVII (2). — C. 4-13.
- Танашян М.М., Максимова М.Ю., Домашенко М.А. Дисциркуляторная энцефалопатия // Терапевтический справочник. — 2015. — Т. 2. — С. 2-26.
- Федин А.И., Старых Е.П., Парфенов А.С., Миронова О.П., Абдрахманова Е.К., Старых Е.В. Фармакологическая коррекция эндотелиальной дисфункции при атеросклеротической хронической ишемии головного мозга // Журнал неврологии и психиатрии им. С.С. Корсакова. — 2013. — Т. 113, № 10. — С. 45-48.
- Федин А.И., Старых Е.П., Путилина М.В., Старых Е.В., Миронова О.П., Бадалян К.Р. Эндотелиальная дисфункция у больных хронической ишемией мозга и возможности ее фармакологической коррекции // Медицинский научно-практический журнал «Лечащий врач». — 2015. — № 5. — С. 45-52.
- Яхно Н.Н., Захаров В.В., Локшина А.Б. и др. Синдром умеренных когнитивных расстройств при дисциркуля- торной энцефалопатии // Журнал неврологии и психиатрии им. С.С. Корсакова. — 2005. — № 2. — С. 13-17.
- Chhabra N. Endothelial dysfunction — a predictor of atherosclerosis // Internet J. Med. — Update. — 2009. — Vol. 4 (1). — P. 33-41.
- Coffey E., Jeffrey M., Cummings M. Geriatric neuropsychiatry. — Washington, London, England, 2001. — 999 p.
- Dambrova M., Daija D., Liepin’sh E., Kir’ianova O., Kalvin’sh I. Biochemical mechanisms of mildronate action during ischemic stress // Lik. Sprava. — 2004. — Vol. 2. — С. 68-74.
- Heart rate variability, standards of measurement, physiological interpretation and clinical use. Task force of the European Society of Cardiology and the North American Society of pacing and electrophysiology // Eur. Heart J. — 1996. — Vol. 17. — Р. 354-381.
- Esper R.J., Nordaby R.A., Vilarino J.O. et al. Endothelial dysfunction: a comprehensive appraisal // Cardiovascular Diabetology. — 2006. — Vol. 5 (4). — P. 1-18.
- Fegan P.G., Tooke J.E., Gooding K.M., Tullett J.M., MacLeod K.M., Shore A.C. Capillary pressure in subjects with type 2 diabetes and hypertension and the effect of antihypertensive therapy // Hypertension. — 2003. — Vol. 41 (5). — P. 1111-1117.
- Gibbons G.H., Dzau VJ. The emerging concept ofvascular remodeling // N. Engl. J. Med. — 1994. — Vol. 330. —
P. 1431-1438.
- Landmesser U., Hornig B., Drexler H. Endothelial function. A critical determinant in atherosclerosis? // Circulation. — 2004. — Vol. 109 (suppl II). — P. П27-П33.
- Lind L., Granstam S.O., Millgard J. Endothelium- dependent vasodilation in hypertension: a review // Blood Pressure. — 2000. — Vol. 9. — P. 4-15.
- Mudau M., Genis A., Lochner A., Strijdom H. Endothelial dysfunction: the early predictor of atherosclerosis // Cardiovasc. J. Afr. — 2012. — Vol. 23 (4). — P. 222-231.
Надійшла до редакції 18.12.2015 р.

