«МЕЖДУНАРОДНЫЙ НЕВРОЛОГИЧЕСКИЙ ЖУРНАЛ», №5 (75) 2015
Т. С. Мищенко, И. В. Здесенко, В. Н. Мищенко
ГУ «Институт неврологии, психиатрии и наркологии Национальной академии медицинских наук Украины», г. Харьков
Резюме. Изучалась эффективность комбинированного антиишемического цереброваскулярного препарата Капикор в сравнении с препаратом Милдронат в лечении пациентов с дисциркуляторной энцефалопатией IIстадии и сахарным диабетом IIтипа на фоне гипертонической болезни и атеросклеротического поражения сосудов головного мозга. 60 пациентов (33 женщины и 27мужчин; средний возраст 54,2 ± ± 5,6 года) были распределены на две группы — основную и группу сравнения (по 30 больных). Пациенты основной группы получали Капикор (комбинация у-бутиробетаина 60мг и мельдония дигидрата 180мг) в дозе 2 капсулы 2раза в сутки, группы сравнения — Милдронат 500 мг в дозе 1 капсула 2раза в сутки в течение 28 дней. Изучение эффективности препаратов проводили с использованием клинико-неврологических, психодиагностических (шкалы ММБЕ, СЫ-Б), инструментальных (транскраниальная допплерография (ТКД)), биохимических (оценка функции эндотелия по показателям эндотелина-1, эндотелиальной ИО-синтазы) методов исследования. Установлено, что препарат Капикор оказывает выраженное терапевтическое влияние на клинические показатели, когнитивные функции, церебральную гемодинамику, астеническую симптоматику, восстановление функции эндотелия и является более эффективным, чем препарат Милдронат. Побочных эффектов и нежелательных явлений при терапии препаратом Капикор не наблюдалось. Сделан вывод о показаниях к широкому применению препарата Капикор у пациентов с дисциркуляторной энцефалопатией и сахарным диабетом.
Ключевые слова: Капикор, дисциркуляторная энцефалопатия, сахарный диабет, эффективность.
В современном мире цереброваскулярные заболевания (ЦВЗ) являются наиболее распространенными. В популяции населения возрастает количество не только острых, но и хронических нарушений мозгового кровообращения [1, 2].
По данным официальной статистики Министерства здравоохранения Украины и статистических регистров, более 2,5 млн людей страдают различными формами ЦВЗ. При этом наиболее распространенной является дисциркуляторная энцефалопатия (ДЭ), которая составляет более 90 % в структуре всех форм ЦВЗ. С каждым годом в нашей стране наблюдается неуклонный рост заболеваемости ЦВЗ, и именно за счет этой формы нарушения мозгового кровообращения [2]. Наиболее частыми факторами риска ДЭ являются атеросклероз, артериальная гипертензия, артериальная гипотензия, сахарный диабет (СД), болезни сердца и др. [3]. Наличие у пациентов нескольких факторов значительно повышает степень риска развития мозгового инсульта (МИ), деменции и требует более активного медикаментозного вмешательства.
Основными патогенетическими механизмами развития ДЭ являются: стенозирующие поражения магистральных артерий головы, диффузные поражения мелких пенетрирующих артерий, нарушения реологических свойств крови, внутрисосудистая активация гемостатического потенциала, изменения эндотелия, факторы гуморального и клеточного иммунитета [3]. В последние годы пристальное внимание многих исследователей обращено на проблему роли эндотелия в развитии сердечно-сосудистых заболеваний (ССЗ), в том числе ДЭ [4—6].
Воздействие на эндотелиальную дисфункцию — новая стратегия превентивной кардионеврологии. Эндотелий сосудов является органом-мишенью при профилактике и лечении цереброваскулярной патологии [6—10]. Он продуцирует более 30 важнейших медиаторов, участвующих в фибринолизе, регуляции тонуса сосудов, пролиферации и регуляции иммунных реакций. Среди всего изобилия медиаторов, вырабатываемых эндотелием, ключевая роль принадлежит оксиду азота (N0), который является универсальным биологическим регулятором, содержащимся во всех клетках человеческого организма. Оксид азота поддерживает нормальный тонус сосудов, подавляет пролиферацию гладкой мускулатуры сосудов, предотвращая патологическую перестройку сосудистой стенки (ремоделирование), прогрессирование атеросклероза. Кроме того, оксид азота обладает антиоксидантным действием, ингибирует агрегацию тромбоцитов, адгезию нейтрофилов к эндотелию и миграцию моноцитов [11—19].
Признаки эндотелиальной дисфункции наблюдаются при артериальной гипертензии, атеросклерозе, ишемической болезни сердца, инфаркте миокарда, хронических цереброваскулярных заболеваниях, МИ, почечной недостаточности, СД, эректильной дисфункции, гестозах и метаболическом синдроме и др. [5, 6, 20—24].
Таким образом, целостность и физиологическая функция эндотелия сосудов являются основой здоровья сердечно-сосудистой системы. Именно эндотелиальная функция находится под влиянием сосудистых факторов риска. Дисфункция эндотелия сосудов является ранним патофизиологическим признаком и независимым предиктором неблагоприятного прогноза при большинстве ССЗ.
Для коррекции эндотелиальной дисфункции применяется несколько лекарственных препаратов. Одним из первых лекарственных средств этой группы был мельдоний. Действующим началом мельдония является 3-(2,2,2-триметилгидразиний) пропионата дигидрат. Этот препарат был разработан в середине 70-х годов XX века в Латвийском институте органического синтеза Иваром Калвиньшом и другими исследователями. С 1984 года это лекарство широко используется в медицинской практике под названием «Милдронат».
Как известно, механизм действия мельдония включает в себя ингибирование ГББ-гидроксилазы, которая превращает у-бутиробетаин (ГББ) в карнитин. В результате этого постепенно (в течение 10 дней) происходит снижение концентрации карнитина и накопление ГББ, что приводит к оптимизации энергопроизводства в ишемизированных клетках. К сожалению, данный процесс происходит медленно, и лечебный эффект мельдония начинает проявляться лишь после того, как концентрация ГББ во всем организме существенно возрастет, что затрудняет применение мельдония при острых случаях нарушения кровообращения.
При анализе механизма действия мельдония было высказано предположение о том, что этот недостаток препарата можно устранить, создав такую композицию мельдония и ГББ, которая обеспечивала бы
незамедлительное повышение концентрации ГББ до нужного уровня. В экспериментальных исследованиях эта гипотеза подтверждена, так как было установлено, что если к мельдонию добавляется необходимое количество ГББ, то эффект от этой композиции наступает незамедлительно. Таким образом, был создан комбинированный цереброваскулярный антиишемический препарат — Капикор (мельдоний + у-бутиробетаин), который сочетает в себе достоинства предшественника мельдония и широкие возможности N0.
Комбинация у-бутиробетаина 60 мг и мельдония дигидрата 180 мг в препарате Капикор позволяет достичь максимально быстрого и стойкого физиологического антиишемического эффекта путем оптимизации выработки оксида азота и восстановления функции эндотелия. Одновременное введение мельдония и ГББ сопровождается быстрым накоплением эфиров ГББ, так как мельдоний не позволяет гидроксилировать у-бутиробетаин в карнитин. Образующиеся эфиры ГББ связываются со своими специфическими рецепторами и/или с М-ацетилхолиновыми рецепторами. Происходит активация эндотелиальной синтазы окиси азота и его биосинтез. В свою очередь, оксид азота вызывает быструю вазодилатацию и каскад N0-зависимых эффектов, что обусловливает восстановление функции эндотелия. Снижение уровня карнитина приводит к торможению окисления жирных кислот, активации гликолиза, уменьшению потребности в кислороде и оптимизации энергообеспечения.
Эти совокупные механизмы обеспечивают оптимальный уровень гамма-бутиробетаина дигидрата, что обусловливает более выраженные и быстрые N0-зависимые эффекты: сосудорасширяющий, антиагрегантный, антикоагулянтный, антиоксидантный и другие; влияет на регуляцию апоптоза и пролиферации, поддержание сосудистого гомеостаза и т.д.
Такая комбинация обеспечивает мощное и быстрое кардио- и церебропротекторное действие, устраняя зависимость скорости наступления терапевтических эффектов от истощения организма в условиях ишемии и стресса различного генеза (оксидантного в том числе).
При сердечной недостаточности Капикор улучшает сократительную способность миокарда, повышает толерантность к физической нагрузке; при стабильной стенокардии II и III функционального класса — снижает частоту сердечных приступов; обеспечивает умеренный гипотензивный эффект и нормализует ритм сердечных сокращений.
При сосудистых поражениях головного мозга Капикор улучшает церебральную гемодинамику, нормализует метаболизм в нервных клетках, оптимизирует потребление кислорода мозговой тканью, благодаря чему улучшаются когнитивные функции, умственная и физическая деятельность, нормализуется психоэмоциональное состояние, снижается чувство переутомления.
Таблица 1
Распределение больных по полу возрасту и массе тела
|
Показатели |
Группы больных |
|
|
Основная |
Контрольная |
|
|
Количество больных |
30 |
30 |
|
Возраст, годы |
53,8 ± 6,2 |
54,2 ± 5,8 |
|
Мужчины |
14 (53 %) |
13 (43 %) |
|
Женщины |
16 (47 %) |
17 (57 %) |
|
Масса тела, кг |
79,10 ± 12,12 |
78,70 ± 13,11 |
С учетом вышеизложенного представляло интерес изучение клинической эффективности, переносимости, а также влияния препарата Капикор на эндотелиальную функцию у больных с ДЭ II стадии и СД II типа.
Целью данного исследования явилась оценка эффективности и переносимости препарата Капикор (комбинация у-бутиробетаина 60 мг и мельдония дигидрата 180 мг), капсулы, производства АО «Олайнфарм» (Латвия) в сравнении с препаратом Милдронат 500 мг, капсулы, производства фирмы Grindex при лечении пациентов с дисциркуляторной энцефалопатией II стадии и сахарным диабетом II типа на фоне гипертонической болезни и атеросклеротического поражения сосудов головного мозга.
Задачи исследования:
- изучить терапевтическую эффективность препарата Капикор в отношении клинико-неврологических проявлений заболевания;
- оценить эффективность влияния препарата Ка- пикор на когнитивные функции;
- исследовать воздействие препарата Капикор на церебральную гемодинамику;
- изучить влияние препарата Капикор на эндотелиальную дисфункцию;
- изучить переносимость и возможные побочные явления исследуемого препарата;
- сравнить результаты применения препаратов в основной и контрольной группах и оценить превышающую эффективность лекарственного средства Капикор, капсулы, производства АО «Олайнфарм» (Латвия) в сравнении с препаратом Милдронат, капсулы, производства фирмы Grindex при лечении пациентов с ДЭ II стадии и СД II типа.
Для осуществления поставленной цели и задач были применены следующие методы: общеклинические, клинико-неврологические с оценкой общего клинического впечатления по шкале CGI-S, психодиагностические (шкала MMSE), инструментальные (транскраниальная допплерография на ультразвуковом сканере ULTIMA Pro 30 («РАДМИР», Украина) и Sigma Iris 880 CE (Франция)), биохимические (оценка состояния функции эндотелия по показателям эндотелина-1 (ЕТ1), эндотелиальной NO- синтазы), клинико-лабораторные, статистические методы.
Результаты исследования и их анализ
В исследование были включены 60 пациентов обоих полов в возрасте от 52 до 75 лет с ДЭ II стадии и СД II типа, находящихся на стационарном лечении в отделении сосудистой патологии головного мозга ГУ «Институт неврологии, психиатрии и наркологии НАМН Украины».
Преобладали женщины: среди всех обследованных было 33 женщины (55 %) и 27 мужчин (45 %) в возрасте от 25 до 70 лет. Большинство относилось к возрастной группе 56—70 лет. По характеру сосудистого заболевания у 36 больных была диагностирована гипертоническая болезнь, у 14 — атеросклероз, в 10 случаях имело место сочетание гипертонической болезни с атеросклерозом. Все больные страдали СД II типа.
Включенные в исследование пациенты были распределены на две группы по 30 человек — основную и группу сравнения.
Группы больных были однородными по возрасту (средний возраст больных составлял: в основной группе — 53,8 ± 6,2 года, в группе сравнения — 54,2 ± ± 5,8 года), полу, массе тела (табл. 1).
Наиболее значительные и распространенные жалобы: головные боли, которые зачастую были связаны с колебаниями артериального давления («стягивает голову»), чувство тяжести, шум, звон в голове, головокружения, шаткость при ходьбе («земля уходит из-под ног»), снижение памяти, внимания, работоспособности, изменения настроения, повышенная раздражительность, утомляемость («быстрое наступление усталости после небольших нагрузок»). Пациенты жаловались на рассеянность, замедление сообразительности, отмечали, что им «трудно собраться с мыслями». Ухудшение общего самочувствия сопровождалось нарушением сна (трудности засыпания, беспокойный сон с частыми пробуждениями, устрашающими сновидениями, ранним и окончательным пробуждением, отсутствием ощущения отдыха после сна).
При объективном исследовании у всех больных отмечалась диффузная органическая симптоматика в сочетании с очаговыми нарушениями. Превалировали глазодвигательные нарушения: слабость конвергенции, ограничение взора вверх, недостаточность отводящих нервов. У больных выявлялись асимметрия лицевой мускулатуры, нистагм при крайних отведениях, нарушения статики и координации, двигательные (разной степени выраженности), чувствительные, тонусные нарушения, анизорефлексия. Отмечалась группа симптомов: снижение корнеальных рефлексов, отечность языка с отпечатками зубов, болезненость глазных яблок при надавливании, которые расценивались как косвенные признаки ликворной гипертензии.
Кроме того, у больных обнаруживались рефлексы орального автоматизма, патологические знаки.
Анализ субъективной и объективной неврологической симптоматики позволил выделить ведущие клинические синдромы.
Цефалгический синдром встречался в 93,3 % случаев. Он характеризовался выраженностью, монотонностью и однообразием головной боли, иногда только в одной половине головы, но чаще без четкой локализации.
Вестибулоатактический синдром отмечался у 86,7 % больных, характеризовался головокружениями, шаткостью при ходьбе, усиливающейся при взгляде на движущиеся предметы, и изменениями положения тела, сопровождался нарушениями статики и координации, атаксией в пробе Ромберга.
Ликворно-гипертензионный синдром встречался в 50,0—53,3 % случаев. Он характеризовался упорными головными болями распирающего характера, с чувством давления на глазные яблоки, тошнотой и обусловливал развитие и усугубление неврологической симптоматики вторично-стволового характера — глазодвигательные нарушения, пирамидные знаки, патологические рефлексы, псевдобульбарные нарушения. Наличие гипертензионного синдрома подтверждалось данными обследования глазного дна, компьютерной томографии, косвенными признаками, выявленными при проведении электроэнцефалографии, ультразвуковой допплерографии.
Астенический синдром отмечался у 93,3 % больных. Он представлен в основном в виде выраженного компонента физической и психической утомляемости и снижения сенсорной толерантности.
Когнитивные нарушения различной степени выраженности встречались у 90,0—93,3 % больных. Их более подробная характеристика будет дана ниже.
Как видно из представленных данных, группы больных были также однородными по выраженности субъективной и объективной неврологической симптоматики.
Включенные в исследование пациенты были распределены на две группы по 30 пациентов — основную и группу сравнения.
Пациенты основной группы получали исследуемый препарат Капикор, капсулы, производства АО «Олайнфарм» по 2 капсулы 2 раза в сутки. Курс применения лекарственного средства составил 28 дней.
Пациентам группы сравнения по такой же схеме назначалось референтное лекарственное средство Милдронат, капсулы, производства фирмы Grindex по 1 капсуле (500 мг) 2 раза в сутки. Курс применения лекарственного средства составил 28 дней.
Клинико-неврологическая оценка эффективности препарата Капикор
Динамика субъективной неврологической симптоматики и выраженности ведущих неврологических синдромов до и после лечения препаратами Капикор и Милдронат представлена в табл. 2—4.
Как видно из табл. 2—4, синдромальная структура, характер и выраженность субъективной и объективной неврологической симптоматики у больных обеих групп до начала лечения были практически идентичными, количественно сходными.
Пациенты как основной, так и группы сравнения оценивали выраженность исследуемых показателей как «высокую» (3 балла) и «среднюю» (2 балла). На момент включения в исследование никто из больных не давал клиническим симптомам характеристику «слабая выраженность» (1 балл) или «отсутствие признака» (0 баллов).
Таблица 2. Динамика субъективной неврологической симптоматики у исследуемых больных до и после лечения препаратами Капикор и Милдрон
|
Жалобы |
Капикор |
Милдронат |
||||||
|
До лечения |
После лечения |
До лечения |
После лечения |
|||||
|
Абс. |
% |
Абс. |
% |
Абс. |
% |
Абс. |
% |
|
|
Головная боль |
28 |
93,3 |
10 |
33,3* |
27 |
90,0 |
10 |
33,3* |
|
Боль в глазах |
23 |
76,6 |
9 |
30,0* |
25 |
83,3 |
11 |
36,7* |
|
Головокружение |
26 |
86,7 |
12 |
40,0* |
25 |
83,3 |
13 |
43,3 |
|
Шаткость при ходьбе |
26 |
86,7 |
10 |
33,3* |
26 |
86,7 |
12 |
40,0* |
|
Тошнота |
24 |
80,0 |
5 |
16,7* |
16 |
53,3 |
10 |
33,3 |
|
Шум в ушах и в голове |
24 |
80,0 |
6 |
20,0* |
23 |
76,6 |
9 |
30,0* |
|
Онемение конечностей |
13 |
43,3 |
9 |
30,0 |
10 |
33,3 |
7 |
23,3 |
|
Нарушение сна |
20 |
66,6 |
7 |
23,3* |
24 |
80,0 |
10 |
33,3* |
|
Раздражительность, снижение фона настроения |
23 |
76,6 |
5 |
16,7* |
22 |
73,3 |
8 |
26,7* |
|
Нарушение памяти, внимания, мышления |
27 |
90,0 |
8 |
26,7* |
28 |
93,3 |
16 |
53,3 |
|
Астеническая симптоматика |
28 |
93,3 |
6 |
20,0* |
28 |
93,3 |
18 |
60,0 |
Примечание: здесь и в табл. 3-5: * — р < 0,05 между результатами до и после лечени
Таблица 3. Динамика степени выраженности клинических проявлений у исследуемых больных в процессе лечения
|
Жалобы |
Капикор |
Милдронат |
||
|
До лечения |
После лечения |
До лечения |
После лечения |
|
|
Головная боль |
2,92 ± 0,32 |
1,08 ± 0,05* |
2,95 ± 0,31 |
1,10 ± 0,09* |
|
Чувство тяжести в голове |
2,96 ± 0,20 |
0,95 ± 0,08* |
2,94 ± 0,22 |
1,05 ± 0,09* |
|
Головокружение |
2,87 ± 0,34 |
1,25 ± 0,02* |
2,77 ± 0,26 |
1,28 ± 0,08* |
|
Неустойчивость при ходьбе |
2,88 ± 0,33 |
0,98 ± 0,07* |
2,92 ± 0,30 |
1,02 ± 0,09* |
|
Шум в голове и ушах |
2,87 ± 0,34 |
0,85 ± 0,05* |
2,80 ± 0,29 |
1,02 ± 0,06* |
|
Повышенная утомляемость |
2,84 ± 0,37 |
0,72 ± 0,28* |
2,90 ± 0,27 |
1,26 ± 0,10* |
|
Ухудшение памяти |
2,81 ± 0,39 |
0,91 ± 0,09* |
2,78 ± 0,40 |
1,18 ± 0,09* |
|
Ослабление внимания |
2,72 ± 0,45 |
0,72 ± 0,08* |
2,76 ± 0,45 |
1,09 ± 0,09* |
|
Нарушение сна |
2,61 ± 0,49 |
0,62 ± 0,09* |
2,70 ± 0,45 |
1,02 ± 0,09* |
Таблица 4. Динамика выраженности ведущих неврологических синдромов у исследуемых больных до и после лечения препаратами Капикор и Милдронат
|
Синдромы |
Капикор |
Милдронат |
||||||
|
До лечения |
После лечения |
До лечения |
После лечения |
|||||
|
Абс. |
% |
Абс. |
% |
Абс. |
% |
Абс. |
% |
|
|
Цефалгический |
28 |
93,3 |
10 |
33,3* |
27 |
90,0 |
10 |
33,3* |
|
Ликворно-гипертензионный |
16 |
53,3 |
9 |
30,0 |
15 |
50,0 |
10 |
33,3 |
|
Вестибулоатактический |
26 |
86,7 |
10 |
33,3* |
26 |
86,7 |
12 |
40,0* |
|
Пирамидной недостаточности |
13 |
43,3 |
9 |
30,0 |
10 |
33,3 |
7 |
23,3 |
|
Астенический |
28 |
93,3 |
6 |
20,0* |
28 |
93,3 |
18 |
60,0 |
|
Когнитивные нарушения |
27 |
90,0 |
8 |
26,7* |
28 |
93,3 |
16 |
53,3 |
По шкале общего клинического впечатления о тяжести заболевания (CGI-S) у 9 пациентов основной группы и у 10 — контрольной отмечено пограничное расстройство, а в остальных (21 пациент основной группы и 20 — контрольной) наблюдениях — «легкое заболевание».
В ходе исследования под влиянием терапии сравниваемыми препаратами у больных основной и контрольной групп существенно уменьшался объем жалоб, каких-либо значимых различий в количественной динамике практически всех показателей субъективной и объективной неврологической симптоматики выявлено не было. По завершении лечения пациенты обеих групп ставили такую оценку исследуемым признакам: преимущественно «слабая выраженность» (1 балл) или «отсутствие признака» (0 баллов). Высокой степени выраженности симптома по завершении курса лечения не отметил никто из пациентов как основной, так и группы сравнения. В отдельных случаях признаки оценивались пациентами как «средневыраженные».
Однако под влиянием лечения препаратом Капикор отмечена статистически значимая положительная динамика в восстановлении когнитивных функций и уменьшении выраженности астенической симптоматики. Пациенты, принимавшие Капикор, в большей степени констатировали уменьшение утомляемости, улучшение ночного сна, возрастание активности и работоспособности (пациенты отмечали, что «в голове просветлело», «прибавилось сил»). Наряду с редукцией астенических расстройств, восстановлением эмоциональной устойчивости лиц, получавших Капикор, большая положительная динамика у них наблюдалась и в отношении нарушений когнитивного функционирования. Улучшалась концентрация внимания, уменьшалась заторможенность, ускорялся темп психической деятельности, что находило отражение в лучших показателях этих пациентов по шкале ММSЕ.
Влияние препарата Капикор на когнитивные функции
При психодиагностическом исследовании общий показатель по шкале ММSЕ у пациентов основной и контрольной групп не отличался, составляя 25,3 ± ± 2,2 балла из 30 возможных, что соответствовало преддементным когнитивным нарушениям. Имели место: сужение объема вербальной памяти (4,6 ± ± 0,9 балла из 6 в основной и 4,7 ± 0,3 в контрольной группе), нарушения счетных операций (3,8 ± 0,2 балла из 5 возможных в основной и 4,0 ± 0,3 балла в контрольной), перцептивно-гностических функций (7,8 ± 0,3 балла из 9 в основной и 7,3 ± 0,4 балла в контрольной), ориентации (9,1 ± 0,8 балла из 10 возможных в основной и 9,3 ± 0,7 балла в контрольной группе) (табл. 5).
Анализ динамики когнитивных функций в процессе лечения показал, что у пациентов основной группы, принимающих Капикор, отмечалось статистически значимое улучшение всех показателей когнитивной сферы (памяти, внимания, ориентации, счетных функций). У этих больных после лечения общий показатель когнитивной продуктивности увеличился на 3 балла и составил 28,4 ± 1,6 балла, что соответствовало отсутствию когнитивных нарушений. У пациентов группы сравнения динамика показателей когнитивной сферы была меньшей, показатель когнитивной продуктивности по шкале ММ8Е увеличился лишь на 2 балла и составлял 27,2 ± 1,5 балла, что соответствовало преддементным когнитивным нарушениям.
Таким образом, динамика показателей продуктивности когнитивных функций (по шкале ММ8Е) у больных, получавших Капикор, превышала таковую у пациентов, получавших Милдронат.
К моменту завершения лечения (28 дней) общая частота улучшения различной степени выраженности (шкала CGI-I) составляла в основной группе 100 %, в контрольной — 93,3 %. Умеренное улучшение отмечено у 63,3 % пациентов, получавших Капикор, выраженное — у 16,7 %, минимальное — у 10 %. У пациентов, получавших Милдронат, умеренное улучшение наблюдалось также в 63,3 % случаев, выраженное — лишь в 13,3 %, минимальное — в 16,7 %. У 2 пациентов этой группы состояние не изменилось (рис. 1).
Таким образом, в процессе лечения препаратом Капикор отмечена позитивная динамика когнитивных функций у обследованных больных. Получено статистически достоверное уменьшение астенических нарушений, увеличение показателей когнитивной продуктивности. После лечения общий показатель когнитивной продуктивности (по шкале ММ8Е) составил 28,4 ± 1,6 балла, увеличившись более чем на 3 балла, что соответствовало отсутствию когнитивных нарушений. Общая частота улучшения различной степени выраженности (шкала CGI-I) составила у пациентов основной группы 100 %, выраженного
улучшения — 16,7 %.
Влияние препарата Капикор на церебральную гемодинамику
О состоянии церебральной гемодинамики судили по данным ТКД. Регистрировали среднюю линейную скорость кровотока в сифоне внутренней сонной артерии (ВСА), средней мозговой артерии (СМА) и в интракраниальных сегментах позвоночной артерии (ПА). Определяли также индекс пульсации.
По данным ТКД, у всех больных отмечалось снижение линейной систолической скорости кровотока в бассейне СМА до 62,4 ± 2,6 см/с, средней ЛСК по интракраниальным артериям, уменьшение пульсационного индекса, что свидетельствовало об ухудшении эластикотонических свойств церебральных сосудов (табл. 6).
При дуплексном сканировании стенок сонных артерий выявлялось достоверное увеличение комплекса интима-медиа (КИМ) — до 1,4 ± 0,2 мм, отсутствие его дифференциации на слои, большое количество кальцифицированных бляшек.
Таблица 5.
Динамика показателей продуктивности когнитивных функций у исследуемых больных
до и после лечения препаратами Капикор и Милдронат (по шкале ММSЕ), баллы
|
Показатели |
Капикор |
Милдронат |
||
|
До лечения |
После лечения |
До лечения |
После лечения |
|
|
Ориентация (макс.10 баллов) |
9,1 ± 0,8 |
9,7 ± 0,3 |
9,3 ± 0,7 |
9,5 ± 0,4 |
|
Память (макс. 6 баллов) |
4,6 ± 0,9 |
5,3 ± 0,7* |
4,7 ± 0,3 |
5,4 ± 0,6 |
|
Счетные операции (макс. 5 баллов) |
3,8 ± 0,2 |
4,6 ± 0,4* |
4,0 ± 0,8 |
4,4 ± 0,2 |
|
Перцептивно-гностические функции (макс. 9 баллов) |
7,8 ± 0,3 |
8,8 ± 0,2* |
7,3 ± 0,4 |
7,9 ± 0,3 |
|
Общий показатель когнитивной продуктивности (макс. 30 баллов) |
25,3 ± 2,2 |
28,4 ± 1,6* |
25,3 ± 2,2 |
27,2 ± 1,5 |
У пациентов оценивали показатели потокзависи- мой вазодилатации (ПЗВ), по которым судили о состоянии сосудисто-двигательной функции эндотелия. ПЗВ определяли по результатам манжеточной пробы как процентное отношение внутреннего диаметра плечевой артерии до и через 30 с после ее проведе
ния. ПЗВ у пациентов обеих групп была снижена до 4,2 ± 1,3 %.
В процессе лечения пациентов препаратом Капикор показатели церебральной гемодинамики по данным ТКД улучшались — увеличивалась ЛСК в сосудах сонных и позвоночных артерий, нормализовался пульсационный индекс. Линейная систолическая скорость кровотока в бассейне СМА повысилась на 26 % (более чем на 15 % от исходной) и составляла 78,7 ± 3,8 см/с, нормализовался пульсационный индекс, снижались показатели КИМ, увеличивались показатели ПЗВ (до 16,4 ± 1,4 %), что говорило о восстановлении функции эндотелия. В процессе лечения препаратом Милдронат динамика показателей церебральной гемодинамики была незначительной. Полученные результаты свидетельствуют также в пользу превышающей эффективности препарата Капикор по сравнению с референтным препаратом Милдронат при лечении пациентов с ДЭ II стадии и СД II типа на фоне гипертонической болезни и атеросклеротического поражения сосудов головного мозга.
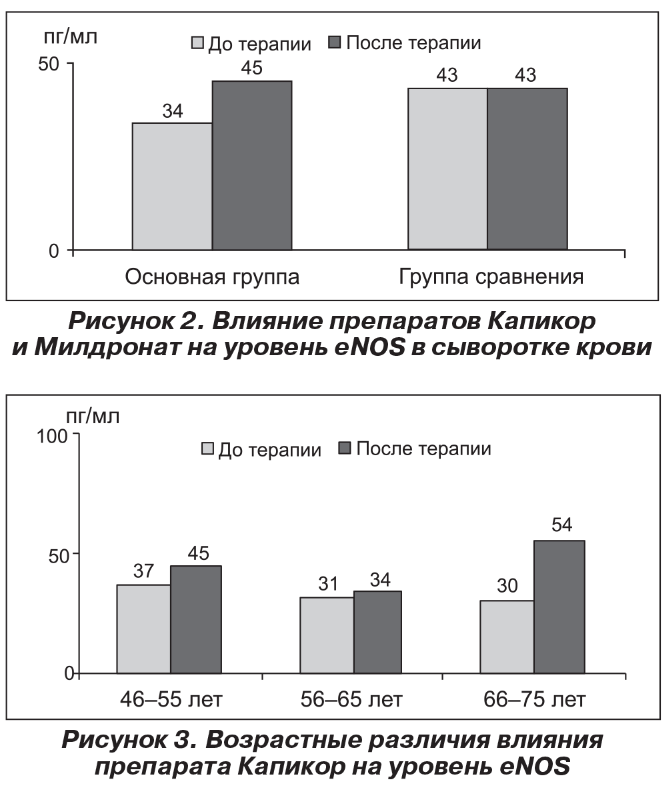
Влияние препарата Капикор на уровень эндотелиальной NO-синтазы (еNOS) в сыворотке крови обследованных больных
Для оценки эффективности препарата Капикор и его влияния на эндотелиальную дисфункцию было проведено исследование содержания еNOS в сыворотке крови у обследованных больных.
В результате терапии наблюдалось повышение содержания еNOS в сыворотке крови у пациентов основной группы (на 24 %) по сравнению с отсутствием изменений у больных контрольной группы (рис. 2).
При этом более выраженное повышение еNOS (на 44 %) в процессе лечения было отмечено у пациентов старшей возрастной группы (от 66 до 75 лет) (рис. 3).
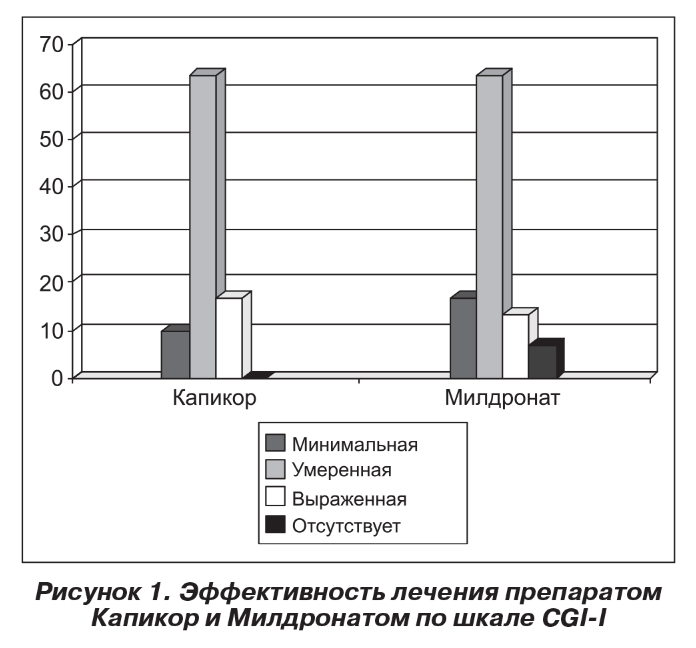
Таблица 6. Средние показатели церебральной гемодинамики и функционального состояния эндотелия
по данным ТКД у исследуемых больных до и после лечения препаратами Капикор и Милдронат
|
Параметры ТКД |
Исследуемая область |
До лечения |
После лечения |
|
|
Капикор |
Милдронат |
|||
|
Линейная скорость кровотока (средняя, см/с) |
ВСА |
30,3 ± 2,7 |
36,0 ± 2,6 |
31,0 ± 1,4 |
|
СМА |
46,2 ± 2,5 |
60,3 ± 4,7* |
46,6 ± 2,5 |
|
|
ПА |
35,0 ± 6,0 |
37,9 ± 7,0 |
36,0 ± 6,0 |
|
|
Пульсационный индекс |
ВСА |
0,90 ± 0,20 |
0,96 ± 0,10 |
0,91 ± 0,10 |
|
СМА |
0,56 ± 0,20 |
0,7 ± 0,2 |
0,6 ± 0,2 |
|
|
ПА |
0,82 ± 0,20 |
0,95 ± 0,20 |
0,80 ± 0,20 |
|
|
Линейная систолическая скорость кровотока (см/с) |
СМА |
62,4 ± 2,6 |
78,7 ± 3,8* |
63,2 ± 2,6 |
|
КИМ (мм) |
|
1,4 ± 0,2 |
1,1 ± 0,2 |
1,3 ± 0,2 |
|
ПЗВ (%) |
Плечевая артерия |
4,2 ± 1,3 |
16,4 ± 1,4* |
6,7 ± 1,5 |
Примечание: * — разница достоверна (р < 0,01).
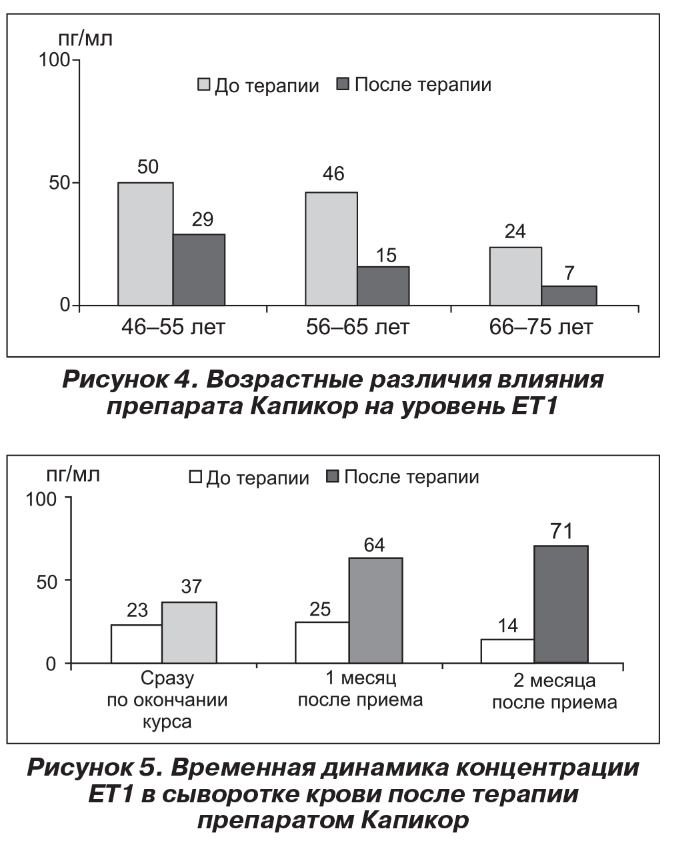
Влияние препарата Капикор на уровень эндотелина-1 (ЕТ1) в сыворотке крови обследованных больных
Для оценки влияния препарата Капикор на эндотелиальную дисфункцию было также проведено исследование содержания уровня ЕТ1 в сыворотке крови обследованных больных.
В ходе терапии наблюдалось снижение в 2 раза уровня ЕТ1 в сыворотке крови большинства пациентов основной группы. У больных группы сравнения таких изменений не наблюдалось.
Обращало на себя внимание увеличение эффективности препарата Капикор с возрастом пациентов. Если в группе пациентов 46—55 лет эффект Капикора проявлялся в снижении ЕТ1 в 1,7 раза, то в следующих возрастных группах — в 3,0 и 3,4 раза соответственно (рис. 4).
Результаты оценки переносимости препарата Капикор
При осмотре и опросе пациентов основной и контрольной групп в ходе настоящего клинического исследования не выявлено каких-либо жалоб, неожиданных побочных реакций, осложнений или явлений непереносимости сравниваемых препаратов Капикор, капсулы, и Милдронат, капсулы.
Отсутствие побочных и токсических эффектов под влиянием терапии препаратом Капикор подтверждается и по данным объективных клинических и лабораторных исследований.
Ни один пациент в обеих сравниваемых группах не предъявлял жалоб и не испытывал каких-либо неприятных ощущений, которые можно было бы связать с действием изучаемых препаратов.
Назначение в течение 28 дней исследуемого препарата не оказало какого-либо влияния на показатели морфологического состава периферической крови, на уровни ее основных биохимических констант и не отразилось на показателях клинического анализа мочи.
Таким образом, по результатам проведенного исследования можно заключить, что препарат Капикор оказывает достаточно выраженное терапевтическое влияние на клинические показатели, когнитивные функции, астеническую симптоматику, церебральную гемодинамику, восстановление функции эндотелия у больных с ДЭ II стадии и СД II типа.
У большинства пациентов зарегистрировано отчетливое улучшение основных когнитивных функций: вербальной памяти — в виде увеличения объемов непосредственного запоминания и долговременной памяти; улучшение функций произвольного внимания, увеличение объемов перерабатываемой информации, уменьшение явлений истощаемости, улучшение скоростных параметров; улучшение качества счетных операций; уменьшение выраженности перцептивно-гностических расстройств; общее повышение когнитивной продуктивности больных.
После курса лечения препаратом Капикор наблюдалась также положительная динамика показателей церебральной гемодинамики по данным ТКД. У пациентов увеличивалась ЛСК в сосудах сонных и позвоночных артерий (на 26 %), нормализовался пульсационный индекс, снижались показатели КИМ, увеличивались показатели ПЗВ (до 16,4 ± 1,4 %), что говорило о восстановлении функции эндотелия.
В пользу восстановления функции эндотелия у пациентов, принимавших Капикор, свидетельствовали и данные биохимических исследований. В ходе терапии препаратом Капикор у больных отмечалось снижение в сыворотке крови уровня ЕТ1 в 2 раза, тогда как у больных группы сравнения таких изменений не наблюдалось. Также у больных основной группы в результате терапии наблюдалось повышение содержания eNOS в сыворотке крови (на 24 %) по сравнению с отсутствием изменений у больных группы сравнения.
Общая частота улучшения различной степени выраженности (шкала CGI-I) у пациентов, получавших Капикор, составила 100 %, тогда как в группе больных, получавших Милдронат, — 93,3 %.
Полученные данные показали, что у пациентов с ДЭ II стадии и СД II типа препарат Капикор более эффективен, чем препарат Милдронат. Это, по-видимому, обусловлено тем, что фиксированная комбинация мельдония и ГББ является более сильным вазорелаксантом, чем ее компоненты по отдельности, что связано с их синергическим эффектом.
ВЫВОДЫ
- В процессе лечения препаратом Капикор отмечена статистически значимая положительная динамика восстановления когнитивных функций и уменьшения выраженности астенической симптоматики. Динамика показателей когнитивной продуктивности по шкале ММSЕ составила 28,4 ± 1,6 балла, увеличиваясь более чем на 3 балла у больных, получавших Капикор, что превышало таковую у пациентов, получавших Милдронат.
- После лечения препаратом Капикор достоверно улучшались показатели церебральной гемодинамики по данным транскраниальной допплерографии: увеличилась линейная систолическая скорость кровотока СМА на 26 %, нормализовался пульсационный индекс, снизились показатели КИМ, увеличились показатели ПЗВ до 16,4 ± 1,4 %, что указывает на восстановление функции эндотелия. В процессе лечения препаратом Милдронат динамика показателей церебральной гемодинамики была незначительной.
- Препарат Капикор хорошо переносится пациентами и не вызывает побочных эффектов при назначении его по 2 капсулы 2 раза в сутки в течение 28 дней.
- Эффективность и безопасность препарата Капикор, капсулы, производства АО «Олайнфарм» определяет перспективу более широкого его применения в медицинской практике, не только для лечения больных с ДЭ II стадии и СД II типа на фоне гипертонической болезни и атеросклеротического поражения сосудов головного мозга, но и для восстановления функции эндотелия, редукции астенических расстройств, замедления темпов прогрессирования дементирующего процесса.
Список литературы
- Волошин П.В., Міщенко Т.С., Лекомцева Є.В. Аналіз поширеності та захворюваності на нервові хвороби в Україні// Международный неврологический журнал. — 2006. — № 3(7). — С. 9-13.
- WHO. World Health Report 2008. — Geneva: World Health Organization, 2008.
- Дамулин И.В., Захаров В.В. Дисциркуляторная энцефалопатия: Методические рекомендации. — М., 2000. — 20 с.
- Трещинская М.А. Теоретические и практические аспекты применения L-аргинина с целью профилактики цереброваскулярной патологии // Укр. мед. часопис. — 2011. — № 5(85). — С. 1-12.
- Сторожаков Г.И., Федотова Г.С., Червякова Ю.Б. Эндотелиальная дисфункция при артериальной гипертензии // Лечебное дело. — 2005. — № 4. — С. 58-64.
- Коноплева Л.Ф. Эндотелиальная дисфункция в патогенезе сердечно-сосудистых заболеваний и методы ее коррекции // Терапия. — 2011. — № 3(56). — С. 26-30.
- Степанов Ю.М., Кононов И.Н., Журбина А.И., Филиппова А.Ю. Аргинин в медицинской практике (обзор литературы) //Журн. АМН України. — 2004. — 10. — 340-352.
- Achan V., Broadhead M., Malaki M. et al. Asymmetric dimethylarginine causes hypertension and cardiac dysfunction in humans and is actively metabolized by dimethylarginine dimethyl- aminohydrolase // Arterioscler. Thromb. Vase. Biol. — 2003. — 23. — 1455-1459.
- Cooke J.P. The endothelium: a new targetfor therapy //Vase. Med. — 2000. — 5. — 49-53.
- Csiszar A., Wang M., Lakatta E.G., Ungvari Z. Inflammation and endothelial dysfunction during aging: role of NF-kappa // B. J. Appl. Physiol. — 2008. — 105. — 1333-1341.
- Adams M.R., Forsyth C.J., Jessup W. et al. Oral L-arginine inhibits platelet aggregation but does not enhance endothelium- dependent dilation in healthy young men // J. Am. Coll. Cardiol. — 1995. — 26. — 1054-1061.
- Bachetti Т., Comini L., Francolini G. et al. Arginasepathway in human endothelial cells in pathophysiological conditions// J. Moll. Cell. Cardiol. — 2003. — 37. — 515-523.
- Besset A., Bonardet A., Rondouin G. et al. Increase in sleep related GH and Prl secretion after chronic arginine aspirate administration in man //Acta Endocrinol. (Copenh.). — 1982. — 99. — 18-23.
- Blum A., Hathaway L., Mincemoyer R. et al. Oral L-arginine in patients with coronary artery disease on medical management // Circulation. — 2000. — 101. — 2160-2164.
- Boger G.I., Rudolph Т.К., Maas R. et al. Asymmetric dimethylarginine determines the improvement of endothelium- dependent vasodilation by simvastatin: effect of combination with oral L-arginine // J. Am. Coll. Cardiol. — 2007. — 49. — 2274-2282.
- Brown-Borg H.M., Rakoczy S.G. Growth hormone administration to long-living dwarf mice alters multiple components of the anti-oxidative defense system //Mech. Ageing Dev. — 2003. — 124. — 1013-1024.
- Buga G.M., Singh R., Pervin S. et al. Arginase activity in endothelial cells: Inhibition by NG-hydroxyarginine during highoutput nitric oxide production // Am. J. Physiol. — 1996. — 271. — 1988-1998.
- Mayer В., John M., Heinzel B. et al. Brain nitric oxide synthase is a biopterin-and flavincontaining multifunctionaloxido- reductase // FEBS Lett. — 1991. — 288. — 187-191.
- 19. Morris C.R., Kuypers F.A., Poljakovic M. et al. Elevated arginase activity and limited arginine availability: a common feature in asthma and sickle cell disease // Nitric. Oxide. — 2004. — 11. — 112.
- Deanfield J.E., Halcox J.P., Rabelink T.J. Endothelial function and dysfunction: testing and clinical relevance // Circulation. — 2007. — 115. — 1285-1295.
- Donato A., Gano L., Eskurza I. et al. Vascular endothelial dysfunction with aging: endothelial and endothelial nitric oxide synthase//Am. J. Physiol. Heart Circ. Physiol. — 2009. — 297. — 425-432.
- Heffernan K.S., Fernhall B. Hemodynamic and vascular response to resistance exercise with L-arginine // Med. Sci. Sports Exerc. — 2009. — 41.— 773-779.
- Li H., Meininger C.J., Hawker J.R. Jr. et al. Activities of arginase landII are limiting for endothelial cell proliferation//Am. J. Physiol. — 2000. — 282. — 64-69.
- OharaY., Peterson Т.Е., Harrison D.G. Hypercholesterolemia increases endothelial superoxide anion production // J. Clin. Invest. — 1993. — 91. — 2546-2551.

