ЖУРНАЛ КАРДИОЛОГИЯ: ОТ НАУКИ К ПРАКТИКЕ 2016. № 2 (21)
Хомазюк Т. А., д-р мед. наук, проф.
Кротова В. Ю., асист.
Кафедра пропедевтики внутрішньої медицини, ДЗ «Дніпропетровська медична академія Міністерства охорони здоров’я України», м. Дніпропетровськ, Україна
Резюме. За результатами обстеження 90 хворих на артеріальну гіпертензію (АГ) II стадії, 1-2 ступенів, контрольовану на фоні антигіпертензивної терапії, із когнітивними порушеннями (КП) дослідили ефективність і безпечність застосування у-аміно-(3-фенілмасляної кислоти гідрохлориду та іпідакрину в комплексному лікуванні хворих, провели аналіз ступенів тяжкості КП, оцінили серцево-судинний ризик, визначили рівень особистісної та реактивної тривожності, вегетативні порушення та якість життя. Інструментальне обстеження: добове моніторування артеріального тиску (ДМАТ); амбулаторний контроль артеріального тиску (AT); електрокардіографія (ЕКГ); ультразвукове дослідження магістральних артерій голови та шиї (УЗД МАГ). Нейропсихологічне обстеження: інтегральна оцінка когнітивних функцій (КФ) за шкалою MMSE; оцінка пам’яті за методикою Лурія «Запам’ятовування 10 слів»; оцінка уваги та швидкості сенсомоторних реакцій за Шульте та за методикою Рибакова. Загальний серцево-судинний ризик визначали за шкалою SCORE, якість життя - за загальноприйнятою методикою SF-36 Health Status Survey, тривогу - за опитувальниками особистісної та реактивної тривожності, вегетативней статус - за методикою Вейна. Установили, що КП характерні для хворих з АГ працездатного віку, навіть за контрольованого AT. Виявлено наявність порушень вербальної пам’яті, пов’язаних з АГ. Показано важливість визначення загального серцево-судинного ризику, діагностики когнітивних розладів і вимірювання товщини комплексу інтима-медіа артеріальної стінки як факторів ураження головного мозку, органа-мішені за АГ 1-2 ступенів. Дослідження якості життя хворих з АГ встановило зниження її рівня за всіма показниками: фізичне функціонування (PF) - 62,02 ± 7,75 балів; фізично-рольове функціонування (RP) - 37,50 ± 8,07 балів; фізичний біль (ВР) - 49,85 ± 4,94 балів; загальне здоров’я (GH) - 52,16 ± 3,56 балів; життєва сила (VT) - 47,63 ± 5,14 балів; соціальне функціонування (SF) - 36,17 ± 3,04 балів; емоційно-рольове функціонування (RE) - 39,06 ± 6,98 балів; ментальне здоров’я (МН) - 51,16 ± 3,48 балів. Для покращення якості життя хворих і довготривалого прогнозу перебігу АГ важлива своєчасна діагностика КП за скринінговою шкалою оцінки КФ MMSE. Корекція КП і вегетативного статусу у хворих з АГ досягається додаванням до антигіпертензивної терапії комбінації середньої терапевтичної дози у-аміно-3-фенілмасляної кислоти гідрохлориду (Ноофен®, 750 мг/добу) та іпідакрину (Нейромідин®, 20 мг/добу) протягом щонайменше 1,5 місяця. Курси лікування доцільні двічі на рік. Комплексна терапія АГ і КП повинна передбачати, окрім антигіпертензивної програми лікування, ще й курсове призначення комбінації інгібітора ацетилхолінестерази та ноотропного препарату (Ноофен® і Нейромідин®, «Олфа»), що приводить до корекції когнітивних розладів, психоемоційного та вегетативного станів, покращує якість життя та підвищує рівень адаптації в соціумі.
Ключові слова: артеріальна гіпертензія, когнітивні порушення, Ноофен®, Нейромідин®.
На сьогодні не існує загальноприйнятих підходів до ефективного лікування когнітивних порушень (КП) у хворих на артеріальну гіпертензію (АГ) і не визначено стандартів їх діагностики. В Україні зареєстровано понад 12 млн хворих на АГ і понад 3 млн людей із різними формами судинних захворювань головного мозку, які зумовлюють зниження когнітивних функцій (КФ) [2, 7,17]. Майже третина цих хворих працездатного віку [13].
Відповідно до анатомічних особливостей кровопостачання головного мозку АГ вражає передусім підкіркові базальні ганглії та глибинні відділи білої речовини, де найчастіше локалізовані лакунарні інфаркти, що є вельми важливим для когнітивної діяльності людини [18, 21]. Одними з перших клінічних проявів ураження підкоркових структур головного мозку за АГ є зниження швидкості реакції та концентрації уваги, підвищена втомлюваність, ригідність інтелекту [8]. Існують погляди, що серцево-судинні захворювання (ССЗ) є фактором не тільки хронічної ішемії головного мозку, а і дегенеративних процесів (деменціі) [20]. Відомо, що тривога та депресія супроводжуються певними змінами в метаболізмі нейромедіаторів і деяких гормонів, що прискорює розвиток нейродегенеративнихзмін у хворих на АГ [11].
Одним із пріоритетних напрямів сучасної кардіології є попередження виникнення та прогресування уражень органів-мішеней у хворих на АГ [12,15]. Основне завдання сучасної антигіпертензивної терапії - зниження ризику розвитку та смертності від ССЗ, тому нині терапія АГ спрямована не тільки на корекцію рівня артеріального тиску (AT) і факторів ризику її виникнення, а і на зворотній розвиток змін у органах-мішенях [14]. Зважаючи на патогенетичну роль АГ щодо КФ, її адекватне та своєчасне лікування можна вважати профілактикою КП. Але профілактичний ефект щодо прогресування КП і виникнення деменції серед антигіпертензивних препаратів було доведено лише у блокаторів ангіотензинових рецепторів (за результатами дослідження MOSES - у-епросартану) [22]. Вплив статинів, діуретиків, інгібіторів ангіотензинперетворювального ферменту, антагоністів кальцію є неоднозначним [12,19]. Тому розробка стратегії профілактики та лікування КП у хворих з АГ є вельми актуальною.
Дискутивним у формуванні КП є патогенетичне значення дисфункції автономної нервової системи, психоемоційного стану хворих, їх позитивного налаштування на лікування, ефективності антигіпертензивної терапії та рівня якості життя [16]. У зв’язку з цим актуальним є питання вивчення ефективності та безпечності ноотропних засобів у лікуванні КП у хворих на АГ. Насамперед викликає зацікавлення похідний від у-аміномасляної кислоти та фенілетиламіну оригінальний ноотропний препарат комплексної дії Ноофен® («Олфа») (діюча речовина - амінофенілмасляна кислота), якому притаманні ноотропний, анти- астенічний, транквілізуючий, аналгетичний і вегетостабілізуючий ефекти [10]. Саме препарати комплексної дії дають змогу уникати поліпрагмазії, але підвищувати ефективність лікування. Застосування Ноофену® приводить до покращення показників добового моніторингу AT (ДМАТ): зменшення варіабельності AT протягом доби, нормалізації вегетативного балансу з позитивною динамікою клінічних проявів вегетативної дисфункції [10].
Останнім часом увагу дослідників і клініцистів привертає й можливість застосування інгібіторів ацетилхолінестерази для патогенетичної терапії КП, пов’язаних із судинним ураженням головного мозку, що базується на ролі ацетилхолінергічної недостатності (центральний холінергічний дефіцит) у їх походженні, а також здатності впливати на нейропластичність, регенерацію та реіннервацію структур центральної нервової системи [5, 6]. Результати окремих клінічних досліджень свідчать про те, що за АГ дебютують м’які та помірні КП, саме тому доцільно використовувати мінімальні дози інгібіторів ацетилхолінестерази, проте лікування повинно бути тривалим і безперервним, аби забезпечити надійність відновлення КФ [3].
Актуальним напрямом корекції КП, що формуються у хворих з АГ, є застосування інгібітора холінестерази Нейромідину® («Олфа») (діюча речовина - іпідакрин). Препарат прискорює процеси адаптивної нейропластичності за периферичними та центральними механізмами через синаптичнута гліальну модуляцію, синаптогенез, нейрогенез, зміну чутливості до нейротрансміттерів, підвищує активність і стимулює процеси реорганізації нейронів у проекційних зонах головного мозку, підвищує рівень нейротрофічного фактора мозку (BDNF) як маркера нейропластичності, має нейропротекторну дію, регулює процеси довготривалої потенціації (головного механізму запам’ятовування та навчання) [5]. Доведено позитивний вплив іпідакрину на КФ за хронічної ішемії мозку, що підтверджено результатами нейропсихологічного тестування та даними досліджень когнітивних викликаних потенціалів [1]. Отримано дані, що іпідакрин уповільнює прогресування КП, є ефективним і безпечним засобом у терапії змішаної деменції легкого та помірного ступенів [1, 3, 4]. Але доказової бази ефективності та безпечності застосування інгібіторів ацетилхолінестерази, а саме іпідакрину у хворих на АГ із КП, немає. Не вивчено також вплив церебропротекторів загалом.
Отже, поширеність когнітивних розладів за АГ, брак стандартів діагностики та, що найголовніше, скринінгу хворих на прийомі лікаря загальної практики та цілеспрямованого лікування КП визначають актуальність проблеми. Отже, поглиблення уявлень про значення синдрому КП у прогнозі перебігу АГ, впливу на якість життя хворих, розширення можливостей адекватної персоніфікованої медикаментозної корекції є актуальним питанням у практиці лікарів-інтерністів (лікарів загальної практики - сімейної медицини, а також суміжних спеціальностей - терапії, кардіології, неврології) та є соціально значущим.
Мета роботи - визначити ефективність і безпечність застосування у-аміно- (3-фенілмасляної кислоти гідрохлоридута іпідакрину в комплексному лікуванні хворих на АГ II стадії, 1-2 ступенів із КП.
МЕТОДИКА ДОСЛІДЖЕННЯ ТА РЕЗУЛЬТАТИ
У дослідженні взяли участь 90 хворих на АГ II стадії, 1-2 ступенів, контрольовану на фоні антигіпертензивної терапії за стандартними протоколами для кардіологічних хворих (Наказ Міністерства охорони здоров’я від 24.05.2012 р. № 384 з урахуванням рекомендацій Європейського товариства кардіологів (European Society of Cardiology, ESC) 2013 p. і Об’єднаного національного комітету з профілактики, виявлення, обстеження та лікування високого кров’яного тиску (The Joint National Committee on Prevention, Detection, Investigation and Treatment of High Blood Pressure, JNC) 2014 p.), у яких діагностували КП. Критерії виключення: ішемічний і/або геморагічний інсульт, черепно-мозкова травма в анамнезі, зловживання алкоголем і/або наркотичними речовинами, депресивний синдром, онкологічні захворювання, оперативні втручання на мозку в анамнезі, ішемічна хвороба серця, симптоматична та резистентна АГ.
Тривалість АГ у досліджених хворих становила 10,7 ± 7,2 років. Більшість із них була у віковій групі від 50 до 59 років - 37,8 %, вікова група від 60 до 70 років становила 26,7 % хворих, від 40 до 49 років - 22,2 %, від ЗО до 39 років - 13,3 % (рисунок 1). Отже, серед хворих домінували особи працездатного віку - 73,3 %. У дослідженні було 44,4 % чоловіків і 55,6 % жінок (рисунок 2).
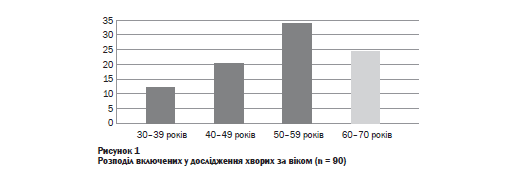
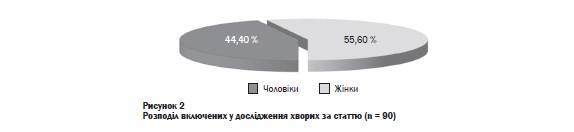
Розподіл на групи проводили шляхом простої рандомізації (за методом «конвертів»). У першу групу дослідження ввійшли ЗО хворих на АГ II стадії, 1-2 ступенів із КП, які додатково до ефективної персоніфікованої антигіпер- тензивної терапії отримували ноотропний засіб у-аміно-Р-фенілмасляної кислоти гідрохлорид (Ноофен®, «Олфа») в дозі 500 мг 2 рази на добу. У другу групу ввійшли ЗО хворих на АГ II стадії, 1-2 ступенів із КП, які додатково до анти- гіпертензивної терапії отримувати у-аміно-Р-фенілмасляної кислоти гідрохлорид (Ноофен®, «Олфа») в дозі 250 мгЗ рази на добу й антихолінестеразний препарат іпідакрин (Нейромідин®, «Олфа») в дозі 10 мг 2 рази на добу. Третю групу порівняння становили ЗО хворих на АГ II стадії, 1-2 ступенів із КП, які отримували лише антигіпертензивну терапію. Курс лікування хворих із КП тривав 45 діб, а спостереження за хворими з повторним визначенням стану та динаміки КФ проводили наприкінці 1-го, 3-го та 6-го місяців дослідження.
Основні демографічні характеристики та індекс маси тіла (ІМТ) обстежених осіб наведено в таблиці 1. У першій групі дослідження було 9 чоловіків і 21 жінка з середнім значенням ІМТ 30,7 ± 4,6 кг/м2, надлишкова маса тіла була в 11 хворих, 17 осіб мали ожиріння. Тривалість АГ - 10,7 ± 7,6 років. У другій групі було 16 чоловіків і 14 жінок, середня величина ІМТ становила 28,4 ± 4,7 кг/м2, надлишкова маса тіла була в 15 хворих, 8 осіб мали ожиріння. Тривалість АГ становила 9,4 ± 8,5 років. Щодо третьої групи хворих (група порівняння), то в неї ввійшло по 15 осіб різної статі з середнім ІМТ 31,2 ±3,7 кг/м2, надлишковою масою тіла в 8 хворих і ожирінням - у 16. Усі три групи хворих були співставними між собою за клінічними характеристиками (р > 0,05). Під час аналізу загального кардіоваскулярного ризику в обстежених із АГ 1-2 ступенів і КП встановлено, що 25 % мали вірогідність розвитку фатальних серцево-судинних подій менше за 1 %, у 17 % ця вірогідність становила 2 %, у 14 % хворих - 3-4 %, у 10 % осіб - 5-9 %, у 6 % - 10-14 %, і тільки б 3 % обстежених 10-річний ризик серцево-судинних подій становив понад 15 %. Таким чином, переважна більшість хворих була з низьким ризиком серцево-судинних подій.
Дизайн дослідження: відкрите, когортне, повздовжнє, контрольоване дослідження в трьох паралельних групах хворих. Дизайн дослідження представлено на рисунку 3.
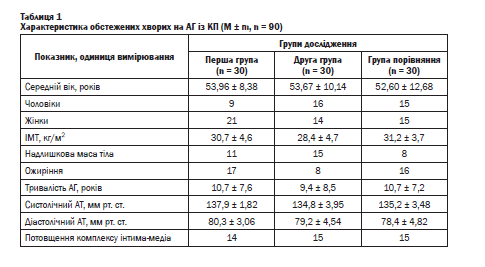
Рисунок З
Дизайн дослідження
Інструментальні методи дослідження:
- ДМАТ апаратом «CardioTens» (Mediteech, Угорщина) [9];
- амбулаторний контроль АД;
- електрокардіографія апаратом «HeartScreen, HS 60G» (Budapest, Угорщина);
- ультразвукове дослідження магістральних артерій голови.
Нейропсихологічне обстеження:
- інтегральна оцінка КФ за шкалою MMSE;
- оцінка пам’яті за методикою Лурія «Запам’ятовування 10 слів»;
- оцінка уваги та швидкості сенсомоторних реакцій за таблицями Шульте та за методикою Рибакова;
- дослідження тривоги за рівнем особистісноїта реактивної тривожності.
Наявність вегетативних порушень визначали за Вейном, якість життя - за загальноприйнятою методикою SF-36 Health Status Survey, а загальний кардіо- васкулярний ризик - за шкалою SCORE. Статистичну обробку результатів проводили з використанням пакету програм Statistica 6.1 (StatSoft Inc., США).
Під час аналізу скарг хворих виявили певні закономірності: погіршення пам’яті через зниження продуктивності процесів уваги, порушення запам’ятовування за збереження довготривалої пам’яті. Для хворих були притаманні швидка втомлюваність, нерівномірність під час виконання завдання, відмова від подальшого виконання через втому та неможливість зосередитися. Зниження розумової працездатності реєстрували в 73,5 % хворих, 94% скаржилися на погіршення стану за зміни погоднихумов. У групі дослідження фактор ризику розвитку АГ за спадковістю виявили в 88,2 % хворих, за наявністю КП - у 85,2%.
Екстракраніальні та транскраніальні магістральні судини в 98 % досліджених хворих не мали гемодинамічно значимих змін і порушень процесів ауто- регуляції. Одна жінка з першої групи спостереження мала помірний вазо- спазм у басейні середньої мозкової артерії, який зник після лікування, кожен другий хворий на АГ II стадії, 1-2 ступенів мав потовщення комплексу інтима-медіа. Середні показники розмірів комплексу інтима-медіа за групами: у першій - 1,15 ± 0,18 мм; у другій - 1,17 ± 0,16 мм; у групі порівняння - 1,16 ± 0,14 мм (р > 0,05).
Оцінка результатів дослідження за методиками Шульте та Рибакова виявила порушення довільної уваги (час виконання завдань - 68,3 ± 7,7 с; ефективність роботи - 64,9 ± 0,9 с), концентрації, розподіл і переключення уваги (помилки під час виконання завдань у 59,3 % хворих). Час адаптації у виконанні завдань становив 1,06 ± 0,09 с. Показники ефективності функцій уваги та часу виконання завдань свідчили про зниження як довільної уваги, так і розумової працездатності. Після лікування хворі обох груп спостереження, на відміну від групи порівняння, демонстрували зменшення часу виконання завдань до 46,4 ± 6,2 су першій групі та до 44,1 ± 7,1 с - у другій, що наближалося до нормальних значень. Також у дослідних групах знижено кількість помилок до 24,1 %, що свідчило про позитивний вплив додаткового призначення ноотропного й антихолінестеразного препаратів на рівень напруженості уваги, темп сенсомоторних реакцій, рівень розумової працездатності та ступінь концентрації збудливих процесів у аналізаторах головного мозку.
Під час аналізу структури КП з’ясували, що їх характеристики на різних рівнях вищих мозкових функцій відповідають усім сферам когнітивної діяльності людини, але більше страждають процеси нейродинамічного характеру (здатність до концентрації уваги, швидкість психомоторних реакцій) і вербальна пам’ять. Під час тестування за ММБЕ в 35,4 % осіб були легкі КП, у 56,1 % - помірні КП і в 8,5 % - деменція легкого ступеня (рисунок 4).
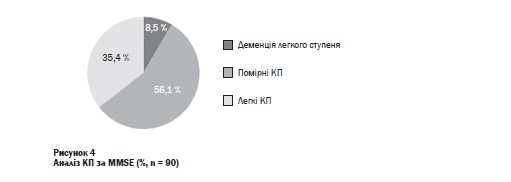
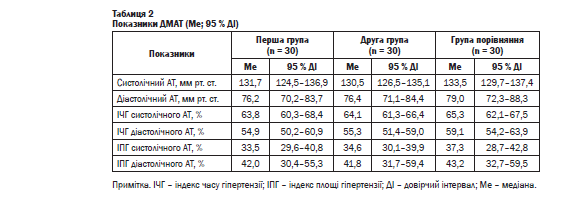
Після лікування переважна більшість хворих (88 %) демонструвала за даними ДМАТ стабілізацію перебігу АГ (таблиця 2).
У першій групі дослідження після лікування, за даними MMSE, 5 хворих (16,6 %) не мали приросту результатів у балах, 19 хворих (63,5 %) мали підвищення на 1 бал, у 5 хворих (16,6 %) реєстрували збільшення на 2 бали, на З бали підвищилися показники в 1 хворого (3,33 %). Суттєві зрушення з покращенням інтегральних показників інтелекту, за даними MMSE, спостерігали в усіх хворих другої групи (рівень приросту: на 1 бал - 11 хворих (36,66%), на 2 бали - 10 хворих (33,3 %), на 3 бали - 7 хворих (23,33 %) і на 4 бали - 2 хворих (6,66 %) (рисунок 5).
Динаміка інтегральних показників інтелекту в другій групі порівняно з першою була достовірно вищою за непараметричним W-критерієм Вілкоксона (Temp > Tkr). У групі порівняння позитивні дані щодо КФ отримано лише в чотирьох хворих (13,3 %): у трьох - підвищення на 1 бал, у одного - на 2 бали. Хворі другої групи на фоні лікування КП демонстрували на 24 % кращу швидкість сенсомоторних реакцій і концентрацію уваги. Показники вербальної пам’яті у хворих першої групи на тлі лікування зросли в середньому на 2-3 слова (об’єм першого відтворення), у другій групі - на 4-5 слів (рисунок 6). Після цілеспрямованого лікування КП 78,6 % хворих досягли нормальних показників ефективності запам’ятовування.
Рисунок 5
Динаміка змін КФ після лікування (Д)за шкалою ММвЕ, бали (п = 90)
1 група 1 група 2 група 2 група Група Група
до лікування після лікування до лікування після лікування порівняння порівняння
Об’єм 2 відтворення О Об’єм 3 відтворення ■ Об’єм 4 відтворення І Об’єм відкладеного відтворення
Рисунок 6
Динаміка змін вербальної пам’яті до та після лікування за методикою Лурія, кількість слів (п = 90)
Стійкі позитивні зміни КФ зберігалися протягом трьох місяців (р > 0,05), але через півроку на контрольному обстеженні в першій групі КП знову почали повільно прогресувати в 6 хворих (20 %), зниження на 2 бали за ММБЕ спостерігали в 1 хворого, а в 5 хворих - на 1 бал. У другій групі показники покращення КФ були більш стійкими, але у двох хворих (6,66 %) виявили зниження на 1 бал, що свідчило про необхідність продовження курсу цілеспрямованого лікування.
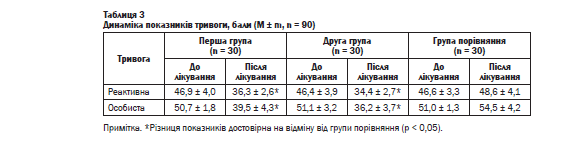
Під час аналізу рівнів тривоги (таблиця 3) виявили, що у хворих групи порівняння був підвищений рівень реактивної та особистої тривоги, незважаючи на ефективний контроль рівнів АТ, а в групах спостереження, де хворим додатково до антигіпертензивноїтерапії призначали препарати, що впливають на показники тривоги, отримали достовірні дані про зниження її рівнів.
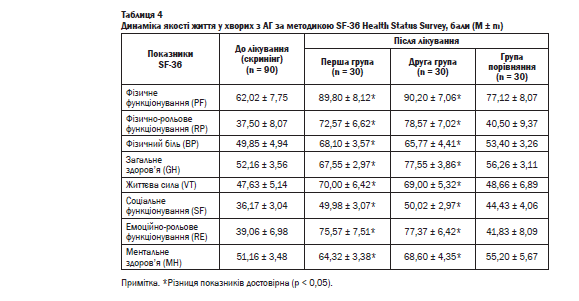
Дослідження якості життя хворих з АГ встановило зниження її рівня за всіма показниками. У перших двох групах дослідження після лікування показники якості життя у хворих достовірно підвищилися, ніж в групі порівняння (таблиця 4).
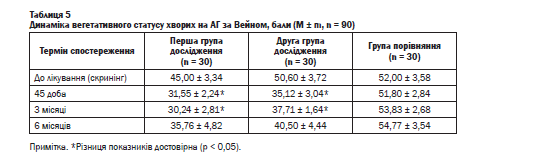
Динаміку вегетативного статусу на фоні лікування представлено в таблиці 5. Достовірне зниження балів за опитувальником Вейна після лікування зафіксовано в першій групі з 45,00 ± 3,34 до 31,55 ± 2,24 балів (р < 0,05) і в другій групі - з 50,60 ± 3,72 до 35,12 ± 3,04 балів (р < 0,05) на відміну від третьої групи, де зміни незначні - з 52,00 ± 3,58 лише до 51,80 ± 2,84 балів (р > 0,05). Навіть через 6 місяців після лікування в перших двох групах хворих зберігаються позитивні зміни, у той час як у групі порівняння реєстрували поглиблення порушень із боку вегетативного статусу на 2,77 бали відносно показників скринінгу. Односпрямоване зменшення клінічних проявів дисфункції автономної нервової системи в першій і другій групах лікування дало підставу стверджувати про позитивну динаміку та фоні фармакотерапевтич- них ефектів у-аміно-р-фенілмасляної кислоти.
Важливими з клінічної точки зору були результати динамічного спостереження у другій групі хворих за додавання до антигіпертензивної терапії комбінації середньотерапевтичної дози у-аміно-Р-фенілмасляної кислоти гідро- хлориду (Ноофен®, 750 мг/добу) та іпідакрину (Нейромідин®, 20 мг/добу) з вірогідним синергічним ефектом поєднання вегетостабілізуючої дії, зменшення тривоги, достовірних позитивних зрушень КФ і покращення якості життя хворих з АГ.
ВИСНОВКИ
- Когнітивні порушення притаманні хворим працездатного віку з АГ навіть за контрольованого АТ.
- Для покращення якості життя хворих і довготривалого прогнозу перебігу АГ важлива своєчасна діагностика КП за скринінговою шкалою оцінки КФ ММЭЕ.
- Корекція КП і вегетативного статусу у хворих з АГ досягається з додаванням до антигіпертензивної терапії комбінації середньої терапевтичної дози у-аміно-р-фенілмасляної кислоти гідрохлориду (Ноофен®, 750 мг/добу) та іпідакрину (Нейромідин®, 20 мг/добу) протягом щонайменше 1,5 місяця. Курси лікування доцільні двічі на рік.
- Комплексна терапія АГ і КП повинна передбачати, окрім антигіпертензивної програми лікування, ще й курсове призначення комбінації інгібітора ацетилхолінестерази та ноотропного препарату (Ноофен® і Нейромідин®, «Олфа»), що приводить до корекції когнітивних розладів, психоемоційного та вегетативного станів, покращує якість життя та підвищує рівень адаптації в соціумі.
Khomazyuk T. A., Doctor of Medical Science, Professor Krotova V. Yu., Teaching Assistant
Department of Propedeutic of Internal Medicine, SE “Dnipropetrovsk Medical Academy of the Ministry of Health of Ukraine”, Dnipropetrovsk, Ukraine
■ Optimizing treatment of cognitive dysfunction in patients with hypertension
SUMMARY
Nowadays there are no universally effective treatment approaches to cognitive dysfunction (CD) in patients with arterial hypertension (AH) and undefined standards of diagnosis.
Purpose. The aim of this study was to determine the effectiveness and safety of nootropic agent (y-amino- P-phenylbutyric acid hydrochloride) and anticholinergic drug (ipidacrinum) in treatment of patients with hypertension stage II with CD.
Methods. The study included 90 patients with hypertension stage II, controlled on a background of antihypertensive therapy on standard protocols for cardiac patients (Order of the Ministry of Health of 24.05.2012 no. 384 with the advice of the European Society of Cardiology (ESC) in 2013 and The Joint National Committee on prevention, detection, investigation and treatment of high blood pressure (JNC), 2014) with diagnosed CD. Exclusion criteria: ischemic and/or hemorrhagic stroke, traumatic brain injury history, alcohol and/or drugs, depressive syndrome, cancer, surgery on the brain, a history of coronary artery disease, symptomatic and resistant hypertension.
The duration of hypertension in the studied patients was 10.7 ± 7.2 years. Most of them were in the age group of 50 to 59 years - 37.8 %, the age group of 60 to 70 years accounted for 26.7 %, patients of 40 to 49 years - 22.2 %, from 30 to 39 years - 13 3 %. Thus, among patients there were dominated people of working age - 73.3 %. The study presented 44.4 % of men and 55.6 % of women. The first study group included 30 patients with hypertension stage II and CD that in addition received antihypertensive effective personalized nootropic agent Y-amino-(3-phenylbutyric acid hydrochloride (Noofen®, “Olfa”) at a dose of 500 mg 2 times per day. The second group included 30 patients with hypertension stage II with CD that in addition to receiving antihypertensive with therapy Y-amino-(3-phenylbutyric acid hydrochloride (Noofen®, “Olfa") at a dose of 250 mg 3 times daily and anticholinergic drug ipidacrinum (Neiromidin®, “Olfa") at a dose of 10 mg 2 times a day. The third group of comparison included 30 patients with hypertension stage II with CD treated with antihypertensive therapy only. The course of treatment lasted about 45 days, and monitoring of patients with redefining the status and dynamics of cognitive functions (CF) was performed at the end of the 1st, 3rd and 6th months of the study.
Instrumental methods: blood pressure daily monitoring with unit “CardioTens" (Mediteech, Hungary); ambulatory blood pressure monitoring; electrocardiography with device “HeartScreen, HS 60G” (Budapest, Hungary); ultrasound of the main arteries of the head. Neuropsychological examination: integrated evaluation of CF with a scale MMSE; Luria's methodology of memory assessment “Memorize 10 words”; evaluation of attention and speed of sensomotor reactions with Schulte tables and the method of Rybakov; study of anxiety in terms of personal and reactive anxiety. The presence of autonomic disorders determined by Wayne, quality of life - with a common method SF-36 Health Status Survey, and total cardiovascular risk - with a SCORE scale.
Results. Established CD characteristic of patients with hypertension in working age, even with controlled blood pressure. Revealed the presence of verbal memory disorders associated with hypertension. Shown the importance of determining the overall cardiovascular risk, diagnosis of cognitive disorders and thickness measurement of intima-media of the arterial wall as factors of brain damage target organs in hypertension. Extracranial and transcranial main vessels in 98 % of surveyed patients had no hemodynamically significant changes and disturbances of autoregulation processes. Every second patient with hypertension stage II has thickening of intima-media. Size averages of intima-media groups: the first - 1.15 ± 0.18 mm; the second - 1.17 ± 0.16 mm; in the control group - 1.16 ± 0.14 mm (p > 0.05). The study of quality of life of patients with established hypertension reducing its level in all aspects: physical functioning (PF) - 62.02 ± 7.75 points; physical and role functioning (RP) - 37.50 ± 8.07 points; bodily pain (BP) - 49.85 ± 4.94; general health (GH) - 52.16 ± 3.56; vitality (VT) - 47.63 ± 5.14; social functioning (SF) - 36.17 ± 3.04; role-functioning emotional (RE) - 39.06 ± 6.98; mental health (MH) - 51.16 ± 3.48 points. Conclusions. To improve the quality of life and long-term prognosis of hypertension is important for timely diagnosis of CD scale screening assessment CF MMSE. Correction of CD and vegetative status in patients with hypertension is achieved by the addition of combination of antihypertensive therapy in average therapeutic dose of y-amino-ß-phenylbutyric acid hydrochloride (Noofen®, 750 mg/day) and ipidacrinum (Neiro- midin®, 20 mg/day) for at least 1.5 months. Courses appropriate treatment are recommended twice a year. Combined therapy of hypertension and CD should include, in addition to antihypertensive treatment programs, and more courses of destination combinations inhibitor of acetylcholinesterase and nootropic agent (Noofen® and Neiromidin®, “Olfa”), which leads to correction of cognitive dysfunction, emotional and vegetative states, improves quality of life and increases level of adaptation in society.
Keywords: hypertension, cognitive dysfunction, Noofen®, Neiromidin®.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
- Баранцевич Е. Р. Эффективность Нейромидина при алкогольной энцефалопатии / Е. Р. Баранцевич // Журнал неврологии и психиатрии. - 2011. - № 3. - С. 49-53.
- Виленский Б. С. Инсульт - современное состояние проблемы / Б. С. Виленский // Неврологический журнал. - 2008. - № 2. - С. 4-10.
- Головкова М. С. Применение нейромидина в терапии сосудистых когнитивных нарушений разной выраженности / М. С. Головкова, В. В. Захаров, М. Ю. Лифшиц [и др.] // Журнал неврологии и психиатрии. - 2007. - № 9. - С. 20-26.
- Дамулин И. В. Использование Нейромидина при смешанной (сосудистой и альцгеймеровской) деменции / И. В. Да- мулин, Д. А. Степкина // Журнал неврологии и психиатрии. - 2011. - № 2. - С. 40-43.
- Живолупов С. А. Нейропластичность: патофизиологические аспекты и возможности терапевтической модуляции / С. А.Живолупов, И. Н. Самарцев//Журнал неврологии и психиатрии. - 2009. - № 4. - С. 78-85.
- Захаров В. В. Нарушения когнитивных функций как медико-социальная проблема / В. В. Захаров // Докгор.Ру. -- № 5. - С. 19-23.
- Коваленко В. М. Динаміка стану здоров’я народу України та регіональні особливості / В. М. Коваленко, В. М. Кор- нацький. - Київ : Моріон, 2013. - 123 с.
- Корнеева О. Н. Патогенетические взаимосвязи артериальной гипертензии и инсулинорезистентности/ О. Н. Корнеева, О. М. Драпкина// Российский кардиологический журнал. - 2006. - № 5. - С. 34-38.
- Кошля В. І. Добовий моніторинг артеріального тиску у клінічній практиці / В. І. Кошля, Т. В. Колесник, Н. К. Мурашко. - Дніпропетровськ, 2005. - 128 с.
- Кузьмінова Н. В. Вегетативні розлади у пацієнтів із гіпертонічною хворобою: діагностика та медикаментозна корекція/ Н. В. Кузьмінова, В. К. Серкова//Український медичний часопис. - 2009. - № 2 (70). - С. 37-41.
- МіщенкоТ. С. Аналіз епідеміології церебровасіулярниххвороб в Україні/Т. С. Міщенко//Судинні захворювання головного мозку. - 2010. - № 3. - С. 2-9.
- Настанова та клінічний протокол надання медичної допомоги »Артеріальна гіпертензія». - Київ, 2012. - 196 с.
- Проблема патології нервової системи в Україні та стан вітчизняної неврологічної служби на межі десятиріччя/ М. К. Хобзей, М. 0. Зінченко, М. В. Голубчиков [та ін.]// Здоров'я України. - 2010. - № 3 (14). - С. 3-4.
- Рекомендації Української асоціації кардіологів з профілактики та ліі^вання артеріальної гіпертензії/ ННЦ«Інс™тут кардіології ім. М. Д. Стражеска НАМИ України». - Київ, 2008. - 79 с.
- Суслина 3. А. Ишемический инсульт: сосуды, сердце, кровь/ 3. А. Суслина // Журнал неврологии и психиатрии. -- № 5. - С. 36-37.
- ХомазюкТ. А. Когнітивні порушення ухворих на артеріальну гіпертензію в реальній лікарській практиці/Т. А. Хома- зюк, В. Ю. Кротова, О. В. Соя [та ін.] // Медичні перспективи. - 2015. - № 2. - С. 42-47.
- Яхно Н. Н. Инсульт как медико-социальная проблема / Н. Н. Яхно, Б. С. Виленский // Русский медицинский журнал. - 2005. - № 13. - С. 807-815.
- Skoogl. Effect of baseline cognitive function and anti hypertensive treatment on cognitive and cardiovascular outcomes: Study on cognition and prognosis in the elderly (SCOPE)/ I. Skoog, H. Lithell, L. Hansson, [et at] // American Journal of Hypertension. - 2005. - Vol. 18. - No. 8. - P. 1052-1059.
- Arima H. Lower target blood pressures are safe and effective for the prevention of recurrent stroke: the PROGRESS trial / H. Arima, J. Chalmers, J. Woodward, [et al ] // Hypertension. - 2006. - Vol. 24. - No. 6. - P. 1201-1208.
- Kerola T. The complex interplay of cardiovascular system and cognition. How to predict dementia in the elderly? / T. Kerola, R. Kettunen, T. Nieminen // International Journal of Cardiology. - 2011. - Vol. 150. - No. 2. - P. 123-129.
- Fang M. Trends in stroke rates, risk, and outcomes in the United States, 1988-2008 / M. C. Fang, M. C. Perraillon, K. Ghosh, [et aI.]//American Journal of Medicine. - 2014. - Vol. 127. - No. 7. - P. 608-615.
- Schrader J. Morbidity and Mortality After Stroke, Eprosartan Compared with Nitrendipine for Secondary Prevention: principal results of a prospective randomized controlled study (MOSES) / J. Schrader, A. Kulschewski, F. Hammersen, [et aI.]//Journal of Stroke and Cerebrovascular Diseases. - 2005. - Vol. 36. - No. 6. - P. 1218-1226.
REFERENCES
- Barantsevich Ye. R. (2011) Effektivnost Neyromidina pri alkogolnoyentsefalopatii [Efficiency of Neuromidin in alcoholic encephalopathy]. Zhurnal nevrologii ipsikhiatrii, vol. 3, pp. 49-53. (in Russ.)
- Vilenskiy B. S. (2008) Insult - sovremennoe sostoyanie problemy [Stroke - modern status of problem]. Nevrologicheskiy zhurnal, vol. 2, pp. 4-10. (in Russ.)
- Golovkova M.S., Zakharov V. V., Lifshitz M. Yu., Yahno N. N. (2007) Primenenie neyromidina vterapii sosudistykh kogni- tivnykh narusheniy raznoy vyrazhennosti [Application of neuromidin in the treatment of vascular cognitive disorders of varying severity]. Zhurnal nevrologii ipsikhiatrii, vol. 9, pp. 20-26. (in Russ.)
- Damulyn I. V., Stepkina D. A. (2011) Ispolzovanie Neyromidina pri smeshannoy (sosudistoy i altsgeymerovskoy) dementsii [Using neuromidin when mixed (Alzheimerand vascular) dementia].Zhuma/nevrologiiipsikhiatrii, vol. 2, pp. 40-43. (in Russ.)
- ZhivolupovS. A., Samartsev J. H. (2009) Neyroplastichnost: patofiziologicheskie aspekty i vozmozhnosti terapevticheskoy modulyatsii [Neuroplasticity: pathophysiological aspects and therapeutic modulation possibilities]. Zhurnal nevrologii i psikhiatrii, vol. 4, pp. 78-85. (in Russ.)
- Zakharov V. V. (2006) Narusheniya kognitivnykh funktsiy kak mediko-sotsialnaya problema [Cognitive impairment as a medical and social problem]. Doktor.Ru, vol. 5, pp. 19-23. (in Russ.)
- KovalenkoV. M., KornatskyV. M. (2013)DynamikastanuzdorovianaroduUkrainytarehionalniosoblyvosti[Dynamicsof the health of the people of Ukraine and regional features]. Kyiv: Morion, 123 p. (in Ukr.)
- Korneeva 0. N., Drapkina О. M. (2006) Patogeneticheskie vzaimosvyazi arterialnoy gipertenzii i insulinorezistentnosti [The pathogenetic relationship of hypertension and insulin resistance]. Rossiyskiy kardiologicheskiyzhurnal, vol. 5, pp. 34-38. (in Russ.)
- Koshlya V. I., Kolesnik T. V., Murashko N. K. (2005) Dobovyi monitorynh arterialnoho tysku и klinichnii praktytsi [Daily monitoring of blood pressure in clinical practice]. Dnipropetrovsk, 128 p. (in Ukr.)
- Kuzminova N. V., Serkova V. K. (2009) Vehetatyvni rozlady u patsiientiv iz hipertonichnoiu khvoroboiu: diahnostyka ta medykamentozna korektsiia [Autonomic disorders in hypertensive patients: diagnostics and pharmacological correction]. Ukrainskyi medychnyi chasopys, vol. 2, no. 70, pp. 37-41. (in Ukr.)
- Mishchenko T. S. (2010) Analiz epidemiolohii tserebrovaskuliarnykh khvorob v Ukraini [Analysis of epidemiology of cerebrovascular diseases in Ukraine]. Sudynnizakhvoriuvannia holovnoho mozku, vol. 3, pp. 2-9. (in Ukr.)
- Nastanova ta klinichnyiprotokol nadannia medychnoidopomohy “Arterialna hipertenziia" [Guidelines and clinical protocols of medical care “Hypertension”]. Kyiv, 2012,196 p. (in Ukr.)
- Khobzey M. K„ Zinchenko M. 0., Golubchikov M. V, Mischenko T. S. (2010) Problema patolohii nervovoi systemy v Ukraini tastan vitchyznianoi nevrolohichnoisluzhby na mezhi desiatyrichchia [The problem of pathology of the nervous system in Ukraine and the state of the domestic neurology service at the border of the decade], Zdorovia Ukrainy, vol. 14, pp. 3-4. (in Ukr.)
- National Scientific Center “Institute of Cardiology named after academician N. D. Strazhesko” of NAMS of Ukraine (2008) Rekomendatsii Ukrainskoi asotsiatsii kardiolohiv z profilaktyky ta likuvannia arterialnoi hipertenzii [Recommendations of Ukrainian Association of Cardiology on prevention and treatment of hypertension]. Kyiv, 79 p. (in Ukr.)
- 15.Suslina Z. A. (2007) Ishemicheskiy insult: sosudy, serdtse, krov [Ischemic stroke: blood vessels, the heart, the blood], Zhurnal nevrologii i psikhiatrii, vol. 5, pp. 36-37. (in Russ.)
- Khomazyuk T. A., Krotova V. Yu., Soya О. V., Yaholnyk V. N. (2015) Kohnityvni porushennia u khvorykh na arterialnu hipertenziiu v realnii likarskii praktytsi [Cognitive impairment in patients with hypertension in actual medical practice], Medychni perspektyvy, vol. 2, pp. 42-47. (in Ukr.)
- Jahno N. N.. Vylenskyy B. S. (2005) Insult как mediko-sotsialnaya problema [Stroke as a medical and social problem], Russkiy meditsinskiyzhurnal, vol. 13, pp. 807-815. (in Russ.)
- Skoog I., Lithell H., Hansson L., Elmfeldt D., Hofman A., Olofsson B., Trenkwalder P., Zanchetti A. (2005) Effect of baseline cognitive function and antihypertensive treatment on cognitiveand cardiovascularoutcomes: Study on cognition and prognosis in the elderly (SCOPE). American Journal of Hypertension, vol. 18, no. 8, pp. 1052-1059.
- Arima H., Chalmers J., Woodward J., Anderson C., Rodgers A., Davis S., Macmahon S., Neal B. (2006) Lower target blood pressures are safe and effective for the prevention of recurrent stroke: the PROGRESS trial. Hypertension, vol. 24, no. 6, pp. 1201-1208.
- Kerola T„ Kettunen R„ Nieminen T. (2011) The complex interplay of cardiovascular system and cognition. How to predict dementia in the elderly? International Journal of Cardiology, vol. 150, no. 2, pp. 123-129.
- Fang M„ Perraillon M. C„ Ghosh K„ Cutler D. M„ Rosen A. B. (2014) Trends in stroke rates, risk, and outcomes in the United States, 1988-2008. American Journal of Medicine, vol. 127, no. 7, pp. 608-615.
- Schrader J„ LQders S„ Kulschewski A., Hammersen E, Plate K„ Berger J., Zidek W„ Dominiak P„ Diener H. C. (2005) Morbidity and Mortality After Stroke, Eprosartan Compared with NitrendipineforSecondary Prevention: principal results of a prospective randomized controlled study (MOSES). Journal of Stroke and Cerebrovascular Diseases, vol. 36, no. 6, pp. 1218-1226.

