ЖУРНАЛ МЕДИЧНІ ПЕРСПЕКТИВИ, 12 / ТОМ XVI I / 2
Н. И. Сьяксте, М. Я. Дзинтаре, И. Я. Калвиньш
Латвийский институт органического синтеза
Ключевые слова: Капикор, Милдронат, Вазонат, Мельдониум, у-бутиробетаин
Существует современная концепция об эндотелии как о мишени для профилактики и лечения патологических процессов, приводящих или реализующих сердечно-сосудистые заболевания. Под эндотелиальной дисфункцией понимают дисбаланс физиологических механизмов и биологических веществ, которые в норме обеспечивают гомеостаз и тонус сосудов. Среди множества биологически активных веществ, вырабатываемых эндотелием, важнейшим является оксид азота - N0. N0 является универсальным ключевым ангиопротективным фактором, который необходим для поддержания нормального базального тонуса сосудов. Поэтому основой нового клинического направления стал тезис о необходимости коррекции дисфункции эндотелия (т.е. нормализации функции эндотелия) как показателя адекватности терапии. Представлены результаты экспериментальных исследований, которые установили, что если к Мельдонию добавляется необходимое количество ГББ, тогда эффект от этой комбинации наступает незамедлительно. Так как ГББ по своей геометрии напоминает ацетилхолин, то повышение концентрации ГББ в плазме крови влечет за собой активацию ацетилхолиновых рецепторов на эндотелии кровеносных сосудов. Активация ацетилхолиновых рецепторов на эндотелии кровеносных сосудов вызывает индукцию биосинтеза N0-радикалов. Таким образом был создан оригинальный регулятор эндотелиальной функции Капикор (Мельдоний + у-бутиробетаин), сочетающий в себе достоинства цитокорректора Мельдония и широкие возможности эндотелийпротектора у-бутиробетаина.
SUMMARY
There is a modern concept about endothelium as a target for prophylactic and treatment of the pathological processes leading to or realizing cardiovascular diseases. We consider an endothelium dysfunction as disbalance of physiological mechanisms and biological substances which ensure homeostasis and vascular tone in normal condition. Nitric oxide (NO) is the most important biologically active substance among abundance of biologically active substances developed by endothelium. NO is an universal key angioprotective factor which is necessary for maintenance of normal basal vascular tone. That's why the thesis about necessity of correction of endothelium dysfunction (i.e. normalization of endothelium function) became basis of a new clinical trend and this correction to be as an indicator of therapy response. The article presents results of experimental trials which have established that if necessary quantity of Gammabutyrobetaine is added to Meldonium then we see an immediate effect from this composition. As y-butyrobetaine is similar by its geometry to acetylcholine so an increase in concentration of y-butyrobetaine in blood plasma involves activation of acetylcholine receptors located on blood vessels endothelium. Activation of the acetylcholine receptors located on blood vessels endothelium causes an induction of NO-radicals biosynthesis. Thus, an original regulator of endothelium function, Capicor (Meldonium + y-butyrobetaine) was developed. It combines advantages of cytocompensator Meldonium and wide potentialities of endothelium protect y-butyrobetaine.
Keywords: Capicor, Mildronat, Vasonat, Meldonium, y-butyrobetaine
1. ВВЕДЕНИЕ
Адекватное и непрерывное снабжение энергией клеток является необходимым условием для нормального функционирования целого организма и отдельных органов. Мозг и сердце - самые уязвимые с этой точки зрения органы. Жирные кислоты и глюкоза - главные источники производства энергии в человеческом организме. Окисление жирных кислот обеспечивает производство приблизительно 80% энергии поставляемой человеческому сердцу, однако этот процесс потребляет чрезвычайно много кислорода. Следует учитывать и то, что в случае ишемических явлений промежуточные продукты окисления жирных кислот накапливаются в клетках организма и нарушают целостность клеточных мембран, вызывая их гибель. Поэтому защита клеток против цитотоксических метаболитов или цитопротекция является одной из наиболее перспективных стратегий лечения губительных последствий ишемии.
В середине семидесятых годов в Латвийском Институте органического синтеза Иваром Калвиньшом и другими исследователями была начата разработка нового лекарственного препарата, который известен под международным непатентованным названием (INN) Мельдоний. Действующим веществом Мельдония является 3-(2,2,2-триметилгидразиний) пропионата дигидрат. Это лекарство широко используется в медицинской практике с 1984 года под названием Милдронат®, а с недавнего времени и под названием Вазонат®.
Как известно, механизм действия Мельдония включает в себя ингибирование ГББ-гидроксилазы, которая превращает Y-бутиробетаин (ГББ) в карнитин. В результате этого постепенно (в течение 10 дней) происходит снижение концентрации карнитина и накопление ГББ, что приводит к оптимизации энергопроизводства в ишемизированных клетках. К сожалению, этот процесс происходит медленно, и лечебный эффект Мельдония начинает проявляться лишь после того, как концентрация ГББ во всем организме существенно возрастет, что ограничивает применение Мельдония в острых случаях нарушения кровообращения.
При анализе механизма действия Мельдония было высказано предположение о том, что этот недостаток Мельдония можно устранить, создав такую комбинацию Мельдония и ГББ, которая обеспечивала бы незамедлительное повышение концентрации ГББ до нужного уровня. Экспериментальные исследования подтвердили эту гипотезу, так как было установлено, что если к Мельдонию добавляется необходимое количество ГББ, то эффект от этой комбинации наступает незамедлительно (12, 13). Таким образом был создан оригинальный комбинированный препарат-цитопротектор нового поколения Капикор (Мельдоний + Y-бутиробетаин), который сочетает в себе достоинства предшественника Мельдония и широкие возможности оксида азота (N0).
Было показано, что именно ГББ и его эфиры ответственны за индукцию биосинтеза N0, который, в свою очередь, является молекулой мессенджером, принимающей активное участие в регуляции тонуса кровеносных сосудов, переноса сигнала в ЦНС и активизации иммунной системы. Благодаря выверенному соотношению двух действующих веществ - Мельдония и ГББ, Капикор по сравнению с Мельдонием более быстро и мощно проявляет именно N0-зависимые эффекты в регуляции сосудистого гомеостаза, что открывает широкие перспективы для применения Капикора в клинике.
2. ВОЗДЕЙСТВИЕ НА ЭНДОТЕЛИАЛЬНУЮ ДИСФУНКЦИЮ - НОВАЯ СТРАТЕГИЯ ПРЕВЕНТИВНОЙ КАРДИОНЕВРОЛОГИИ
В свете современных биохимических и патофизиологических представлений эндотелиальные клетки являются автономным сердечно-сосудистым эндокринным органом, выполняющим ряд важнейших функций. Эндотелий принимает участие в высвобождении вазоактивных веществ и дезагрегантов, участвует в фибринолизе, регуляции иммунных реакций. Клетки эндотелия имеют собственную ферментативную активность, воздействуют на гладкомышечные клетки, регулируя их рост и защищая от действия вазоконстрикторов. Изучение роли эндотелия в патогенезе
сердечно-сосудистых заболеваний (ССЗ) привело к пониманию, что эндотелий регулирует не только периферический кровоток, но и другие важные функции. Именно поэтому объединяющей стала концепция об эндотелии как о мишени для профилактики и лечения патологических процессов, приводящих к ССЗ и реализующих их. Понимание многоплановой роли эндотелия уже на качественно новом уровне вновь приводит к достаточно известной, но хорошо забытой формуле «здоровье человека определяется здоровьем его сосудов».
Ведущая концепция превентивной кардионеврологии основана на оценке и коррекции так называемых факторов сердечно-сосудистого риска. Объединяющим началом для всех таких факторов является то, что рано или поздно, прямо или косвенно все они вызывают повреждение сосудистой стенки, и прежде всего, в ее эндотелиальном слое. Поэтому можно полагать, что одновременно они же являются факторами риска дисфункции эндотелия (ДЭ) как наиболее ранней фазы повреждения сосудистой стенки и в дальнейшем развития атеросклероза, артериальной гипертензии, ишемической болезни сердца и т.д.
Т.о. под эндотелиальной дисфункцией понимают дисбаланс физиологических механизмов и биологических веществ, которые в норме обеспечивают гомеостаз и тонус сосудов. Поэтому основой нового клинического направления стал тезис о необходимости коррекции дисфункции эндотелия (т.е. нормализации функции эндотелия) как показателя адекватности терапии. Среди множества биологически активных веществ, вырабатываемых эндотелием, важнейшим является оксид азота (N0). Сегодня - это самая изучаемая молекула, вовлеченная в патогенез ССЗ.
РИСУНОК 1.
Метаболизм и транспорт карнитина на уровне организма и точки ингибирующего действия Мельдония
Сокращения: ТМЛ - триметиллизин; ТМАМА - триметиламино- масляный альдегид
3. ОКСИД АЗОТА (II) (ОКИСЬ АЗОТА, МОНООКСИД АЗОТА, N0): НОВЫЕ ВОЗМОЖНОСТИ ДАВНО ИЗВЕСТНОЙ МОЛЕКУЛЫ. NO-ЗАВИСИМЫЕ ЭФФЕКТЫ
За два последних десятилетия было установлено, что оксид азота (NO) обладает широким спектром биологического действия. NO, являясь одним из вторичных мессенджеров (переносчиков сигнала), участвует в регуляции систем внутри- и межклеточной сигнализации. В 1998 году трое американцев - Фурчготт, Игнарро и Мюрад - были удостоены премии Нобелевского комитета по физиологии «за открытия, касающиеся оксида азота, как сигнальной молекулы в сердечно-сосудистой системе». Выяснилось, что оксид азота является универсальным биологическим регулятором и содержится практически во всех тканях человеческого организма. Эффект воздействия определяется концентрацией оксида азота.
В организме человека NO синтезируется из аминокислоты L-аргинин под влиянием ферментов NO-синтаз (NOS). Под влиянием эндотелиальной NO-синтазы происходит синтез физиологических уровней оксида азота. Образующийся из L-аргинина NO активирует в гладкомышечных клетках гуанилатциклазу, стимулирующую синтез циклического гуанозинмонофосфата (ц-ГМФ), который в свою очередь обусловливает вазодилатацию. Характерной особенностью NO является способность быстро (менее чем за 5 секунд) диффундировать через мембрану синтезировавшей его клетки в межклеточное пространство и легко проникать в клетки-мишени. Внутри клетки он активирует одни энзимы и ингибирует другие, таким образом, участвуя в регуляции клеточных функций. По сути, оксид азота (N0) является локальным тканевым гормоном. Целый ряд научных исследований доказали участие N0 во многих физиологических процессах.
N0 является универсальным ключевым ангиопротективным фактором, который необходим для поддержания нормального базального тонуса сосудов. Оксид азота подавляет пролиферацию гладкой мускулатуры сосудов, предотвращая тем самым патологическую перестройку сосудистой стенки (ремоделирование), прогрессирование атеросклероза. N0 обладает антиоксидантным действием, ингибирует агрегацию и адгезию тромбоцитов, адгезию нейтрофилов к эндотелию, миграцию моноцитов.
Кроме того, оксид азота участвует в различных процессах в нервной, репродуктивной и иммунной системах. N0 также обладает цитотоксическими и цитостатическими свойствами. Клетки-киллеры иммунной системы используют оксид азота для уничтожения бактерий и клеток злокачественных опухолей. С нарушением биосинтеза и метаболизма N0 связаны такие заболевания, как эссенциальная артериальная гипертензия, ишемическая болезнь сердца, инфаркт миокарда, первичная легочная гипертензия, бронхиальная астма, невротическая депрессия, эпилепсия, нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона), сахарный диабет, импотенция и др.
РИСУНОК 2.
Схема транспорта жирных кислот и Р-окисления в митохондриях с указанием мест ингибирующего действия Мельдония
Сокращения: КПТ I - карнитин- пальмитоилтран- сфераза I;КПТ II - карнитин- пальмитоилтран- сфераза II;
КАТ - карнитин-ацетил- трансфераза; КАКТ - карнитин-ацилкарнитин-транслоказа.
4. ПРИМЕНЕНИЕ МЕЛЬДОНИЯ В КАРДИОЛОГИИ И НЕВРОЛОГИИ. КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
В связи с тем, что механизм действия Мельдония направлен в первую очередь на энергосбережение клеток, а воздействие на сосудистый компонент вторично и развивается медленно, рассмотрим основные результаты многочисленных клинических исследований, которые подтверждают мультимодальное цитопротекторное действие Мельдония. Включение Мельдония в комплексную терапию заболеваний сердечно-сосудистой системы (различные формы ИБС: острый коронарный синдром, стабильная стенокардия; ХСН) способствовало улучшению сократительной функции миокарда и гемодинамических показателей, регрессу ремоделирования ишемизированного миокарда при ишемии и реперфузии. Мельдоний улучшает качество жизни пациентов, повышает толерантность к физической нагрузке, улучшает систолическую функцию, уменьшает периферическое сопротивление артерий, позволяет уменьшить прием нитратов и других антиангинальных средств (7, 9). Методом перфузионной сцинтиграфии при исследовании кровоснабжения миокарда ЛЖ, после инфаркта миокарда, было выявлено достоверное снижение глубины дефекта перфузии (12). Имеются данные и об антиаритмическом действии Мельдония (Милдроната) при наличии ИБС и желудочковых экстрасистол (8). Патогенетически обоснованным является включение Мельдония в курс терапии ишемического инсульта. У больных, принимающих Мельдоний (Милдронат), выявлено улучшение мозговой гемодинамики, неврологической симптоматики, а также электрофизиологических и нейропсихологических показателей (2, 6, 16, 18). При постинсультных двигательных и когнитивных расстройствах, на фоне приема Мельдония, выявлено улучшение устойчивости и походки пациентов, улучшение ориентации и памяти, снижение нейродинамических расстройств (5). Мельдоний (Милдронат) оказался эффективным для лечения дисциркуляторной энцефалопатии, осложненной инсулиннезависимым сахарным диабетом (15). Эффективно назначение препарата и при лечении диабетической периферической сенсомоторной нейропатии (14).
5. ЭКСПЕРИМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Эффективность применения препарата в клинике избавляет нас от необходимости подробно излагать здесь результаты экспериментальных исследований, тем более, что это было сделано ранее (Sjakste and Kalvinsh, 2006; Sjakste et al., 2005). Остановимся лишь на наиболее интересных результатах последних лет в отношении эффектов, которые могут быть объяснены с учетом регуляции синтеза NO под влиянием Мельдония. Сообщалось, что назначение Мельдония в болюсном введении увеличило выживание животных после экспериментально вызванного инфаркта миокарда и улучшило биоэнергетические параметры ишемизированного миокарда у крыс. Увеличивался кровоток в дуге аорты и уменьшалось периферическое сопротивление в кровеносных сосудах, увеличивался кровоток в каротидной, брыжеечной и бедренной артериях (Ratunova T.M.).
Неожиданный результат был получен нами при исследовании воздействия Мельдония на крысах с экспериментальной моделью сепсиса. Однократное введение Мельдония (Милдроната (120 мг/кг)) снижало патологическую продукцию супероксидных радикалов вдвое, уменьшало эндотелиальную дисфункцию, стимулируя биосинтез оксида азота (NO). Таким образом, препарат мог бы быть рекомендован для лечения нарушений мозгового кровообращения при сепсисе (Sjakste et al., 2004). Эффективен препарат и при периферической невропатии при экспериментальном диабете (Sokolovska et al., 2011). Длительное курсовое введение Мельдония (100 мг/кг, 4 месяца) уменьшало размер атеросклеротических бляшек у подверженных быстрому развитию атеросклероза мышей (Vilskersts et al., 2009). В целом результаты экспериментальных исследований выглядят многообещающе - применение Мельдония в клинике в будущем, безусловно, расширится.
6. КАРНИТИН-ЗАВИСИМЫЙ МЕХАНИЗМ ДЕЙСТВИЯ МЕЛЬДОНИЯ, ОБЕСПЕЧИВАЮЩИЙ МУЛЬТИМОДАЛЬНОЕ ЦИТОПРОТЕКТОРНОЕ ДЕЙСТВИЕ
Мельдоний был задуман как аналог карнитина, основной фармакологический эффект Мельдония достигается путем ингибирования Y-бутиро- бетаингидроксилазы и снижения р-окисления жирных кислот (Sjakste and Kalvinsh, 2006; Sjakste et al., 2005). Как известно, большая часть энергии, используемая клеткой в нормальных условиях, образуется в результате окисления жирных кислот. Однако в условиях нехватки кислорода для клетки более выгодно использовать окисление глюкозы, чем жирных кислот, так как для этого процесса необходимо меньшее количество кислорода. Карнитин является переносчиком (играет роль «челнока») длинноцепочечных жирных кислот через внутреннюю митохондриальную мембрану для их р-окисления в матрице митохондрий. В организме человека карнитин синтезируется из триметиллизина (ТМЛ), далее аминокислота гидроксилируется, превращается в гидрокситриметиллизин, который в цепи реакций, протекающих как в митохондриях, так и в цитозоле клетки, образует Y-бутиробетаин (ГББ), гидроксилирование последнего дает карнитин. Последний этап этого биосинтеза у человека происходит в печени, почках, головном мозге и семенниках. Транспортируется карнитин в кардиомиоциты, волокна скелетных мышц и другие клетки натрий-зависимым транспортером OCTN 2. Рис. 1 представляет в обобщенном виде схему биосинтеза и транспорта карнитина в организме, там же указаны точки приложения Мельдония. В цитозоле свободные жирные кислоты захватываются ферментом КоА и образуется ацил-КоА, который передает остаток жирной кислоты карнитину, образовавшийся под действием карни-тинацилтрансферазы ацилкарнитин с помощью карнитин-ацилтранслоказы доставляет карнитин внутрь митохондрий, где из ацилкарнитина вновь образуется ацил-КоА. Последний при наличии кислорода подвергается ß-окислению, а в случае отсутствия кислорода просто накапливается и блокирует транспорт уже синтезированного АТФ из митохондрий в цитозоль, а также разрушает мембраны. Ограничение потока длинноцепочечных жирных кислот через мембраны митохондрий защищает клетку от гибели в условиях кислородного голодания, в то время как короткоцепочечные жирные кислоты могут проникать в митохондрии свободно и окисляться там. Это означает, что Мельдоний практически не способен оказывать токсическое действие на дыхание митохондрий, так как блокирует окисление не всех жирных кислот. Кроме того, предотвращается интенсивное потребление кислорода и накопление кардиотоксичных промежуточных продуктов ß-окисления: ацил-КоА, ацилкарнитина. Клетки переключаются на окисление глюкозы - альтернативный процесс производства АТФ, который требует на 12% меньше кислорода на каждую произведенную молекулу. Этот механизм был подробно обобщен и проанализирован ранее (Шутенко и др., 1995; Simkhovich et al, 1988; Dambrova et al., 2002; Sjakste and Kalvinsh, 2006; Sjakste et al., 2005), однако в последние годы были получены новые факты в его подтверждение, которые, безусловно, заслуживают упоминания. Латвийскими исследователями описана кристаллическая трехмерная структура Y-бутиробетаингидроксилазы (Tars et al., 2010), охарактеризовано и место связывания Мельдония с этим ферментом. Помимо ингибирующего эффекта на биосинтез карнитина Мельдоний, как оказалось, способен блокировать транспорт карнитина внутри митохондрий путем ингибирования карнитин-ацил-трансферазы. Позже было показано, что Мельдоний ингибирует №+-зависимый транспорт карнитина в культивируемые мышечные трубочки и изолированные миоциты. Показано, что OCTN 2 транспортирует Мельдоний даже более эффективно, чем карнитин (Grigat et al., 2009), что даже позволило выдвинуть гипотезу о том, что этот транспортер является главной мишенью Мельдония. Гипотезу подтверждает и вызываемое Мельдонием компенсаторное увеличение экспрессии гена OCTN 2 в почках (Schürch et al., 2010), и экспрессия данного транспортера в эндотелии предсердий человека (Grube et al., 2006). Получены новые данныео возможном ингибировании Мельдонием и карнитин-ацилкарнитинтранслоказы (Oppedisano et al., 2008). Таким образом, Мельдоний эффективно снижает синтез карнитина посредством ингибирования: 1) Y-бутиробетаингидроксилазы; 2) OCTN 2; 3) карнитин-ацетилтрансферазы и 4) карнитин-ацилкарнитинтранслоказы. Кроме того, имеются данные об увеличении почечной экскреции карнитина и конкурентном ингибировании транспорта карнитина через мембрану микроворсинок щеточной каймы почек, которое считается столь же важным в механизме действия Мельдония как и блок биосинтеза карнитина.
Получены убедительные доказательства отсутствия неблагоприятного воздействия препарата на функции сердца и печени. Несмотря на ингибирование окисления жирных кислот, сразу в двух исследованиях отмечено отсутствие стеатоза печени у животных, длительно получавших Мельдоний (Liepinsh et al., 2009; Trumbeckaite et аl., 2009). Все вышесказанное подтверждает, что Мельдоний при помощи ряда различающихся механизмов способен регулировать в клетках количество доступного карнитина и вместе с тем скорость окисления длинноцепочечных жирных кислот, что является необходимым инструментом регуляции энергетического метаболизма в условиях кислородного голодания. Однако, для лечебного эффекта важно не только снизить уровень карнитина, но также повысить уровень Y-бутиро-бетаина. Объяснить этот эффект может второй карнитин-независимый механизм действия, способствующий проявлению NО-зависимых эффектов, которые наиболее сильно выражены у Капикора (комбинация Мельдоний + Y-бутиробетаин).
7. «БЫСТРЫЙ», КАРНИТИН-НЕЗАВИСИМЫЙ МЕХАНИЗМ ДЕЙСТВИЯ КАПИКОРА (МЕЛЬДОНИЙ + Y-БУТИРОБЕТАИН), СПОСОБСТВУЮЩИЙ ИНДУКЦИИ ЭНДОТЕЛИЕМ ОКСИДА АЗОТА
Снижение уровня карнитина в организме возможно лишь при длительном курсовом введении Мельдония. ГББ синтезируется всеми соматическими клетками, скорость его биосинтеза контролируется интенсивностью образования и потребления энергии и концентрацией карнитина - переносчика жирных кислот к месту их утилизации через митохондриальные мембраны. Поэтому падение концентрации карнитина вызывает увеличение скорости биосинтеза его предшественника - ГББ, а в случае снижения потребности в энергии или избыточного накопления карнитина - подавляется биосинтез ГББ. В случае блокирования Y-бутиробетаингидроксилазы, Y-бутиробетаинББ), который при гидроксилировании превращается в карнитин, может подвергаться этерификации. Структура сложного этилового эфира Y-бутиробетаина поразительно напоминает структуру ацетилхолина. Furchgott (1980) обнаружил, что ацетилхолин взаимодействует с рецепторами клеток эндотелия кровеносных сосудов, приводит к образованию малых молекул, мигрирующих в мышечный слой и вызывающих его расслабление, впоследствии которые были идентифицированы как NО-радикалы. Т.о. активация ацетилхолиновых рецепторов на эндотелии кровеносных сосудов вызывает индукцию биосинтеза NО-радикалов.
Доказано, что «быстрый», карнитин-независимый механизм действия Мельдония усиливается при его одновременном применении вместе с Y-бутиробетаином (ГББ). Эта комбинация предотвращала вазоконстрикцию, вызванную ингибитором синтазы оксида азота (Kalvinsh, Veveris, 1999), т.о. комбинация Мельдония и ГББ оказалась более сильным вазорелаксантом, чем ее компоненты в отдельности (Sjakste et аl., 2004).
Как же объяснить быстрые эффекты Мельдония + ГББ, а также зависимость от оксида азота? Объяснение может дать предложенная И.Я. Калвиньшем гипотеза о существовании определенной системы передачи сигнала, основанной на сложных эфирах Y-бутиробетаина (Kalvinsh et аl., 2006). ГББ легко этерифицируется, структура этилового эфира ГББ имеет те же центры связывания с рецептором, что и ацетилхолин. Гипотетический механизм «быстрого» действия препарата можно представить себе следующим образом:
- Введение Мельдония сдвигает равновесие между гидроксилированием ГББ до карнитина в сторону образования эфиров ГББ. Эфиры ГББ физиологически активны, их эффекты развиваются очень быстро.
- Эфиры ГББ связываются со специфическими рецепторами и/или т-ацетилхолиновыми рецепторами, ГББ-эстераза гидролизует связанные с рецепторами эфиры подобно ацетилхолинэстеразе.
- Гидролиз эфиров ГББ запускает передачу сигнала с возможным участием вторичных мессенджеров (Рис. 3). Было доказано, что эфиры ГББ связываются с ацетилхолиновыми рецепторами, то есть эфир ГББ оказался мощным агонистом т-ацетилхолиновых рецепторов (Dambrova et al., 2004), молекулярная структура этих соединений позволяет им связываться с активным центром ацетилхолинэстеразы (Kalvinsh et аl., 2006; Sjakste et аl., 2005). Оксид азота оказался самым подходящим кандидатом на роль вторичного мессенджера
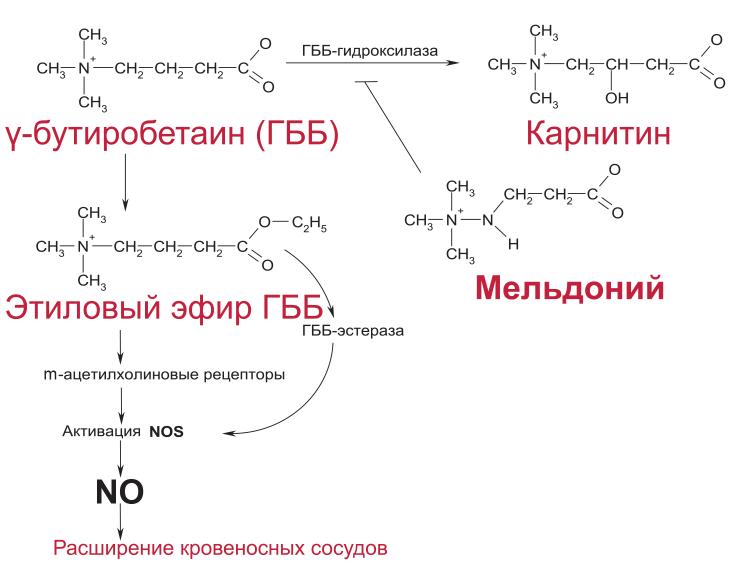
РИСУНОК 3. Механизм действия Капикора Сокращения: ГББ - у-бутиробетаин; ГББ-эстераза - у-бутиробетаин- эстераза.
для передачи сигнала после гидролиза эфиров ГББ. Вышеупомянутые результаты обеспечивают доказательство того, что эфиры ГББ являются мощными NО-зависимыми вазорелаксантами, а сам ГББ - слабым вазорелаксантом, однако Мельдоний усиливал его эффект (Sjakste et аl., 2004). Нам удалось уловить небольшое и быстро проходящее увеличение синтеза окиси азота в некоторых органах крыс после введения Мельдония (Dzintare et al., 2002; Sjakste etl., 2004). Интересно, что по времени (15-30 мин после введения) этот эффект совпадал с падением давления у некоторых людей, принявших разовую дозу Мельдония (Эниня и др., 1991; Sokolovska et al., 2006). Ни Мельдоний, ни ГББ, ни эфиры последнего не взаимодействуют непосредственно с синтазами оксида азота, поэтому возможно только опосредованное рецепторами действие.
Учитывая вышеприведенные соображения, механизм действия Капикора (Мельдоний + у-бутиробетаин) можем представить себе следующим образом:
- Одновременное введение Мельдония и ГББ сопровождается быстрым накоплением эфиров ГББ, так как концентрация ГББ высокая, а Мель- доний не позволяет гидроксилировать ГББ.
- Образующиеся эфиры ГББ связываются со своими специфическими рецепторами и/или с т-ацетилхолиновыми рецепторами.
- Происходит активация эндотелиальной синтазы оксида азота и биосинтез окиси зота.
- Оксид азота вызывает вазорелаксацию и ряд других механизмов - 140-зависимых эффектов.
ЗАКЛЮЧЕНИЕ. КАПИКОР - ИННОВАЦИОННЫЙ ОРИГИНАЛЬНЫЙ МОДУЛЯТОР ФУНКЦИИ ЭНДОТЕЛИЯ
Таким образом, в отличие от Мельдония комбинация Мельдоний + у-бутиробетаин способствует в большей степени физиологическому образованию эфиров ГББ и впоследствии более быстрому синтезу оксида азота. Быстрое наступление
NО-зависимых эффектов является основным преимуществом Капикора. Следовательно более выраженные и быстрые NО-зависимые эффекты обеспечивают Капикору мощное кардио- и церебропротективное действие, которое выгодно отличает его от предшественников. В последнее время заметен лавинообразный рост числа научных публикаций по исследованию роли оксида азота и возможно впереди нас ждет еще много открытий по изучению его функций.
Как отметил лауреат Нобелевской премии Луи Игнарро: «Оксид азота имеет решающее значение для здоровья и долголетия. Разница между здоровьем и заболеванием зависит от уровня и активности оксида азота в организме».
Литература в редакции

