ЖУРНАЛ КЛІНІЧНА ІМУНОЛОГІЯ. АЛЕРГОЛОГІЯ. ІНФЕКТОЛОГІЯ. № 9–10 (78–79) 2014
С. И. Ильченко, Н. В. Науменко, Н. Л. Пинаева
ГУ «Днепропетровская медицинская академия МЗ Украины», Городской детский аллергологический центр
Атопический дерматит (АД) — одна из важных проблем в педиатрии, так как его распространенность неуклонно возрастает; отмечено более раннее появление первых признаков заболевания у детей на первом году жизни, возросла доля больных с рецидивирующим течением, торпидным к традиционной терапии [1—4].
Основной симптом АД — зуд. Он появляется первым при обострении заболевания и регрессирует последним, доставляет больному ребенку дискомфорт, нарушает сон и активную деятельность, снижает качество жизни. Механизм развития зуда — высвобождение гистамина из тучных клеток, фиксированных в тканях (в случае АД — в коже). В связи с особенностями патогенетического механизма заболевания, одним из ведущих компонентов в лечении таких пациентов является воздействие на медиаторный механизм воспалительной реакции, в частности блокирование на том или ином уровне участия в ней гистамина.
В настоящее время наиболее обсуждаемым вопросом является рациональность использования антигистаминных препаратов (АГП) I поколения, обладающих выраженным противозудным и седативным действием, в терапии АД. На практике, вследствие того, что зуд у большинства пациентов усиливается в ночное время, эти препараты часто назначают в вечернее время, на ночь. Вместе с тем, было установлено, что даже однократный прием седативных АГП вечером влияет на работоспособность, скорость реакции, способность к обучению в течение последующего дня. Вторым недостатком препаратов этой группы является постепенное снижение терапевтической активности (свойство, называемое тахифилаксией), которое развивается довольно быстро. В-третьих, эти препараты могут вызывать слабость, усталость, сухость во рту, несколько реже — мышечную дистонию, задержку мочеиспускания, запор. Иногда, чаще у детей раннего возраста, наблюдается парадоксальный стимулирующий побочный эффект применения АГП I поколения: бессонница, гиперрефлексия, повышенная возбудимость, головная боль, тремор. Вместе с тем, тяжелые побочные реакции на эту группу препаратов крайне редки, а их проти- возудная активность очевидна, в связи с чем АГП I поколения могут с успехом применяться для купирования зуда у детей с АД [5—7].
Особое место в ряду АГП занимает представитель оригинального класса Н1-антагонистов — хинуклиди новых производных — хифенадин (Фенкарол), который был специально разработан с целью исключения седативного эффекта. В отличие от других АГП I поколения Фенкарол обладает высоким сродством к Н1- рецепторам, не оказывает побочного воздействия на сердечно-сосудистую систему и пищеварительный тракт. Важным преимуществом этого препарата является практически полное отсутствие седативного эффекта и других побочных влияний на центральную нервную систему и вегетативные функции.
Противоаллергические свойства Фенкарола шире, чем у АГП I поколения. Это связано с тем, что помимо блокады ^-рецепторов Фенкарол активирует фермент диаминоксидазу (гистаминазу), инактивирующую гистамин и, соответственно, снижающую уровень гистамина в тканях. Это уникальное свойство обеспечивает дополнительную антиаллергическую активность препарата. Следует заметить, что Фенкарол разрешен к применению у детей раннего возраста [5, 6].
Основной задачей данного исследования являлась сравнительная оценка эффективности препарата Фенкарол при лечении АД у детей дошкольного возраста.
Материалы и методы исследования
Обследовано 35 детей с АД в стадии обострения. Средний возраст больных составил 6,4±2,6 года. В исследовании участвовали 3 группы: основная (п=15) — получали хифенадин и традиционную терапию, первая группа сравнения (п=10) — дезлоратадин и традиционную терапию, вторая группа сравнения (п=10) — цетиризин и традиционную терапию.
Основные критерии включения: дети дошкольного возраста; АД, период обострения. Критерием исключения являлся инфекционно-токсический дерматит. Дети были рандомизированы по возрасту, тяжести течения и обострения АД. Оценка тяжести симптоматики обострения АД проводилась нами по 3-балльной шкале (0 — симптомы отсутствуют, 1 — выражены слабо, 2 — выражены умеренно, 3 — выражены сильно).
Дизайн проводимых исследований у пациентов представлен в табл. 1.
Критериями эффективности считали: снижение активности дерматита при объективном осмотре кожи, отсутствие свежих очагов воспаления, снижение зуда по линейке субъективной интенсивности зуда, нормализация сна. Переносимость препарата оценивалась исследователем по следующей шкале: хорошая, удовлетворительная, неудовлетворительная.
Результаты исследования и их обсуждение
Результаты ежедневного анкетирования пациентов и их родителей, заполнения ими дневника самонаблюдения, а также их контрольных визитов к врачу продемонстрировали, что у пациентов основной группы положительная динамика клинических признаков обострения АД (интенсивность кожного зуда, распространенность и выраженность кожных высыпаний, нарушение сна) отмечалась в существенно более короткие сроки (р<0,05 и р<0,01) для всех случаев.
В группе детей, получавших Фенкарол, симптоматика регрессировала значительно быстрее, причем к 11-му дню наступала полная ремиссия. У пациентов, которым была назначена терапия лоратадином или цетири- зином, к концу 2-й недели лечения сохранялся выраженный зуд и к 15-му дню, когда видимых симптомов со стороны кожи почти не наблюдалось, сохранялся зуд выраженностью в 1—2 балла.
Уже через 2,78+0,11 дня после начала приема Фенкарола у пациентов основной группы нами отмечено существенное снижение выраженности кожного зуда, что наступило у обследованных из групп сравнения через 3,96+0,13 и 3,78+0,1 дня соответственно (р<0,01; табл. 2). Полностью кожный зуд был купирован у пациентов основной группы также быстрее, чем у обследованных из группы сравнения (через 6,17+0,23 и 13,83+0,29, 13,03+0,75 дня соответственно, при р<0,05). Распространенность и выраженность кожных высыпаний значительно уменьшились в основной группе через 3,22+0,15 дня, а в группах сравнения — через 4,96+0,32 и 4,76+0,22 дня соответственно (р<0,01).
Таблица 1. Схема обследования пациентов
|
Обследование пациентов |
До лечения |
1-й день |
7-й день |
10-й день |
14-й день |
|
Оценка соответствия пациента критериям включения/исключения |
+ |
+ |
+ |
+ |
|
|
Назначение лечения |
|
+ |
|
|
|
|
Общеклиническое обследование |
+ |
+ |
+ |
+ |
+ |
|
Лабораторное обследование: |
|
|
|
|
|
|
• общий анализ крови с определением абсолютного количества |
|
|
|
|
|
|
эозинофилов • общий анализ мочи |
+ |
|
|
|
+ |
|
• ^Е в сыворотке крови |
|
|
|
|
|
|
• биохимический анализ крови |
|
|
|
|
|
|
Линейка субъективной интенсивности зуда |
+ |
+ |
+ |
+ |
+ |
|
Оценка активности АД |
+ |
+ |
+ |
+ |
+ |
|
Выявление и регистрация побочных явлений |
+ |
+ |
+ |
||
|
Оценка эффективности и переносимости |
+ |
+ |
+ |
+ |
+ |
|
Наличие свежих скарификатов |
+ |
+ |
+ |
+ |
+ |
Таблица 2. Динамика клинических симптомов (дни) у обследованных пациентов
|
Симптомы |
Основная группа |
Г руппа сравнения 1 |
Г руппа сравнения 2 |
|||
|
Улучшение |
Исчезновение |
Улучшение |
Исчезновение |
Улучшение |
Исчезновение |
|
|
Интенсивность кожного зуда |
2,78±0,11* |
6,17±0,23* |
3,96±0,13 |
13,83±0,29 |
3,78±0,1 |
13,03±0,75 |
|
Распространенность и выраженность кожных высыпаний |
3,22±0,15* |
9,72±0,36* |
4,96±0,19 |
13,6±0,44 |
4,76±0,22 |
12,6±0,41 |
|
Нарушение сна |
2,39±0,10* |
3,52±0,16 |
3,61±0,13 |
4,91 ±0,20 |
3,72±0,11 |
4,73±0,20 |
Примечание: *достоверность различий между соответствующими показателями в основной группе и группах сравнения, при p<0,05.
Таблица 3. Динамика лабораторных показателей у обследованных детей на фоне проводимой терапии
|
Гематологические показатели |
Основная группа |
Гуппа сравнения 1 |
Г руппа сравнения 2 |
|||
|
До лечения |
14-й день терапии |
До лечения |
14-й день терапии |
До лечения |
14-й день терапии |
|
|
Лейкоциты, 10,2/л |
6,5±1,9 |
6,9±1,7 |
7,1±1,8 |
6,5+1,6 |
6,9+1,6 |
6,8+2,1 |
|
Эозинофилы, % |
7,3±2,4 |
4,7±1,1* |
7,7+1,9 |
3,8+1,9* |
6,9+2,7 |
4,3+1,5* |
|
Эозинофилы, 109/л |
0,61±0,16 |
0,41±0,11* |
0,71 ±0,21 |
0,49+0,09* |
0,69+0,15 |
0,31+0,19* |
|
IgE, кЕ/л |
114,7±19,8 |
106,7±21,4 |
108,7+24,5 |
103,7+23,5 |
99,8+17,8 |
109,7+20,8 |
Примечание:* достоверность различий показателей до лечения и на фоне лечения при p<0,01.
Полностью кожные высыпания были купированы у пациентов основной группы также значительно быстрее, чем у обследованных из группы сравнения (через 9,72±0,36 и 13,6±0,44, 12,6±0,41 дня соответственно, при р<0,01). Аналогичным образом у пациентов группы сравнения улучшение и нормализация сна отмечены через 2,39±0,10 и 3,52±0,16, а у обследованных в группах сравнения — через 3,61±0,13 и 4,91±0,20 дня соответственно, при р<0,05 для обоих случаев. В 92% случаев (14/15), когда в терапию был включен Фенкарол, родители пациентов оценили эффект как отличный и хороший, в то время как в группах сравнения этот процент составил только 65% (13/20), различия достоверны, р<0,05. У 66,7% (10 детей), принимавших Фенкарол, отмечали значительное улучшение состояния уже на 3-й день, что выражалось в спокойном сне и нормальной дневной активности за счет значительного уменьшения выраженности зуда. В группах сравнения динамика клинических изменений была практически одинаковой (р>0,1), а на уменьшения зуда в первые 3 дня заболевания указала только четверть родителей (5/20), р<0,05.
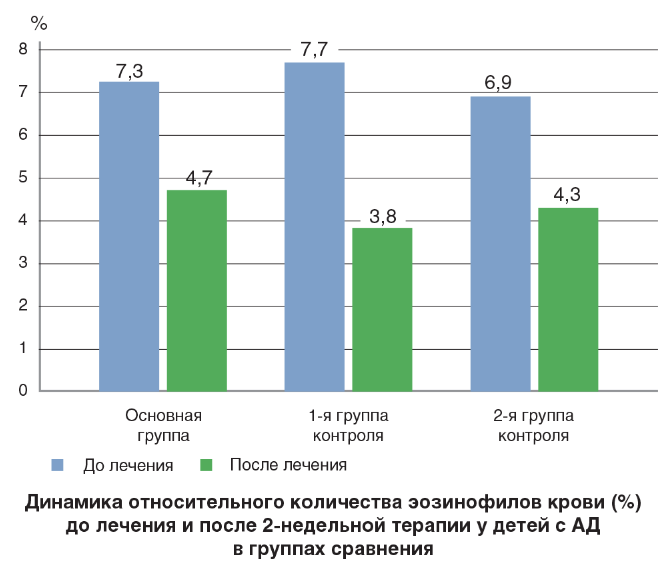
Следует отметить, что снижение уровня как относительного, так и абсолютного количества эозинофилов в крови пациентов на фоне терапии отмечалось во всех группах (см. рисунок). В основной группе до лечения — 0,61±0,16х109/л, 7,3±2,4%; на 14-й день терапии — 0,41±0,11х109/л, 4,7±1,1%, р<0,01. В группе сравнения 1 до лечения — 0,71±0,21х109/л, 7,7±1,9%; на 14-й день терапии — 0,49+0,09х109/л, 3,8±1,9%, р<0,01. В группе сравнения 2 до лечения — 0,69±0,15х109/л, 6,9±2,7%; на 14-й день терапии — 0,31±0,19х109/л, 4,3±1,5%, р<0,01. Достоверного отличия этих показателей между тремя группами не было (табл. 3).
Достоверных изменений уровня ^Е в сыворотке крови детей на фоне терапии не было ни в одной из групп (в основной группе и группах сравнения 1 и 2 до лечения — 114,7+19,8 кЕ/л, 108,7±24,5 кЕ/л и 99,8+17,8 кЕ/л; на фоне терапии — 106,7+21,4 кЕ/л, 103,7+23,5 кЕ/л, 109,7+20,8 кЕ/л соответственно, р>0,01).
Ни у кого из детей не наблюдалось сонливости и других побочных реакций при приеме Фенкарола, переносимость препарата оценена нами как хорошая.
Выводы
Таким образом, включение в режим терапии детей с обострением АД препарата Фенкарол по сравнению с референтными препаратами (лоратадин и цетири- зин) позволило в существенно более короткие сроки купировать основные и наиболее мучительные патологические симптомы данного заболевания (интенсивность кожного зуда, распространенность и выраженность кожных высыпаний, нарушение сна). Препарат показал себя безопасным средством для лечения данного заболевания у детей дошкольного возраста.
Литература
- Аллергический ринит, атопический дерматит: образовательная программа для педиатров // Педиатрическая фармакология. — 2007. - № 4 (прилож.). - 64 с.
- Maintz L. Histamine and histamine intolerance / L . Maintz, N. Novak // Am. J. Clin. Nutr. - 2007; 85: 1185-1196.
- Church M.K. Risk of first-generation H1-antihistamines: a GA- 2LEN position paper / M.K. Church, M. Maurer, F.E. Simons // Allergy. - 2010; 65: 4: 435-444.
- Keller GA. Antihistamines: past answers and present questions / GA. Keller, G.Di Girolamo // Drug. Saf. - 2010; 5: 1: 58-64.
- Недельская С.Н. Лечение атопического дерматита в острый период / С.Н. Недельская, Е.Д. Кузнецова, И.В. Солодова // Український журнал дерматології, венерології i косметологи! - 2008; 3: 64-67.
- Яшина Л.А. Фенкарол - эффективное противовоспалительное средство при лечении персистирующего аллергического ринита легкой и средней степени тяжести / ЛА. Яшина, Ю.И. Фещен- ко, В.А.Игнатьева // Астма та алергія. - 2004; 1-2: 41-48.
- Белан Э.Б. Профилактика ПНЯ у детей с атопическим дерматитом // Э.Б. Белан, М.В. Гутов, Л.В. Лабай // РАЖ. - 2006; 4: 49-53.

