Український неврологічний журнал, № 4, 2012
СТИМУЛЮВАННЯ НЕЙРОПЛАСТИЧНОСТІ — ПЕРСПЕКТИВНИЙ НАПРЯМ У ТЕРАПІЇ ІШЕМІЧНОГО ІНСУЛЬТУ
Л. І. СОКОЛОВА1, В. С. МЕЛЬНИК1, В. Ю. ШАНДЮК1, М. М. СЕПІХАНОВА1, Г. М. ЛЄТОВАЛЬЦЕВА2, О. В. КОСТОВЕЦЬКИЙ2
1 Національний медичний університет ім. О.О. Богомольця, Київ
2 Київська міська клінічна лікарня № 4
Мета — вивчити вплив іпідакрину в пацієнтів з гострим ішемічним інсультом на динаміку відновлення рухових функцій, досягнутий рівень рухової активності, динаміку змін когнітивних функцій та ступінь вираження і поширеність постінсультної депресії.
Матеріали і методи. Проведено комплексне клініко-неврологічне обстеження 45 пацієнтів (22 чоловіків та жінок) у гострий період інфаркту мозку півкульної локалізації. Середній вік пацієнтів — (66,7 ± 1,4) року. Пацієнти були розподілені на дві групи. Основну становили 30 хворих (середній вік — (66,8 ± 1,3) року), які на тлі традиційної терапії отримували протягом 1—5 діб захворювання іпідакрин 0,5 % у дозі 1,0 мл внутрішньом'язово один раз на добу, в наступні 6—10 діб — іпідакрин 1,5 % у дозі 1,0 мл внутрішньом'язово один раз на добу, у період з 11-ї до 40-ї доби — таблетовану форму іпідакрину (20 мг) тричі на добу. До контрольної групи ввійшли 15 хворих (7 чоловіків та 8 жінок), які за демографічними показниками були порівнянними з пацієнтами основної групи та отримували традиційну терапію ішемічного інсульту. Програма обстеження передбачала використання шкал МНЗЗ та ММЗЕ, таблиць Шульте, шкали Гамільтона та індексу Бартел.
Результати. Виявлено кращу динаміку відновлення неврологічних функцій (за шкалою МНЗЗ) у пацієнтів основної групи, а різниця середнього бала щодо групи контролю ставала достовірною, починаючи з 14-ї доби захворювання (р < 0,05). Також, починаючи з 14-ї доби захворювання, встановлено нижчий рівень інвалідизації у пацієнтів основної групи ((82,8 ± 3,0) бала) порівняно з групою контролю ((77,5 ± 2,9) бала; р < 0,05) за індексом Бар- тел. Достовірно кращу динаміку відновлення когнітивних функцій спостерігали на тлі терапії іпідакрином, достовірну різницю фіксували, починаючи з 14-ї доби захворювання (р < 0,05). На тлі застосування іпідакрину відзначено позитивну динаміку депресивних розладів, з поступовим відновленням позитивної емоційної сфери на відміну від групи контролю, в якій спостерігали поглиблення депресивних симптомів на 14-ту добу, що, на нашу думку, пов'язано з гіршою динамікою усунення неврологічного дефіциту.
Висновки. Використання іпідакрину в комплексному лікуванні хворих на гострий ішемічний інсульт сприяє кращому відновленню неврологічних функцій, зниженню рівня інвалідизації та підвищенню ефективності реабілітаційних заходів. Виявлено також позитивний вплив на психоемоційну сферу — поліпшення когнітивних функцій, зменшення частоти та ступеня вираження депресивних розладів, що сприяє функціональному відновленню пацієнтів.
Ключові слова: ішемічний інсульт, іпідакрин, відновлення неврологічних функці.
Проблема ішемічного інсульту головного мозку, беззаперечно, залишається однією з найактуальніших у сучасній неврології. За матеріалами ВООЗ, частота інсультів становить від 1,5 до 7,4 випадку на 1000 населення в різних країнах. У 2005 р. інсульт був причиною 5,7 млн смертельних випадку. Прогнозують зростання смертності внаслідок інсульту до 6,7 млн у 2015 р. та до 7,8 млн — у 2030 р. [2] і понад 100 тис. — в Україні [9], серед них до 80 % припадає на ішемічний інсульт.
За даними реєстру, проведеного в Росії, 31 % хворих, які вижили після інсульту, потребують постійного догляду, а 20 % не можуть самостійно пересуватися, тільки 20 % здатні повернутися до трудової діяльності [4]. Лише на медичне обслуговування пацієнтів з гострим ішемічним інсультом у розвинених країнах щороку витрачають від 4 до 6 % коштів, виділених на охорону здоров'я [3]. Віддалені результати лікування ішемічного інсульту залежать від адекватності організаційних та лікувально-профілактичних заходів [12].
З усіх наслідків інсульту найкраще вивчено рухові розлади, які у вигляді парезів трапляються у 80—90 % осіб, що перенесли інфаркт мозку [10], та у більшості випадків поєднуються з мовними розладами (у 25—30 % пацієнтів), порушеннями чутливості (у 30—35 %) та координації (менш ніж у 15 % пацієнтів). З огляду на те, що геміпарез — це найпоширеніша причина інвалідизації у неврологічних хворих [11], розроблено схеми реабілітації, спрямовані на ефективне відновлення рухових функцій за допомогою різних вправ [15]. Значно менше уваги приділяють іншим наслідкам: постін- сультним когнітивним та емоційно-вольовим розладам, соціальній дезадаптації.
Відновлення будь-яких утрачених неврологічних функцій (починаючи з другої доби захворювання) відбувається, насамперед, завдяки процесам нейропластичності — сукупності різних процесів ремоделювання синаптичних зв'язків, які спрямовані на оптимізацію нейронних мереж [13]. Виділяють такі види нейропластичності: 1) еволюційна — забезпечує розвиток простих нейронних мереж у надскладні мультимодальні мережі, здатні здійснювати вищі психічні функції; 2) онтогенетична — пов'язана з індивідуальним розвитком особи, забезпечує пристосування організму до зовнішнього та внутрішнього середовища; 3) фізіологічна — пов'язана з фізіологічною активацією функціональних систем; 4) реактивна — забезпечує короткочасну активацію синапсів після дії різних патологічних факторів; 5) адаптаційна — тривала активація існуючих функціональних систем мозку в процесі адаптації організму до зовнішнього середовища; 6) репаративна — забезпечує відновлення функціональних систем мозку після їх пошкодження [5]. Різні відділи головного мозку мають різний нейропластичний потенціал: найпластичнішою вважають кору головного мозку, що зумовлено різноманітністю клітинних елементів та їх зв'язків. Окрім того, має значення організація вищих кіркових функцій, яка, з одного боку, чітко локалізована в певних зонах, з другого — «розширена», багата на паралельні й реципрокні зв'язки та зони перекриття, що, насамперед, характерно для таких функцій, як увага, гнозис, складні рухові акти, мовлення [1].
Особливу роль у процесах нейропластичності відводять модуляції активності трансмітерів — ацетилхоліну, серотоніну, норадреналіну, дофаміну та ін. Важливою особливістю нейротрансмітерів є здатність моделювати взаємну активність. Під час активації процесів нейропластичності відбувається активація цереброваскулярної реактивності та змінюється церебральна гемодинаміка під впливом структурних перебудов центральних моторних та сенсорних проекційних ділянок кори півкуль головного мозку.
Таким чином, сучасна диференційована терапія гострого ішемічного інсульту має бути спрямована на посилення процесів нейропластичності з метою відновлення втрачених рухових та когнітивних функцій за допомогою медикаментозних засобів комплексної дії, які впливають одночасно на різні ланки патогенезу захворювання. В нашому дослідженні ми використовували препарат іпідакрин (АО «ОІаіпРагт», Латвія), дія якого пов'язана з інгібуванням ацетилхолінестерази та блокуванням калієвих і натрієвих каналів мембрани нейронів. Іпідакрин позитивно впливає на всі ланки проведення збудження: стимулює пресинаптичні нервові волокна, збільшує викид нейромедіатора в синаптичну щілину, пригнічує руйнування ацетилхоліну в синаптичній щілині, підвищує активність постсинаптичної клітини прямим мембранним та опосередкованим нейромедіаторним впливом, що сприяє відновленню рухових, чутливих та когнітивних функцій [6].
Мета дослідження — вивчити вплив іпідакрину в пацієнтів з гострим ішемічним інсультом на динаміку відновлення рухових функцій, досягнутий рівень рухової активності, динаміку змін когнітивних функцій та ступінь вираження і поширеність постінсультної депресії.
Матеріали і методи
Проведено комплексне клініко-неврологічне обстеження 45 пацієнтів (22 чоловіків та 23 жінок) у гострий період інфаркту мозку півкульної локалізації (вогнище ішемії — в басейні середньої мозкової артерії (СМА)). У дослідження залучали лише пацієнтів з гострим ішемічним порушенням мозкового кровообігу, яке виникло вперше. Середній вік пацієнтів становив (66,7 ± 1,4) року (від 41 до 79 років). У 28 (60 %) пацієнтів вогнище ураження локалізувалося в басейні правої СМА, у решти — лівої СМА.
Пацієнтів вибірковим методом розподілили на дві групи: до основної групи ввійшли 30 хворих (15 жінок та 15 чоловіків) віком від 41 до 77 років (середній вік — (66,8 ± 1,3) року), які на тлі традиційної терапії отримували протягом 1—5 діб захворювання іпідакрин 0,5 % у дозі 1,0 мл внутрішньом'язово один раз на добу, у наступні 6—10 діб — іпідакрин 1,5 % у дозі 1,0 мл внутрішньом'язово один раз на добу, в період з 11-ї до 40-ї доби — таблетовану форму іпідакрину (20 мг) тричі на добу. До контрольної групи ввійшли 15 хворих (7 чоловіків та 8 жінок), які за демографічними показниками були порівнянними з пацієнтами основної групи та отримували традиційну терапію ішемічного інсульту.
У дослідженні застосовано такі методики: визначення тяжкості неврологічного дефіциту за шкалою МН55 на 1-шу, 7-му (± 1), 14-ту (± 1) та 40-ву (± 3) добу захворювання. Починаючи з 7-ї доби захворювання, проводили дослідження вищих психічних функцій за допомогою шкали ММ5Е, тесту запам'ятовування 10 слів і таблиць Шульте.
Вищі психічні функції досліджували скринінговим методом за допомогою шкали ММ5Е, що складається з низки субтестів, які дають змогу оцінити стан нетривалої і тривалої пам'яті, мовну функцію, гнозис та праксис. Ця методика — досить проста та зручна у використанні в повсякденній практиці. Ми використали таку оцінку суми балів: 30—26 балів — когнітивні функції не порушені, 25—23 бали — когнітивне зниження, 22—20 балів — легка постінсультна деменція, < 19 балів — помірна постінсультна деменція, < 12 балів — виражена постінсультна деменція.
Для виявлення постінсультної депресії використовували шкалу Гамільтона, яка передбачає підрахунок загальної кількості балів за 21 пунктом. Сума балів від 7 до 16 відповідає легкій депресії, від 17 до 27 — депресії середньої тяжкості, понад 27 балів — тяжка депресія.
Ефективність реабілітаційних заходів оцінювали за індексом Бартел: діапазон від 0 до 45—50 балів відповідає тяжкій інвалідності хворого, залежності його від сторонньої допомоги, 51—75 балів — помірній інвалідності, від 76 до 100 балів — мінімальному обмеженню або усуненню неврологічного дефіциту.
Результати та обговорення
Вихідний рівень неврологічного дефіциту в пацієнтів основної групи за шкалою МН55 у середньому становив (7,3 ± 0,6) бала, а в групі контролю — (7,2 ± 0,7) бала. Дані щодо динаміки середнього бала неврологічного дефіциту за шкалою МН55 наведено на рис. 1.
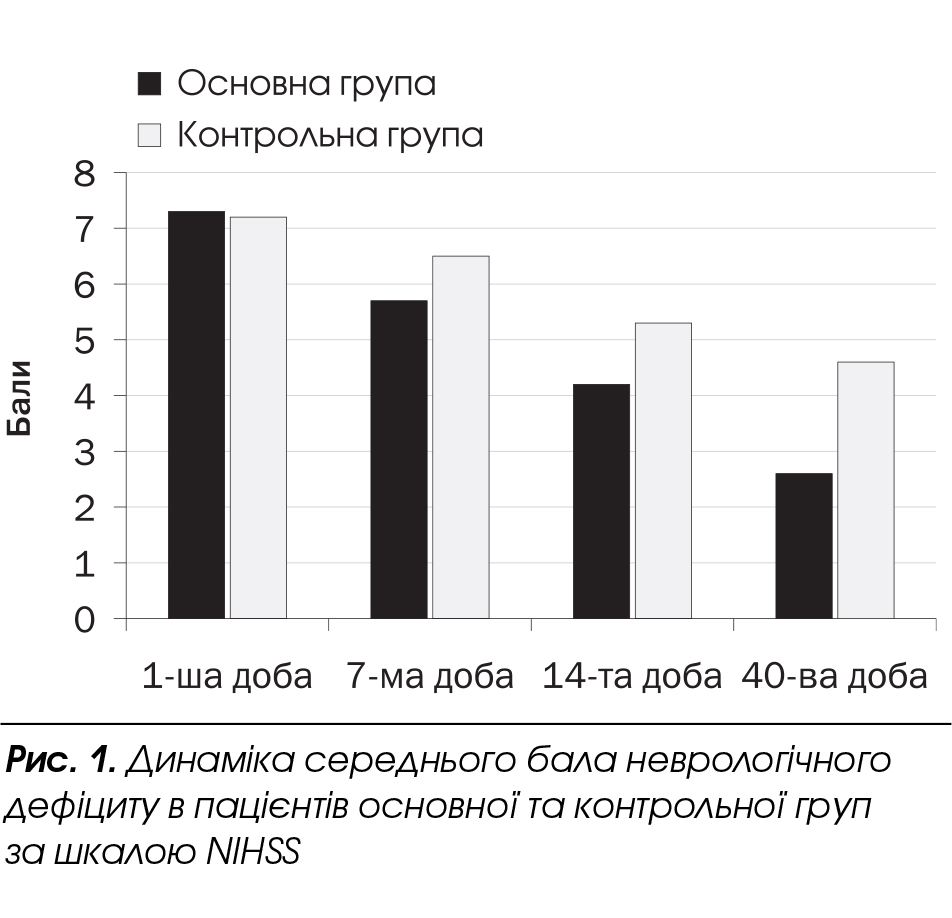
Динаміка відновлення неврологічних функцій була кращою у пацієнтів основної групи. Різниця середнього бала ставала достовірною, починаючи з 14-ї доби захворювання (р < 0,05). В основній групі на 40-ву добу лише в 1 (3,3 %) пацієнта спостерігали неврологічний дефіцит середнього ступеня вираженості, ще у 9 (30 %) — легкий неврологічний дефіцит, а у решти — мінімальні неврологічні розлади. В контрольній групі у більшості (9 (60 %)) пацієнтів на 40-ву добу захворювання зареєстровано легкі неврологічні розлади і лише в одного — мінімальний неврологічний дефіцит.
Застосування іпідакрину також продемонструвало позитивний вплив на ефективність реабілітаційних заходів. Так, досягнутий рівень повсякденної життєвої активності на 7-му добу захворювання за індексом Бартел у пацієнтів основної групи становив (69,5 ± 3,6) бала, а у пацієнтів контрольної групи — (67,5 ± 3,3) бала (р < 0,05), що в обох випадках відповідало помірній інвалідизації. Починаючи з 14-ї доби захворювання, встановлено нижчий рівень інвалідизації у пацієнтів основної групи ((82,8 ± 3,0) бала) порівняно з групою контролю ((77,5 ± 2,9) бала; р < 0,05). Подібну, але менш виражену тенденцію спостерігали на 40-ву добу спостереження — (88,0 ± 2,5) та (84,0 ± 2,3) бала відповідно (р > 0,05).
Існують дані щодо позитивного впливу іпідакрину на когнітивні функції хворих з мозковим інсультом [8], тому одним із завдань було проаналізувати динаміку відновлення когнітивного дефіциту у хворих. Вивчення когнітивних функцій ми розпочали на 7-му добу захворювання, після стабілізації стану пацієнтів. За шкалою ММ5Е середній бал у пацієнтів основної групи відповідав легкій постінсультній деменції ((21,8 ± 0,8) бала), схожі результати виявлено і в контрольній групі — (21,7 ± 1,3) бала. Дані щодо кількості випадків когнітивного дефіциту різного ступеня тяжкості наведено на рис. 2.
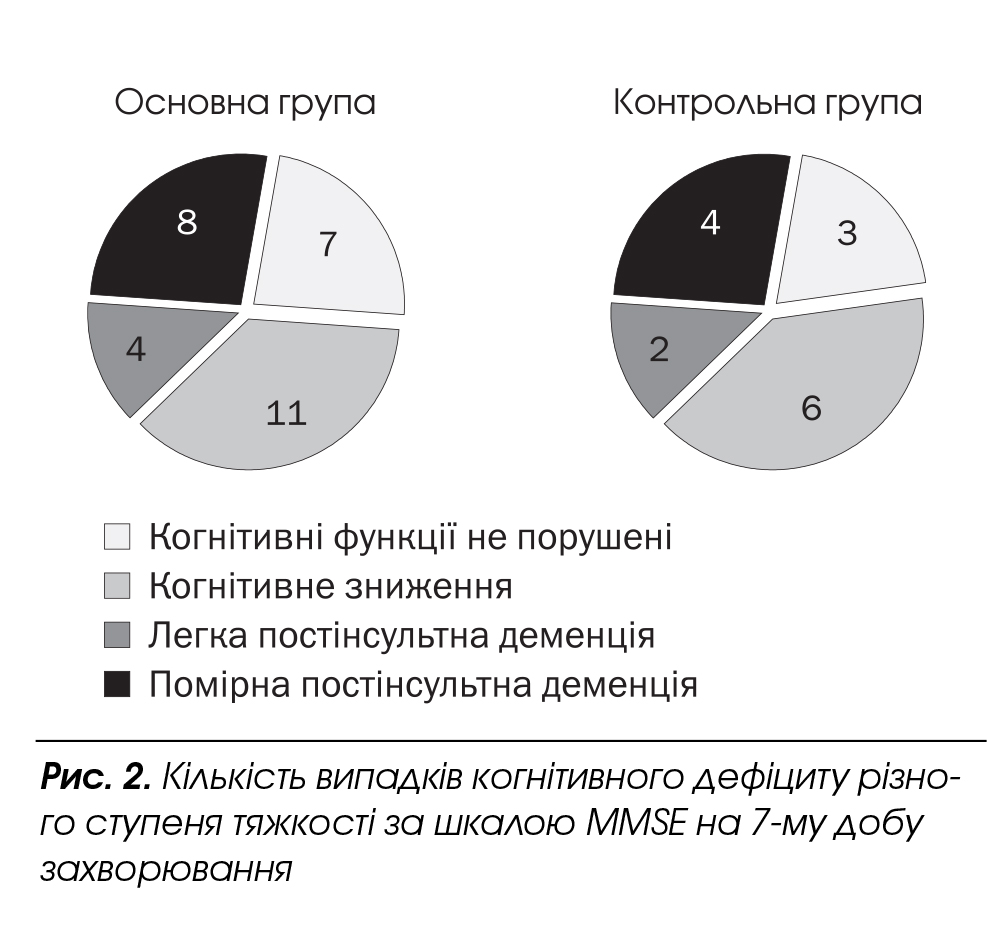
В обох групах частка пацієнтів з деменцією була майже такою, як частка пацієнтів з когнітивним зниженням, яке не досягало рівня деменції, а кожен п'ятий пацієнт продемонстрував задовільні когнітивні функції. Типовими порушеннями в обох групах були: порушення концентрації уваги — більшість пацієнтів розпочинали з правильних відповідей, однак у подальшому помилялися, використовуючи стереотипні відповіді, що є характерним для ураження лобних часток головного мозку [7, 8].
Дані щодо динаміки відновлення когнітивних функцій наведено на рис. 3.
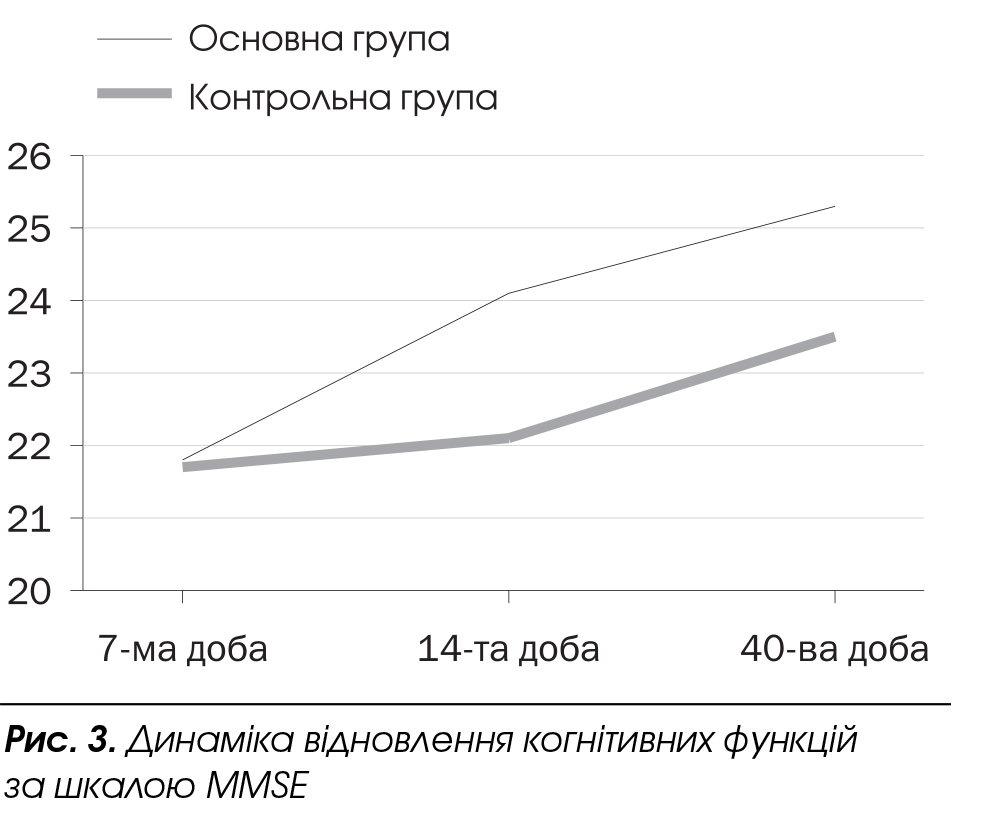
Достовірно кращу динаміку відновлення когнітивних функцій спостерігали на тлі терапії іпідакрином, яка була вираженішою на 14-ту добу захворювання: середній бал за шкалою ММ5Е в основній групі становив (24,13 ± 3,37) бала, а в групі контролю — (22,1 ± 4,17) бала (р < 0,05). Така динаміка зберігалася до кінця спостереження та була достовірно кращою на 40-ву добу ((25,3 ± 3,15) та (23,5 ± 2,5) бала відповідно (р < 0,05)), що, на нашу думку, пов'язано із здатністю препарату посилювати процеси репаративної нейропластичності.
При вивченні темпу сенсомоторних реакцій у пацієнтів контрольної групи за таблицями Шульте на 7-му добу захворювання встановлено їх сповільнення, про що свідчило збільшення часу, необхідного для виконання завдання, порівняно з нормативними значеннями. Середній час, витрачений на одну таблицю, становив (70,6 ± 28,5) с. Спостерігали неухильне зниження показників при заповненні всіх п'яти таблиць ((66,8 ± 23,7) с — час, витрачений на першу таблицю; (68,4 ± 25,9) с — на другу; (69,2 ± 27,8) с — на третю; (72,6 ± 29,2) с — на четверту; (75,8 ± 30,1) с — на п'яту таблицю). Виявлені зміни свідчать про виснаження сенсомоторних реакцій та сповільнення активної уваги хворих, які перенесли ішемічний інсульт.
Серед пацієнтів основної групи середній час виконання завдань за таблицями Шульте на 7-му добу захворювання був дещо кращим та становив (67,8 ± 27,4) с. Пацієнти витратили менше часу на першу таблицю (63,1 ± 26,9) с, однак у них також спостерігали зниження показників при заповненні решти таблиць ((65,3 ± 26,7) с — час, витрачений на другу таблицю; (69,0 ± 27,8) с — на третю таблицю; (67,8 ± 26,2) с — на четверту таблицю; (74,1 ± 32,2) с — на п'яту таблицю).
На 14-ту добу спостереження середній час виконання завдань за таблицями Шульте пацієнтами основної групи порівняно з 7-ю добою зменшився на 15,3 % ((57,4 ± 21,3) с), а у пацієнтів контрольної групи — лише на 9,2 % ((64,1 ± 19,3) с). Подібну тенденцію зареєстровано на 40-ву добу дослідження — показник основної групи поліпшився на 21,5 %, а контрольної — на 14,9 %. На нашу думку, ці результати свідчать про позитивний вплив застосування іпідакрину на рівень розумової працездатності та поліпшення активної уваги хворих.
Також ми дослідили частоту та ступінь вираження депресивних розладів у пацієнтів обох груп (таблиця).
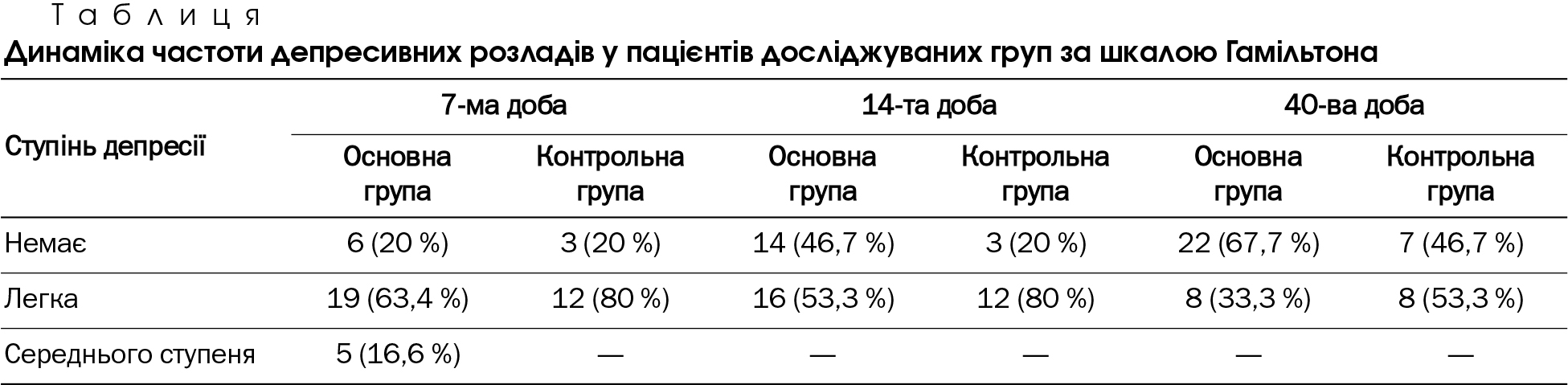
При порівнянні середнього бала за шкалою Гамільтона встановлено, що на 7-му добу захворювання у пацієнтів основної та контрольної груп він відповідав легкій депресії — (10,8 ± 5,3) та (10,7 ± 4,0) бала відповідно. Починаючи з 14-ї доби, зареєстровано достовірно кращі результати в основній групі — (8,3 ± 4,1) бала, тоді як у групі контролю — (13,1 ± 6,4) бала. Після завершення дослідження результати групи контролю дещо поліпшилися — (11,2 ± 5,3) бала, однак були достовірно гіршими порівняно з пацієнтами, схема лікування яких містила іпідакрин, — (6,7 ± 4,1) бала (р < 0,05). Таким чином, на тлі застосування іпідакрину спостерігається позитивна динаміка депресивних розладів, з поступовим відновленням позитивної емоційної сфери на відміну від групи контролю, в якій відзначено поглиблення депресивних симптомів на 14-ту добу спостереження, що, на нашу думку, пов'язано з гіршою динамікою усунення неврологічного дефіциту.
Ми також проаналізували взаємозв'язок депресивних та когнітивних розладів у досліджуваних групах. При проведенні кореляційного аналізу Пірсона встановлено тісний негативний кореляційний зв'язок між середнім балом за шкалою ММ5Е та балом за шкалою депресії Гамільтона у хворих контрольної групи (на 7-му добу г = -0,71, на 14-ту добу г = -0,84, на 40-ву — г = -0,57). Ці дані свідчать про те, що пацієнти зі зниженням когнітивних функцій мають високий ризик розвитку післяінсультної депресії. Подібного взаємозв'язку в пацієнтів основної групи не виявлено (на 7-му добу г = -0,14, на 14-ту — г = -0,17, на 40-ву — г = -0,3), що, на нашу думку, підтверджує позитивний вплив іпідакрину в гострий період інфаркту мозку на відновлення не лише рухового, а й когнітивного дефіциту, що сприяє повнішому та повноціннішому відновленню втрачених функцій, суттєво поліпшуючи реабілітацію цих хворих.
Висновки
Використання іпідакрину в комплексному лікуванні хворих на гострий ішемічний інсульт сприяє кращому відновленню втрачених неврологічних функцій, зниженню рівня інвалідизації та підвищенню ефективності реабілітаційних заходів. Також спостерігали позитивний вплив на психоемоційну сферу — поліпшення когнітивних функцій, зменшення частоти та ступеня вираження депресивних розладів, що сприяло функціональному відновленню пацієнтів.
Література
- Боголепова А.Н., Цуканова Е.И. Проблема нейропластичности в неврологии // Міжнар. неврол. журн.— 2010.— № 8 (38).— С. 69—72.
- Виленский Б.С. Инсульт — современное состояние проблеми // Неврол. журн.— 2008.— № 2.— С. 4—10.
- Волошин П.В., Мищенко Т.С. Профилактика мозгового инсульта // Здоров'я України.— 2002.— № 5.— С. 14—17.
- Гусев Е.И., Шимричек Г., Хаас А., Гехт А.Б. Результати 3-летнего катамнестического наблюдения за больньїми ишемическим інсультом // Неврол. журн.— 2002.— № 5.— С. 10—14.
- Коршняк В.О. Нейропластичність у хворих із наслідками закритих черепно-мозкових травм, терапевтичні можливості її активації // Междунар. неврол. журн.— 2011.— № 8 (46).— С. 61—64.
- Лаврецкая Э.Ф. «Нейромидин» (амиридин) — новьй тип лекарственньх препаратов — стимуляторов нервной и мьшечной систем.— К., 2002.— 39 с.
- Лурия А.Р. Основь нейропсихологии.— М.: Асасіетіа, 2003.— С. 168—175.
- Мищенко Т.С., Шестопалова Л.Ф., Мищенко В.Н. Нейромидин в терапии когнитивньх нарушений у постинсультньх больньх // Укр. вісн. психоневрол.— 2008.— № 3 (56).— Р. 12—15.
- Міщенко Т.С. Епідеміологія цереброваскулярних захворювань в Україні // Судинні захворювання головного мозку.— 2006.— № 1.— С. 3—7.
- Рябова В.С. Отдаленнье последствия мозгового инсульта // Журн. невропат. и психиатрии.— 1986.— № 4.— С. 532—536.
- Duncan P.W., Goldstein L.B., Matchar D. et al. Measurement of motor recovery after stroke: outcome assessment and sample size requirements // Stroke.— 1992.— Vol. 23.— P. 1084—1089.
- Gil Nunez A.C., Vivancos Mora J. Organization of medical care in acute stroke: importance of a good network // Cerebrovasc. Dis.— 2004.— Vol. 17 (suppl. 1).— P. 113—123.
- Hertz_Pannier L. Brain plasticity during development: physiological bases and functional MRI approach // J. Neuroradiol.— 1999.— Vol. 26.— P. 866—874.
- Kaste M., Forgelholm R., Rissanen A. Economic burden of stroke and the evaluation of new therapies // Public Health.— 1999.— Vol. 112.— P. 103—112.
- Page S.J., Levine P., Leonard A.C. Modified constraint_induced therapy in acute stroke: a randomized controlled pilot study // Neurorehabilitation Neural Repair.— 2005.— Vol. 19.— Р. 27—32.
Л. И. СОКОЛОВА, В. С. МЕЛЬНИК, В. Ю. ШАНДЮК, М. М. СЕПИХАНОВА, Г. М. ЛЕТОВАЛЬЦЕВА, О. В. КОСТОВЕЦКИЙ
СТИМУЛИРОВАНИЕ НЕЙРОПЛАСТИЧНОСТИ — ПЕРСПЕКТИВНОЕ НАПРАВЛЕНИЕ В ТЕРАПИИ ИШЕМИЧЕСКОГО ИНСУЛЬТА
Цель — изучить влияние ипидакрина у пациентов с острым ишемическим инсультом на динамику возобновления двигательных функций, достигнутый уровень двигательной активности, динамику изменений когнитивных функций и выраженность и распространенность постинсультной депрессии.
Материалы и методи. Проведено комплексное клинико-неврологическое обследование 45 пациентов (22 мужчин и 23 женщин) в острый период инфаркта мозга полушарной локализации. Средний возраст пациентов — (66,7 ± 1,4) года. Пациенты были разделены на две группы. Основную составили 30 больных (средний возраст — (66,8 ± 1,3) года), которые на фоне традиционной терапии получали в течение 1—5 суток заболевания ипидакрин 0,5 % в дозе 1,0 мл внутримышечно один раз в сутки, в следующие 6—10 суток — ипидакрин 1,5 % в дозе 1,0 мл внутримышечно один раз в сутки, в период с 11-х до 40-х суток—таблетированную форму ипидакрина (20 мг) трижды в сутки. В контрольную группу вошли 15 больных (7 мужчин и 8 женщин), которые по демографическим показателям были сопоставимы с пациентами основной группы и получали традиционную терапию ишемического инсульта. Программа обследования предусматривала использование шкал NN33 и ММ5Е, таблиц Шульте, шкалы Гамильтона и индекса Бартел.
Результаты. Выявлена лучшая динамика возобновления неврологических функций (по шкале NIН55) у пациентов основной группы, а разница среднего балла относительно группы контроля становилась достоверной, начиная с 14-х суток заболевания (р < 0,05). Также, начиная с 14-х суток заболевания, установлен более низкий уровень инвалидизации у пациентов основной группы ((82,8 ± 3,0) балла) по сравнению с группой контроля ((77,5 ± 2,9) балла; р < 0,05) по индексу Бартел. Достоверно лучшую динамику возобновления когнитивных функций наблюдали на фоне терапии ипидакрином, достоверные различия фиксировали, начиная с 14-х суток заболевания. На фоне применения ипидакрина отмечена позитивная динамика депрессивных расстройств, с постепенным восстановлением позитивной эмоциональной сферы в отличие от группы контроля, в которой наблюдали углубление депрессивных симптомов на 14-е сутки, что, по нашему мнению, связано с худшей динамикой устранения неврологического дефицита.
Выводы. Использование ипидакрина в комплексном лечении больных с острым ишемическим инсультом способствует лучшему восстановлению неврологических функций, снижению уровня инвалидизации и повышению эффективности реабилитационных мероприятий. Выявлено также позитивное влияние на психоэмоциональную сферу — улучшение когнитивных функций, уменьшение частоты и выраженности депрессивных расстройств, что способствуют функциональному восстановлению пациентов.
Ключевые слова: ишемический инсульт, ипидакрин, восстановление неврологических функций.
L.I. SOKOLOVA, V.S. MELNYK, V.Yu. SHANDIUK, M.M. SEPYKHANOVA, G.M. LETOVALTSEVA, O.V. KOSTOVETSKII
NEUROFLEXIBILITY STIMULATION AS A PERSPECTIVE METHOD OF ISCHEMIC STROKE THERAPY
Objective – to study the іpidacrinum impact on motor functions recovery level in patients with IS, their motor activity level, cognitive functions changes dynamic and intensity and prevalence of post stroke depression.
Methods and subjects. 45 patients (22 males and 23 females) underwent the clinical and neurological examination at the period of acute IS of hemispheric localization. Mean age constituted (66.7 ± 1.4) ages. Patients were divided into two groups. The main group consisted of 30 patients (mean age 66.8 ± 1.3) who were treated with daily intramuscular іpidacrinum 0.5 % – 1.0 ml during 1–5 days against the background of traditional therapy, the following 6–10 days the dosage was 1.5 % – 1.0 ml daily, the following 11–40 days іpidacrinum pills (20 mg) three times a day. The control group consisted of 15 patients (7 males and 8 females) who underwent the traditional therapy. The examination included the application of NIHSS и MMSE scales, Shulte tables, Hamilton’s scale and Bartel’s index.
Results. Better dynamic of neurological functions (NIHSS scale) was evidenced in patients from the main group, the difference of the average index concerning the control group was reliable from the 14th days of disease (р < 0.05). The rate of disability in patients from the main group decreased on the 14th days ((82.8 ± 3.0) points) comparing to the control group ((77.5 ± 2.9) points, Bartel’s index р < 0.05). Better dynamic of cognitive functional recovery was evidenced against the background of іpidacrinum therapy, reliable differences were marked on the 14th days following the diseases. The positive depression dynamic was also noted against the background of іpidacrinum therapy, with gradual positive emotional status comparing to control group, where patients demonstrated the worsening of depression on the 14th days. It evidences the worse dynamic of neurological deficit elimination.
Conclusions. Better neurological functions recovery, disability level reduction and positive effect of rehabilitation indicate the efficacy of іpidacrinum therapy. It also positively influence the emotional status of patients: cognitive functional improvement, reduction of prevalence and intensity of depression that impacts positively the patients recovery.
Key words: ischemic stroke, іpidacrinum, neurological functional recovery.
Стаття надійшла до редакції 29 листопада 2012 р.

