УКРАЇНСЬКИЙ ВІСНИК ПСИХОНЕВРОЛОГІЇ – ТОМ 14, ВИП. 1 (46) – 2006
И. Н. Карабань1, Е. П. Луханина2, Н. А. Мельник1, Н. М. Березецкая3
1 Институт геронтологии АМН Украины,
2 Институт физиологии им. А. А. Богомольца НАН Украины,
3 Институт физики НАН Украины (г. Киев)
Болезнь Паркинсона (БП) – хроническое прогрессирующее нейродегенеративное заболевание ЦНС, ведущими клиническими симптомами которого являются нарушения двигательной активности (акинезия, ригидность, тремор), к которым впоследствии присоединяются постуральные, когнитивные, психоэмоциональные и вегетативные расстройства.
Распространенность БП по данным мировой статистики составляет 60–187 случаев, а в Украине – 133 на 100 тыс. населения [1,2].
Согласно современным данным БП считают болезнью нейромедиаторного обмена [3, 4]. Специфической биохимической особенностью заболевания является недостаточность продукции дофамина (ДА) в базальных ганглиях и развитие дофадефицитарного дисбаланса в нигростриатной системе головного мозга.
К облигатным симптомам паркинсонизма относят и депрессивные расстройства, которые выявляются у 40–90 %, а изменения настроения – приблизительно у 40–50 % больных. Депрессия обычно возникает в самом начале болезни, предшествуя появлению двигательных нарушений [5] и проявляется в дисфории и грусти, гипертрофированном чувстве собственной вины перед близкими людьми [6].
Когнитивные нарушении считаются вторым по частоте коморбидным состоянием при БП. По данным некоторых авторов [7], риск развития деменции у пациентов с БП в 6 раз выше, чем в соответствующей возрастной группе людей, не страдающих этим заболеванием. При этом вероятность развития деменции с возрастом резко увеличивается.
Уже на ранних стадиях заболевания у большинства пациентов находят нарушения памяти, снижение быстроты планирования действий, а на поздних — возрастает частота дементных нарушений – от 40 % до 80 % [8]. Недостаточность когнитивных функций оказывает существенное влияние на выраженность двигательных нарушений, степень инвалидизации больных, их социальную адаптацию, поэтому применение ноотропных препаратов, улучшающих интеллектуально-мнестические способности, оказывает потенцирующее влияние на эффективность базисной патогенетической терапии.
В ряду ноотропных препаратов достойное место занимают препараты γ-аминомасляной кислоты, и в частности НООФЕН. Спектр клинической эффективности ноофена достаточно широк, поскольку этот препарат сочетает ноотропное и транквилизирующее действие. Ноофен улучшает память, интеллектуальную активность, повышает устойчивость мозга к вредным воздействиям, обладает противосудорожными, седативными свойствами, а также оказывает стабилизирующее действие на вегетативные функции. У лиц пожилого и старческого возраста, особенно на фоне дисциркуляторной энцефалопатии и других проявлений сосудистой патологии, ноофен эффективно влияет на частоту и выраженность симптомов ажитации, страха, тревоги, психомоторного возбуждения; у больных появляется более адекватное отношение к себе и окружающим, повышается уровень интереса к жизни, улучшается сон [10].
Основное ноотропное действие препарата основано на антигипоксическом действии, повышении энергетических ресурсов, активации метаболических процессов, улучшении функциональных особенностей нейронов [9–11]. Ноофен нормализует соотношение аэробных и анаэробных процессов, способствует повышению уровня глюкозы в крови и тканях мозга, увеличивает содержание макроэргических фосфатов в структурах ЦНС [12–13].
Благодаря взаимодействию между ГАМК- и дофаминергической нейромедиаторными системами, особенно в стриатуме, ноофен стимулирует дофаминергические процессы и, что особенно важно с практической точки зрения, усиливает действие противопаркинсонических препаратов [14].
Следует полагать, что Ноофен является патогенетически значимым при дофаминергической недостаточности, свойственной паркинсонизму.
Целью настоящего исследования было оценить эффективность курсового применения ноофена, производства Olain Farm (Латвия) у больных БП на фоне базисной терапии заболевания для улучшения двигательной активности, когнитивных функций и психоэмоционального состояния пациентов.
Было обследовано до и после курсового применения ноофена 25 больных БП (12 мужчин и 13 женщин) в возрасте 51–75 лет, средний возраст 61,5 ± 1,3 лет со стадией заболевания 1,5–3,0 (по Hoehn a. Yahr). Средняя продолжительность болезни составляла 4,87 ± 2,72 лет (табл. 1).
Базисная терапия у больных БП оставалась неизменной в течение 1 месяца до начала курсового приема ноофена и на протяжении всего курса приема препарата.
Курсовое лечение ноофеном было про ведено в условиях стационара Центра пар кинсонизма Института геронтологии в режиме дозирования – 1 таблетка (250 мг) препарата 3 раза в день (750 мг/сутки), в течение 21 дня.
Для объективного исследования двигательной активности мы использовали: унифицированную международную рейтинговую шкалу оценки двигательной активности (Unified Parkinson’s Disease Rating Scale – UPDRS), компьютеризированную электромиографию (ЭМГ), время (латентный период) сенсомоторной реакции и моторный темп.
Таблица 1
Характеристика обследованных больных
|
Количество пациентов |
25 |
|
мужчин |
12 |
|
женщин |
13 |
|
Средний возраст пациентов, лет |
61,5 ± 1,3 |
|
минимальный |
49 |
|
максимальный |
75 |
|
Продолжительность болезни, лет |
4,87 ± 2,72 |
|
минимальная |
0,3 |
|
максимальная |
15 |
|
Стадия по Hoehn a. Yahr |
1,5–3,0 |
|
стадия 1,5 |
1 |
|
стадия 2,0 |
13 |
|
стадия 2,5 |
7 |
|
стадия 3,0 |
4 |
|
Количество больных на долеводопном этапе |
14 |
|
Количество больных, принимающих леводопу |
11 |
|
Средняя доза леводопы, мг |
306,86 |
ЭМГ покоя использовалась для оценки способности к расслаблению мышечного напряжения. Регистрировали поверхностную ЭМГ сгибателей и разгибателей предплечья правой и левой рук – двуглавой (biceps brachii) и трехглавой (triceps brachii) мышц плеча. Для отведения ЭМГ использовали биполярные накожные электроды с постоянным межэлектродным расстоянием 1,5 см. Биоэлектрические сигналы подавали по 4 каналам на усилители электромиографа «Медикор» MG 440 с полосой пропускания 2 Гц – 10 кГц. Анализ ЭМГ проводили с помощью специализированной компьютерной программы.
Моторный темп определялся также посредством компьютерной программы как время между последовательными нажатиями одним и тем же пальцем двух клавиш, разнесенных на клавиатуре на расстояние 20 см. Больному давалась инструкция нажимать клавиши в максимально быстром темпе. Продолжительность каждого теста составляла 20 секунд. Тестирование проводилось для каждой руки отдельно, затем данные усреднялись.
Время простой сенсомоторной реакции определялось как интервал между моментом предъявления зрительного сигнала на мониторе компьютера и моментом нажатия пациентом клавиши в ответ на сигнал. В качестве сигнала использовались геометрические фигуры (круг, квадрат, овал) красного и белого цвета, 20 сигналов предъявлялись с интервалом 2–4 с. Тестирование проводилось для каждой руки отдельно, данные усреднялись.
Мнестические функции оценивали при помощи шкалы Mini Mental State Examination (MMSE). Суммарная оценка этой шкалы в норме соответствует 30 баллам. Снижение общего оценочного бала ниже 25 свидетельствует о начальных признаках деменции.
Для определения объема кратковременной и отсроченной памяти использовали тест запоминания 10 слов, методика которого предложена А. Р. Лурия [15]. Больному устно предъявляли 10 слов, не связанных между собой, и давали инструкцию запомнить их в любой последовательности. Список предъявляли 6 раз. После каждого предъявления проверяли воспроизведение слов. Исследовали 2 вида воспроизведения: непосредственное (сразу после предъявления) и отсроченное (через 30 минут после предъявления, причем в это время больной выполнял другие задания). Результатом являлось количество воспроизводимых слов. Для обследования до и после приема ноофена существовали разные списки, слова в которых не повторялись.
К изменениям, характерным для БП, относят также депрессию и тревожность. Поэтому психоэмоциональное состояние исследовали при помощи шкалы депрессии Бека и шкалы тревожности Спилбергера.
Шкала депрессии Бека заполняется больным самостоятельно. Максимальный балл по шкале соответствует 63, минимальный – нулю, в соответствии с улучшением состояния балл снижается.
Шкала тревожности Спилбергера давала возможность различать два типа тревоги – тревожность как черту личности (конституциональная, личностная тревожность, ЛТ) и тревогу как преходящее клиническое состояние (ситуационная тревожность, СТ).
Двигательная активность. В результате лечения ноофеном на фоне базисной патогенетической терапии выявлено некоторое улучшение общей неврологической симптоматики (табл. 2). У одних больных положительный эффект препарата больше проявлялся в виде улучшения мышления, поведения, настроения или повышения активности в повседневной жизни, у других – в виде уменьшения проявлений акинетико-ригидного синдрома, что соответствовало уменьшению баллов по I, II или III частям UPDRS. В результате усредненный суммарный балл шкалы по всей группе больных снизился с 51,58 ± 2,70 до 48,54 ± 2,83 балла (p < 0,001). С высокой степенью достоверности уменьшились интеллектуальные нарушения, депрессия, расстройства поведения, мышления (І часть UPDRS) – с 2,44 ± 0,44 балла до 1,34 ± 0,30 балла (p < 0,001). У 65 % обследуемых больных наблюдалось также улучшение походки, осанки, моторного темпа, уменьшение тремора или скованности, что вызвало снижение моторного балла (ІІІ часть шкалы) с 37,00 ± 1,99 до 35,86 ± 1,99 (p < 0,01).
Таблица 2
Изменение баллов по шкале UPDRS у больных болезнью Паркинсона в результате курсового применения Ноофена
|
До лечения Ноофеном |
После лечения Ноофеном |
|
|
Суммарный балл шкалы UPDRS |
UPDRS 51,58 ± 2,70 |
48,54 ± 2,83** |
|
I часть UPDRS (мнестические функции) |
2,44 ± 0,44 |
1,34 ± 0,30** |
|
II часть UPDRS (дневная активность) |
12,34 ± 0,75 |
11,70 ± 0,77 |
|
III часть UPDRS (двигательная активность) |
37,00 ± 1,99 |
35,86 ± 1,99* |
* – p < 0,01; ** – p < 0,001
Курсовое применение ноофена оказало благоприятное влияние на способность мышц к расслаблению у 72 % обследованных больных. Это выражалось в уменьшении амплитуды ЭМГ покоя, особенно заметное на более пораженной стороне. Средняя амплитуда ЭМГ по коя в данной группе больных на стороне большего поражения достоверно снизилась с 15,5 ± 3,0 до 9,3 ± 1,7 мкВ (p < 0,05), а максимальная амплитуда – с 79,4 ± 20,6 до 39,5 ± 10,9 мкВ для m. biceps brachii. Для m. triceps brachii значение средней и максимальной амплитуд также уменьшились, хотя и статистически недостоверно: соответственно с 10,5 ± 2,1 до 8,4 ± 1,2 мкВ и с 42,4 ± 12,7 до 31,1 ± 7,7 мкВ (табл. 3).
Таблица 3
Влияние курсового лечения Ноофеном на показатели биоэлектрической активности мышц по данным ЭМГ покоя
|
ЭМГ-показатели, мкВ |
До лечения ноофеном |
После лечения ноофеном |
|
Ср. ампл. m. biceps brachii |
15,5 ± 3,0 |
9,3 ± 1,7 |
|
Ср. ампл. m. triceps brachii |
10, 5 ± 2,1 |
8,4 ± 1,2 |
|
Макс. ампл. m. biceps brachii |
79,4 ± 20,6 |
39,5 ± 10,9 |
|
Макс. ампл. m. triceps brachii |
42,4 ± 12,7 |
31,1 ± 7,7 |
Прием Ноофена оказывал также положительное терапевтическое воздействие на характерную для больных «залповую» мышечную активность, имеющую частоту тремора 4–6 Гц. До курса ноофена она регистрировалась в 52 % всех записей. После лечения ноофеном количество случаев регистрации залповых мышечных разрядов уменьшилось до 38 % (p < 0,05).
Время сенсомоторной реакции, усредненное для обеих рук, в результате курсового лечения ноофеном сократилось с 394,5 ± 26,2 до 316,8 ± 7,1 мс (p < 0,01). Моторный темп после курсового лечения ноофеном существенно повысился, а именно: время между двумя последовательными нажатиями клавиш, усредненное для обеих рук, уменьшилось с 589,9 ± 25,9 до 522,4 ± 21,6 мс (p < 0,001; табл. 4).
Таблица 4
Влияние курсового лечения ноофеном на показатели сенсомоторной реакции и моторного темпа у больных БП
|
Показатели, мс |
До лечения ноофеном |
После лечения ноофеном |
|
Моторный темп (интервал между нажатием клавиш) |
589,9 ± 25,9 |
522,4 ± 21,6** |
|
Время сенсомоторной реакции |
394,5 ± 26,2 |
316,8 ± 7,1* |
* – p < 0,01; ** – p < 0,001
Состояние мнестических функций. Результаты настоящего исследования показали, что ноофен обладает выраженным ноотропным эффектом. Это подтверждается высокодостоверным улучшением показателей по шкале MMSE и тестом запоминания 10 слов Лурия (табл. 5). Суммарный балл по шкале MMSE после лечения повысился с 26,92 ± 0,48 до 29,44 ± 0,18 балла (p < 0,001). Рост суммарного балла после приема ноофена по шкале MMSE был обусловлен повышением показателей в частях шкалы, определяющих память и внимание.
Таблица 5
Динамика когнитивных функций у больных болезнью Паркинсона в результате курсового применения ноофена
|
Показатели |
До лечения ноофеном |
После лечения ноофеном |
|
Суммарный балл шкалы MMSE |
26,92 ± 0,48 |
29,44 ± 0,18* |
|
Память по шкале MMSE |
1,68 ± 0,18 |
2,56 ± 0,12* |
|
Внимание по шкале MMSE |
4,16 ± 0,20 |
4,96 ± 0,04* |
|
Суммарный балл теста Лурия |
35,92 ± 1,30 |
41,64 ± 0,97* |
|
Первый ответ по тесту Лурия |
5,12 ± 0,36 |
6,92 ± 0,33* |
|
Отсроченный ответ по тесту Лурия |
5,56 ± 0,49 |
7,28 ± 0,37* |
* – p < 0,001
Еще более выраженный эффект после приема ноофена был установлен при проведении теста Лурия на запоминание 10 слов. Суммарный балл этого теста увеличился с 35,92 ± 1,30 до 41,64 ± 0,97 (p < 0,001). Улучшилась как кратковременная так и долговременная память.
Оценка психоэмоционального статуса (депрессия, тревожность). После курса приема ноофена у больных отмечалось заметное улучшение психоэмоционального состояния (табл. 6). Уменьшилась степень депрессии – средние баллы по шкале Бека до и после лечения составили 17,65 ± 1,88 и 14,76 ± 1,92 (p < 0,05). Также уменьшилась тревожность, как ЛТ, так и СТ. С достоверностью p < 0,01 изменилась СТ – с 52,96 ± 1,59 балла до 47,54 ± 2,06 балла после приема Ноофена. ЛТ, которая считается более валидной частью шкалы, уменьшилась с 54,83 ± 1,70 балла до 49,33 ± 2,11 балла при ещё более высокой степени достоверности (p < 0,001).
Таблица 6
Улучшение психоэмоционального статуса больных болезнью Паркинсона в результате курсового применения ноофена
|
Показатели |
До лечения ноофеном |
После лечения ноофеном |
|
Балл по шкале Бека |
17,65 ± 1,88 |
14,76 ± 1,92* |
|
Балл по шкале Спилбергера, СТ |
52,96 ± 1,59 |
47,54 ± 2,06** |
|
Балл по шкале Спилбергера, ЛТ |
54,83 ± 1,70 |
49,33 ± 2,11*** |
– p < 0,05; ** – p < 0,01; *** – p < 0,001;
На фоне приема Ноофена мы также отмечали уменьшение болевого синдрома (не связанного с БП), нормализацию сна, настроения, уменьшение головокружения, метеозависимости, повышался уровень интереса к жизни, работоспособность, появлялось более адекватное отношение к себе и к своему заболеванию.
Итогом проведенных исследований эффективности курсового лечения ноофеном у больных БП явился анализ динамики отдельных клинико-физиологических показателей относительно исходного уровня (см. рис.).
Болезнь Паркинсона (БП) – хроническое прогрессирующее нейродегенеративное заболевание ЦНС, ведущими клиническими симптомами которого являются нарушения двигательной активности (акинезия, ригидность, тремор), к которым впоследствии присоединяются постуральные, когнитивные, психоэмоциональные и вегетативные расстройства.
Распространенность БП по данным мировой статистики составляет 60–187 случаев, а в Украине – 133 на 100 тыс. населения [1,2].
Согласно современным данным БП считают болезнью нейромедиаторного обмена [3, 4]. Специфической биохимической особенностью заболевания является недостаточность продукции дофамина (ДА) в базальных ганглиях и развитие дофадефицитарного дисбаланса в нигростриатной системе головного мозга.
К облигатным симптомам паркинсонизма относят и депрессивные расстройства, которые выявляются у 40–90 %, а изменения настроения – приблизительно у 40–50 % больных. Депрессия обычно возникает в самом начале болезни, предшествуя появлению двигательных нарушений [5] и проявляется в дисфории и грусти, гипертрофированном чувстве собственной вины перед близкими людьми [6].
Когнитивные нарушении считаются вторым по частоте коморбидным состоянием при БП. По данным некоторых авторов [7], риск развития деменции у пациентов с БП в 6 раз выше, чем в соответствующей возрастной группе людей, не страдающих этим заболеванием. При этом вероятность развития деменции с возрастом резко увеличивается.
Уже на ранних стадиях заболевания у большинства пациентов находят нарушения памяти, снижение быстроты планирования действий, а на поздних — возрастает частота дементных нарушений – от 40 % до 80 % [8]. Недостаточность когнитивных функций оказывает существенное влияние на выраженность двигательных нарушений, степень инвалидизации больных, их социальную адаптацию, поэтому применение ноотропных препаратов, улучшающих интеллектуально-мнестические способности, оказывает потенцирующее влияние на эффективность базисной патогенетической терапии.
В ряду ноотропных препаратов достойное место занимают препараты γ-аминомасляной кислоты, и в частности НООФЕН. Спектр клинической эффективности ноофена достаточно широк, поскольку этот препарат сочетает ноотропное и транквилизирующее действие. Ноофен улучшает память, интеллектуальную активность, повышает устойчивость мозга к вредным воздействиям, обладает противосудорожными, седативными свойствами, а также оказывает стабилизирующее действие на вегетативные функции. У лиц пожилого и старческого возраста, особенно на фоне дисциркуляторной энцефалопатии и других проявлений сосудистой патологии, ноофен эффективно влияет на частоту и выраженность симптомов ажитации, страха, тревоги, психомоторного возбуждения; у больных появляется более адекватное отношение к себе и окружающим, повышается уровень интереса к жизни, улучшается сон [10].
Основное ноотропное действие препарата основано на антигипоксическом действии, повышении энергетических ресурсов, активации метаболических процессов, улучшении функциональных особенностей нейронов [9–11]. Ноофен нормализует соотношение аэробных и анаэробных процессов, способствует повышению уровня глюкозы в крови и тканях мозга, увеличивает содержание макроэргических фосфатов в структурах ЦНС [12–13].
Благодаря взаимодействию между ГАМК- и дофаминергической нейромедиаторными системами, особенно в стриатуме, ноофен стимулирует дофаминергические процессы и, что особенно важно с практической точки зрения, усиливает действие противопаркинсонических препаратов [14].
Следует полагать, что Ноофен является патогенетически значимым при дофаминергической недостаточности, свойственной паркинсонизму.
Целью настоящего исследования было оценить эффективность курсового применения ноофена, производства Olain Farm (Латвия) у больных БП на фоне базисной терапии заболевания для улучшения двигательной активности, когнитивных функций и психоэмоционального состояния пациентов.
Было обследовано до и после курсового применения ноофена 25 больных БП (12 мужчин и 13 женщин) в возрасте 51–75 лет, средний возраст 61,5 ± 1,3 лет со стадией заболевания 1,5–3,0 (по Hoehn a. Yahr). Средняя продолжительность болезни составляла 4,87 ± 2,72 лет (табл. 1).
Базисная терапия у больных БП оставалась неизменной в течение 1 месяца до начала курсового приема ноофена и на протяжении всего курса приема препарата.
Курсовое лечение ноофеном было про ведено в условиях стационара Центра пар кинсонизма Института геронтологии в режиме дозирования – 1 таблетка (250 мг) препарата 3 раза в день (750 мг/сутки), в течение 21 дня.
Для объективного исследования двигательной активности мы использовали: унифицированную международную рейтинговую шкалу оценки двигательной активности (Unified Parkinson’s Disease Rating Scale – UPDRS), компьютеризированную электромиографию (ЭМГ), время (латентный период) сенсомоторной реакции и моторный темп.
Таблица 1
Характеристика обследованных больных
|
Количество пациентов |
25 |
|
мужчин |
12 |
|
женщин |
13 |
|
Средний возраст пациентов, лет |
61,5 ± 1,3 |
|
минимальный |
49 |
|
максимальный |
75 |
|
Продолжительность болезни, лет |
4,87 ± 2,72 |
|
минимальная |
0,3 |
|
максимальная |
15 |
|
Стадия по Hoehn a. Yahr |
1,5–3,0 |
|
стадия 1,5 |
1 |
|
стадия 2,0 |
13 |
|
стадия 2,5 |
7 |
|
стадия 3,0 |
4 |
|
Количество больных на долеводопном этапе |
14 |
|
Количество больных, принимающих леводопу |
11 |
|
Средняя доза леводопы, мг |
306,86 |
ЭМГ покоя использовалась для оценки способности к расслаблению мышечного напряжения. Регистрировали поверхностную ЭМГ сгибателей и разгибателей предплечья правой и левой рук – двуглавой (biceps brachii) и трехглавой (triceps brachii) мышц плеча. Для отведения ЭМГ использовали биполярные накожные электроды с постоянным межэлектродным расстоянием 1,5 см. Биоэлектрические сигналы подавали по 4 каналам на усилители электромиографа «Медикор» MG 440 с полосой пропускания 2 Гц – 10 кГц. Анализ ЭМГ проводили с помощью специализированной компьютерной программы.
Моторный темп определялся также посредством компьютерной программы как время между последовательными нажатиями одним и тем же пальцем двух клавиш, разнесенных на клавиатуре на расстояние 20 см. Больному давалась инструкция нажимать клавиши в максимально быстром темпе. Продолжительность каждого теста составляла 20 секунд. Тестирование проводилось для каждой руки отдельно, затем данные усреднялись.
Время простой сенсомоторной реакции определялось как интервал между моментом предъявления зрительного сигнала на мониторе компьютера и моментом нажатия пациентом клавиши в ответ на сигнал. В качестве сигнала использовались геометрические фигуры (круг, квадрат, овал) красного и белого цвета, 20 сигналов предъявлялись с интервалом 2–4 с. Тестирование проводилось для каждой руки отдельно, данные усреднялись.
Мнестические функции оценивали при помощи шкалы Mini Mental State Examination (MMSE). Суммарная оценка этой шкалы в норме соответствует 30 баллам. Снижение общего оценочного бала ниже 25 свидетельствует о начальных признаках деменции.
Для определения объема кратковременной и отсроченной памяти использовали тест запоминания 10 слов, методика которого предложена А. Р. Лурия [15]. Больному устно предъявляли 10 слов, не связанных между собой, и давали инструкцию запомнить их в любой последовательности. Список предъявляли 6 раз. После каждого предъявления проверяли воспроизведение слов. Исследовали 2 вида воспроизведения: непосредственное (сразу после предъявления) и отсроченное (через 30 минут после предъявления, причем в это время больной выполнял другие задания). Результатом являлось количество воспроизводимых слов. Для обследования до и после приема ноофена существовали разные списки, слова в которых не повторялись.
К изменениям, характерным для БП, относят также депрессию и тревожность. Поэтому психоэмоциональное состояние исследовали при помощи шкалы депрессии Бека и шкалы тревожности Спилбергера.
Шкала депрессии Бека заполняется больным самостоятельно. Максимальный балл по шкале соответствует 63, минимальный – нулю, в соответствии с улучшением состояния балл снижается.
Шкала тревожности Спилбергера давала возможность различать два типа тревоги – тревожность как черту личности (конституциональная, личностная тревожность, ЛТ) и тревогу как преходящее клиническое состояние (ситуационная тревожность, СТ).
Двигательная активность. В результате лечения ноофеном на фоне базисной патогенетической терапии выявлено некоторое улучшение общей неврологической симптоматики (табл. 2). У одних больных положительный эффект препарата больше проявлялся в виде улучшения мышления, поведения, настроения или повышения активности в повседневной жизни, у других – в виде уменьшения проявлений акинетико-ригидного синдрома, что соответствовало уменьшению баллов по I, II или III частям UPDRS. В результате усредненный суммарный балл шкалы по всей группе больных снизился с 51,58 ± 2,70 до 48,54 ± 2,83 балла (p < 0,001). С высокой степенью достоверности уменьшились интеллектуальные нарушения, депрессия, расстройства поведения, мышления (І часть UPDRS) – с 2,44 ± 0,44 балла до 1,34 ± 0,30 балла (p < 0,001). У 65 % обследуемых больных наблюдалось также улучшение походки, осанки, моторного темпа, уменьшение тремора или скованности, что вызвало снижение моторного балла (ІІІ часть шкалы) с 37,00 ± 1,99 до 35,86 ± 1,99 (p < 0,01).
Таблица 2
Изменение баллов по шкале UPDRS у больных болезнью Паркинсона в результате курсового применения Ноофена
|
До лечения Ноофеном |
После лечения Ноофеном |
|
|
Суммарный балл шкалы UPDRS |
UPDRS 51,58 ± 2,70 |
48,54 ± 2,83** |
|
I часть UPDRS (мнестические функции) |
2,44 ± 0,44 |
1,34 ± 0,30** |
|
II часть UPDRS (дневная активность) |
12,34 ± 0,75 |
11,70 ± 0,77 |
|
III часть UPDRS (двигательная активность) |
37,00 ± 1,99 |
35,86 ± 1,99* |
* – p < 0,01; ** – p < 0,001
Курсовое применение ноофена оказало благоприятное влияние на способность мышц к расслаблению у 72 % обследованных больных. Это выражалось в уменьшении амплитуды ЭМГ покоя, особенно заметное на более пораженной стороне. Средняя амплитуда ЭМГ по коя в данной группе больных на стороне большего поражения достоверно снизилась с 15,5 ± 3,0 до 9,3 ± 1,7 мкВ (p < 0,05), а максимальная амплитуда – с 79,4 ± 20,6 до 39,5 ± 10,9 мкВ для m. biceps brachii. Для m. triceps brachii значение средней и максимальной амплитуд также уменьшились, хотя и статистически недостоверно: соответственно с 10,5 ± 2,1 до 8,4 ± 1,2 мкВ и с 42,4 ± 12,7 до 31,1 ± 7,7 мкВ (табл. 3).
Таблица 3
Влияние курсового лечения Ноофеном на показатели биоэлектрической активности мышц по данным ЭМГ покоя
|
ЭМГ-показатели, мкВ |
До лечения ноофеном |
После лечения ноофеном |
|
Ср. ампл. m. biceps brachii |
15,5 ± 3,0 |
9,3 ± 1,7 |
|
Ср. ампл. m. triceps brachii |
10, 5 ± 2,1 |
8,4 ± 1,2 |
|
Макс. ампл. m. biceps brachii |
79,4 ± 20,6 |
39,5 ± 10,9 |
|
Макс. ампл. m. triceps brachii |
42,4 ± 12,7 |
31,1 ± 7,7 |
Прием Ноофена оказывал также положительное терапевтическое воздействие на характерную для больных «залповую» мышечную активность, имеющую частоту тремора 4–6 Гц. До курса ноофена она регистрировалась в 52 % всех записей. После лечения ноофеном количество случаев регистрации залповых мышечных разрядов уменьшилось до 38 % (p < 0,05).
Время сенсомоторной реакции, усредненное для обеих рук, в результате курсового лечения ноофеном сократилось с 394,5 ± 26,2 до 316,8 ± 7,1 мс (p < 0,01). Моторный темп после курсового лечения ноофеном существенно повысился, а именно: время между двумя последовательными нажатиями клавиш, усредненное для обеих рук, уменьшилось с 589,9 ± 25,9 до 522,4 ± 21,6 мс (p < 0,001; табл. 4).
Таблица 4
Влияние курсового лечения ноофеном на показатели сенсомоторной реакции и моторного темпа у больных БП
|
Показатели, мс |
До лечения ноофеном |
После лечения ноофеном |
|
Моторный темп (интервал между нажатием клавиш) |
589,9 ± 25,9 |
522,4 ± 21,6** |
|
Время сенсомоторной реакции |
394,5 ± 26,2 |
316,8 ± 7,1* |
* – p < 0,01; ** – p < 0,001
Состояние мнестических функций. Результаты настоящего исследования показали, что ноофен обладает выраженным ноотропным эффектом. Это подтверждается высокодостоверным улучшением показателей по шкале MMSE и тестом запоминания 10 слов Лурия (табл. 5). Суммарный балл по шкале MMSE после лечения повысился с 26,92 ± 0,48 до 29,44 ± 0,18 балла (p < 0,001). Рост суммарного балла после приема ноофена по шкале MMSE был обусловлен повышением показателей в частях шкалы, определяющих память и внимание.
Таблица 5
Динамика когнитивных функций у больных болезнью Паркинсона в результате курсового применения ноофена
|
Показатели |
До лечения ноофеном |
После лечения ноофеном |
|
Суммарный балл шкалы MMSE |
26,92 ± 0,48 |
29,44 ± 0,18* |
|
Память по шкале MMSE |
1,68 ± 0,18 |
2,56 ± 0,12* |
|
Внимание по шкале MMSE |
4,16 ± 0,20 |
4,96 ± 0,04* |
|
Суммарный балл теста Лурия |
35,92 ± 1,30 |
41,64 ± 0,97* |
|
Первый ответ по тесту Лурия |
5,12 ± 0,36 |
6,92 ± 0,33* |
|
Отсроченный ответ по тесту Лурия |
5,56 ± 0,49 |
7,28 ± 0,37* |
* – p < 0,001
Еще более выраженный эффект после приема ноофена был установлен при проведении теста Лурия на запоминание 10 слов. Суммарный балл этого теста увеличился с 35,92 ± 1,30 до 41,64 ± 0,97 (p < 0,001). Улучшилась как кратковременная так и долговременная память.
Оценка психоэмоционального статуса (депрессия, тревожность). После курса приема ноофена у больных отмечалось заметное улучшение психоэмоционального состояния (табл. 6). Уменьшилась степень депрессии – средние баллы по шкале Бека до и после лечения составили 17,65 ± 1,88 и 14,76 ± 1,92 (p < 0,05). Также уменьшилась тревожность, как ЛТ, так и СТ. С достоверностью p < 0,01 изменилась СТ – с 52,96 ± 1,59 балла до 47,54 ± 2,06 балла после приема Ноофена. ЛТ, которая считается более валидной частью шкалы, уменьшилась с 54,83 ± 1,70 балла до 49,33 ± 2,11 балла при ещё более высокой степени достоверности (p < 0,001).
Таблица 6
Улучшение психоэмоционального статуса больных болезнью Паркинсона в результате курсового применения ноофена
|
Показатели |
До лечения ноофеном |
После лечения ноофеном |
|
Балл по шкале Бека |
17,65 ± 1,88 |
14,76 ± 1,92* |
|
Балл по шкале Спилбергера, СТ |
52,96 ± 1,59 |
47,54 ± 2,06** |
|
Балл по шкале Спилбергера, ЛТ |
54,83 ± 1,70 |
49,33 ± 2,11*** |
– p < 0,05; ** – p < 0,01; *** – p < 0,001;
На фоне приема Ноофена мы также отмечали уменьшение болевого синдрома (не связанного с БП), нормализацию сна, настроения, уменьшение головокружения, метеозависимости, повышался уровень интереса к жизни, работоспособность, появлялось более адекватное отношение к себе и к своему заболеванию.
Итогом проведенных исследований эффективности курсового лечения ноофеном у больных БП явился анализ динамики отдельных клинико-физиологических показателей относительно исходного уровня (см. рис.).
Болезнь Паркинсона (БП) – хроническое прогрессирующее нейродегенеративное заболевание ЦНС, ведущими клиническими симптомами которого являются нарушения двигательной активности (акинезия, ригидность, тремор), к которым впоследствии присоединяются постуральные, когнитивные, психоэмоциональные и вегетативные расстройства.
Распространенность БП по данным мировой статистики составляет 60–187 случаев, а в Украине – 133 на 100 тыс. населения [1,2].
Согласно современным данным БП считают болезнью нейромедиаторного обмена [3, 4]. Специфической биохимической особенностью заболевания является недостаточность продукции дофамина (ДА) в базальных ганглиях и развитие дофадефицитарного дисбаланса в нигростриатной системе головного мозга.
К облигатным симптомам паркинсонизма относят и депрессивные расстройства, которые выявляются у 40–90 %, а изменения настроения – приблизительно у 40–50 % больных. Депрессия обычно возникает в самом начале болезни, предшествуя появлению двигательных нарушений [5] и проявляется в дисфории и грусти, гипертрофированном чувстве собственной вины перед близкими людьми [6].
Когнитивные нарушении считаются вторым по частоте коморбидным состоянием при БП. По данным некоторых авторов [7], риск развития деменции у пациентов с БП в 6 раз выше, чем в соответствующей возрастной группе людей, не страдающих этим заболеванием. При этом вероятность развития деменции с возрастом резко увеличивается.
Уже на ранних стадиях заболевания у большинства пациентов находят нарушения памяти, снижение быстроты планирования действий, а на поздних — возрастает частота дементных нарушений – от 40 % до 80 % [8]. Недостаточность когнитивных функций оказывает существенное влияние на выраженность двигательных нарушений, степень инвалидизации больных, их социальную адаптацию, поэтому применение ноотропных препаратов, улучшающих интеллектуально-мнестические способности, оказывает потенцирующее влияние на эффективность базисной патогенетической терапии.
В ряду ноотропных препаратов достойное место занимают препараты γ-аминомасляной кислоты, и в частности НООФЕН. Спектр клинической эффективности ноофена достаточно широк, поскольку этот препарат сочетает ноотропное и транквилизирующее действие. Ноофен улучшает память, интеллектуальную активность, повышает устойчивость мозга к вредным воздействиям, обладает противосудорожными, седативными свойствами, а также оказывает стабилизирующее действие на вегетативные функции. У лиц пожилого и старческого возраста, особенно на фоне дисциркуляторной энцефалопатии и других проявлений сосудистой патологии, ноофен эффективно влияет на частоту и выраженность симптомов ажитации, страха, тревоги, психомоторного возбуждения; у больных появляется более адекватное отношение к себе и окружающим, повышается уровень интереса к жизни, улучшается сон [10].
Основное ноотропное действие препарата основано на антигипоксическом действии, повышении энергетических ресурсов, активации метаболических процессов, улучшении функциональных особенностей нейронов [9–11]. Ноофен нормализует соотношение аэробных и анаэробных процессов, способствует повышению уровня глюкозы в крови и тканях мозга, увеличивает содержание макроэргических фосфатов в структурах ЦНС [12–13].
Благодаря взаимодействию между ГАМК- и дофаминергической нейромедиаторными системами, особенно в стриатуме, ноофен стимулирует дофаминергические процессы и, что особенно важно с практической точки зрения, усиливает действие противопаркинсонических препаратов [14].
Следует полагать, что Ноофен является патогенетически значимым при дофаминергической недостаточности, свойственной паркинсонизму.
Целью настоящего исследования было оценить эффективность курсового применения ноофена, производства Olain Farm (Латвия) у больных БП на фоне базисной терапии заболевания для улучшения двигательной активности, когнитивных функций и психоэмоционального состояния пациентов.
Было обследовано до и после курсового применения ноофена 25 больных БП (12 мужчин и 13 женщин) в возрасте 51–75 лет, средний возраст 61,5 ± 1,3 лет со стадией заболевания 1,5–3,0 (по Hoehn a. Yahr). Средняя продолжительность болезни составляла 4,87 ± 2,72 лет (табл. 1).
Базисная терапия у больных БП оставалась неизменной в течение 1 месяца до начала курсового приема ноофена и на протяжении всего курса приема препарата.
Курсовое лечение ноофеном было про ведено в условиях стационара Центра пар кинсонизма Института геронтологии в режиме дозирования – 1 таблетка (250 мг) препарата 3 раза в день (750 мг/сутки), в течение 21 дня.
Для объективного исследования двигательной активности мы использовали: унифицированную международную рейтинговую шкалу оценки двигательной активности (Unified Parkinson’s Disease Rating Scale – UPDRS), компьютеризированную электромиографию (ЭМГ), время (латентный период) сенсомоторной реакции и моторный темп.
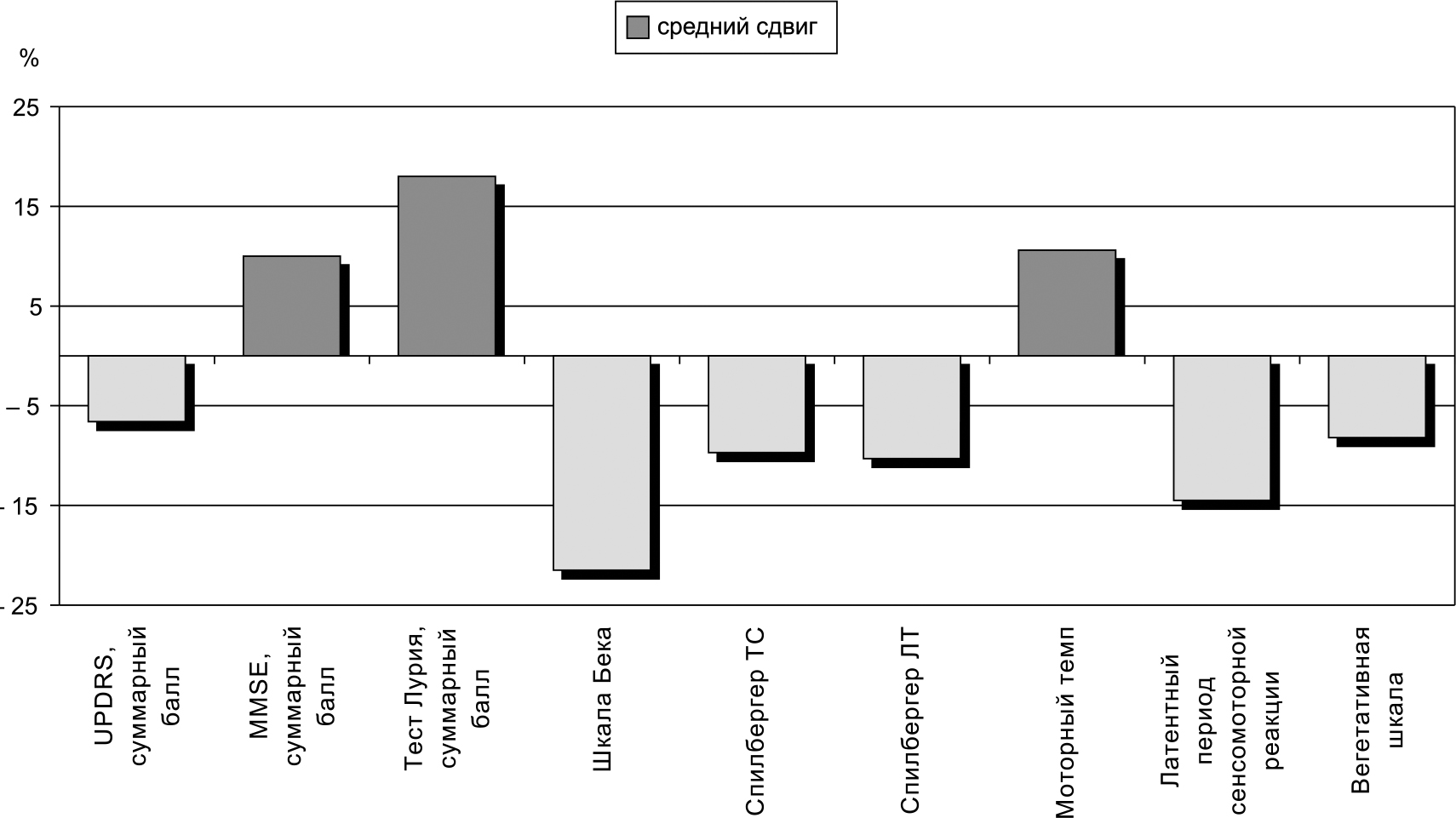
Изменения клинических показателей после приема Ноофена относительно исходного уровня ( %)
Улучшение двигательной активности подтверждалось снижением баллов по шкале UPDRS, уменьшением времени сенсомоторных реакций, повышением моторного темпа, улучшением показателей ЭМГ.
Выявлено выраженное ноотропное действие препарата, что подтверждалось высокодостоверным улучшением показателей по шкалам MMSE и тесту Лурия.
Ноофен оказывал благоприятное влияние на психоэмоциональный статус больных в виде снижения депрессии, уменьшения личностной и ситуационной тревожности.
Аналогичные данные были получены другими авторами при использовании Ноофена при других заболеваниях [10, 16–19].
Способность Ноофена улучшать двигательную активность, когнитивные и психоэмоциональные функции при БП, основана не только на тесной связи ГАМК-ергической системы мозга с другими нейромедиаторными системами (например, дофаминергической), а и наличием в молекуле ноофена бета-фенилэтиламина – вещества, которое является физиологическим модулятором дофаминергической нейромедиации. Бета-фенилэтиламин стимулирует высвобождение и тормозит обратный захват дофамина, тем самым усиливая дофаминергические влияния [15, 20]. Это представляется особенно важным, поскольку значительное снижение концентрации дофамина в ЦНС при старении и нарушение дофаминергической медиации являются одним из основных факторов старения мозга в целом и развития таких форм возрастзависимой патологии как БП, депрессия, когнитивные нарушения [21–23].
Полученные данные позволяют рекомендовать курсовой прием ноофена в комплексной патогенетической терапии болезни Паркинсона в качестве эффективного ноотропного средства, существенно улучшающего мозговые функции и, как следствие, замедляющего процесс прогресса заболевания.
Список литературы
1. Marttila R. J. Diagnosis and epidemiology of Parkinson’s disease // Acta Neurologica Scandin. – 1983. – Vol. 68. – Р. 9–17.
2. Московко С. П. Эпидемиология паркинсонизма в украинской популяции (Подольский регион) // Матер. II Украинского симпозиума с междунар. участием Экстрапирамидные заболевания и возраст. – К., 2004. – С. 56–58.
3. Mizuno Y. Concept and diagnostic criteria of Parkinson’s disease and parkinsonism // Nippon Rinsho. – 1997. – Vol. 55(1). – P. 16–20.
4. Olanow C. W., TattonW. G. Etiology at pathogene sis of Parkinson’s disease // Ann. Rev. Neurosci. – 1999. – Vol. 22. – Р. 123–144.
5. Хаасс А. Новые аспекты терапии болезни Паркинсона // Журнал невропатологии и психиатрии им. Корсакова. – 2001. – № 5. – С. 54–55.
6. Крыжановский Г. Н., Карабань И. Н., Магаева С. В. и др. Болезнь Паркинсона (этиология, патогенез, клиника, диагностика, лечение, профилактика). – М.: Медицина, 2002. – 336 с.
7. Aarsland D., Andersen K., Larsen J. P. et al. Risk of dementia in Parkinson’s disease: A community-based prospective study // Neurology. – 2001. – 56. – 6. – P. 730–736.
8. Emer M. Dementia associated with Parkinson’s disease // Lancet Neurol. – 2003. – Vol. 2. – P. 229–237.
9. Бурчинский С. Г. Препарат ноофен (Фенибут): властивості, перспективи застосування та місце серед ноотропних засобів // Ліки. – 2002. – № 1–2. – С. 1–4.
10. Хаунина Р. А., Лапин И. П. Применение фенибута в психиатрии и неврологии и его место среди других психотропных средств // Журнал невропатологии и психиатрии им. Корсакова. – 1989. – Т. 89. – № 4. – С. 142–151.
11. Ковалев Г. В. Ноотропные средства. – Волгоград: Ниж.-Волжск. кн. изд-во. – 1990. – 368 с.
12. Мехилане Л. С., Ряго Л. К., Алликметс Л. Х. Фармакология и клиника фенибута. – Тарту: Изд-во ТГУ, 1990. – 148 с.
13. Громов Л. Фармакологічний профіль дії ГАМК-ергічних препаратів в ряду психотропних засобів // Вісник фармакології та фармації. – 2001. – № 11.
14. Гольдблат Ю. В., Лапин И. П. Усиление фенибутом лечебного действия антипаркинсонических средств // Журнал невропатологии и психиатрии им. Корсакова. – 1986. – № 8. – С. 1146–1148.
15. Лурия А. Р. Основы нейропсихологии. – М.: Изд-во Моск. ун-та, 1973. – 373 с.
16. Поворознюк В. В., Орлик Т. В. та співавт. Лікування вертебрального больового синдрому при остеохондрозі шийно-грудного відділу хребта в жінок із клімактеричними розладами // Проблеми остеології. – 2003. – Т. 6, № 4. – С. 4–10.
17. Лукач О. И., Кузнецов В. В. Влияние ноофена на психоэмоциональную деятельность и церебральную гемодинамику у больных, перенесших ишемический инсульт // Український вісник психоневрології. – 2003. – Т. 11, вип. 2(35). – С. 24–26.
18. Горохов Е. А., Мокроусова Т. Н., соавт. Лечение фенибутом при сосудистом поражении вестибулярного анализатора // Современная медицина. – 1988. – № 8.
19. Дубенко А. Е. Использование ноофена в качестве ноотропного препарата у больных эпилепсией // Український вісник психоневрології. – 2003. – Т. 11, вип. 2(35). – С. 13–15.
20. Шток В. Н., Федорова В. Н. // Consilium Medicum. – 2002. – № 5. – С. 14–23.
21. Фролькис В. В. Старение мозга. – Л.: Наука, 1991. – 277 с.
22. Крупина Н. А., Крыжановский Г. Н. Недостаточность дофаминергической нигростриатной системы как дизрегуляционный механизм дофаминзависимого депрессивного синдрома // Журнал невропатологии и психиатрии им. Корсакова. – 2003, № 4. – С. 42–47.
23. Литвиненко И. В., Одинак М. М. Патогенетические основы формирования когнитивных и психотических нарушений при болезни Паркинсона // Там же. – 2004, № 4. – С. 72–76.
Надійшла до редакції 19.10.2005 р.
І. М. Карабань, О. П. Луханіна,
Н. О. Мельник, Н. М. Березецька
Вплив курсового лікування Ноофеном на рухову активність,
когнітивні функції та психоемоційний стан у хворих на хворобу Паркінсона
Інститут геронтології АМН України,
Інститут фізіології ім. О. О. Богомольця НАН України,
Інститут фізики НАН України (м. Київ)
Хвороба Паркінсона (ХП) проявляється не тільки прогресуючим руховим дефіцитом, але й комплексом когнітивних та психоемоційних розладів. З метою вивчення ефективності Ноофена в комплексній патогенетичній терапії ХП обстежено 25 пацієнтів віком 49–75 років, зі стадією хвороби 1,5–3,0 по Hoehn a. Yahr. Препарат призначався в дозі 250 мг 3 рази на добу протягом трьох тижнів. Визначали динаміку рухової активності, вираженість когнітивних та психоемоційних порушень. Ноофен достовірно покращував клінічну симптоматику, показники електроміограми, час рухової реакції, пам’ять, зменшував депресію та тривожність.
I. N. Karaban, E. P. Lukhanina,
N. A. Melnik, N. M. Berezetska
Influence of course treatment with Noofen on the motor activity,
cognitive functions and psychoemotional condition in Parkinson disease patients
Institute of Gerontology of the AMS of Ukraine;
A. A. Bogomolets Institute of Physiology of the NAS of Ukraine;
Institute of Physics of the NAS of Ukraine (Kyiv)
The Parkinson’s disease (PD) manifests itself not only by a progressive motor deficit but also by a complex of cognitive and psychoemotional disturbances. This work aimed to study the effectiveness of drug Noofen in complex pathogenetic therapy of PD patients. The study involved 25 patients, age 49–75 years, who suffered from PD, 1.5–3.0 stage according to Hoehn a. Yahr. The drug Noofen was administered in a dose 250 mg three times daily during 3 weeks. The dynamics of motor activity, and the pronouncement
of cognitive and psychoemotional changes were assessed. The findings point to statistically significant improvements, owing to Noofen treatment, in the clinical symptomatics, electromyogram indices, motor reaction time and memory. The conditions of depression and anxiety were likewise reduced.

